11月4日,根据CDE官网显示,乐普生物普特利单抗注射液(HX008)新适应症上市申请结束公示期,正式纳入优先审评,适应症为:用于既往接受一线及以上系统治疗失败的高度微卫星不稳定型(MSI-H)或错配修复缺陷型(dMMR) 的晚期实体瘤患者的治疗。这是该产品继二线治疗黑色素瘤之后,申报的第二个适应症。
MSI-H/dMMR是在实体瘤中广泛存在的一种突变,2016 年,Ronald J Haus 等人利用全基因组外显子测序方法,分析发现 MSI-H 在 18 种癌症均有出现,在所有癌种中的发生率约为 14%,其中子宫内膜癌的发生率接近 30%,结肠腺癌、胃癌的发生率均为 19% 左右。2017 年,美国 FDA 率先批准了 PD-1 K药治疗MSI-H/dMMR的实体瘤患者。打破了既往我们一直按照不同肿瘤来源治疗的理念,通过按照生物标志物的情况分类进行免疫治疗,让更多肿瘤患者,尤其是晚期患者更多治疗的希望。
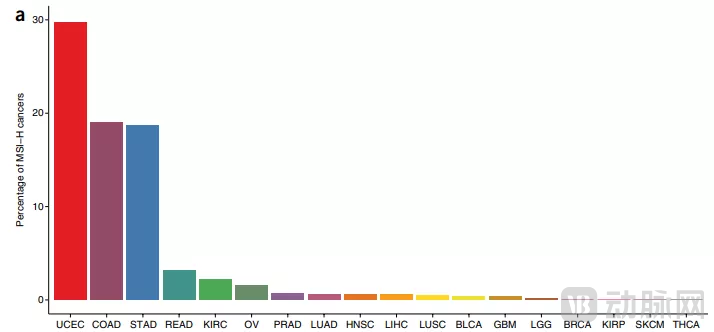
MSI-H/dMMR在18个癌种分布比例
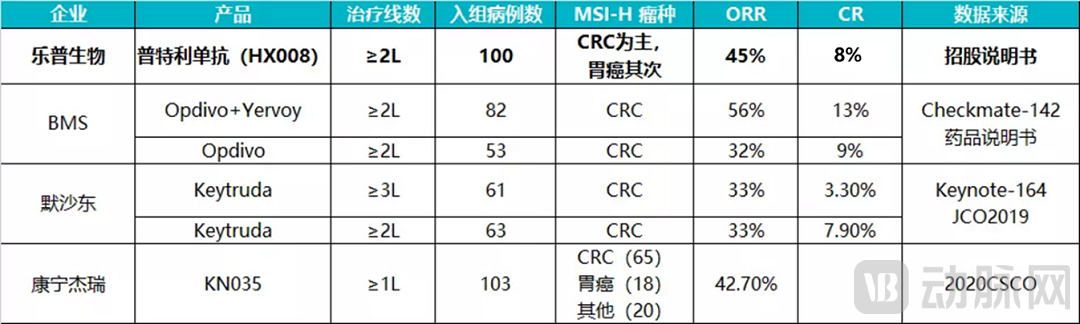
根据此次乐普生物普特利单抗递交的一项在MSI-H/dMMR晚期实体瘤患者中开展的关键性 II 期临床研究结果,截至2021年6月3日,患者的客观缓解率(ORR)为46.0%,完全缓解率(CR)为8%。疾病控制率(DCR)为70.0%,中位无进展生存期(mPFS)尚未达到,12个月无进展生存比例为55.1%。中位OS尚未达到,6个月、9个月、12个月的OS率分别为86.0%、79.4%和76.6%。虽然缺少头对头的对比,但在现有文献证据下,如下表所示,普特利单抗单药治疗 MSI-H 实体瘤已经体现了较为突出的疗效。
据统计,国内一些常见癌种中每年新发 MSI-H 的实体瘤患者数量约为 31.2 万人,与每年新发乳腺癌病例数相当,以患者总数及药物治疗 MSI-H 肿瘤患者比例等计算,预计 2030 年,MSI-H/dMMR 实体瘤潜在用药人数预计可以达到 18.7 万人。目前,国内外仅获批了 3 款抗 PD-1 单抗用于治疗 MSI-H/dMMR 肿瘤,包括普特利单抗在内,共有3款国产 PD-1/PD-L1 已经提交上市申请,尚未有药物正式获批,展现出令人期待的市场开发潜力。
值得关注的是,除PD-1产品外,乐普生物还致力于开发具有高度差异化竞争优势的创新型 ADC 管线及溶瘤病毒产品,积极探索联合疗法,为患者提供更优的治疗方案。在此前结束的欧洲肿瘤内科学会(ESMO)年会上,由中山大学肿瘤防治中心徐瑞华教授和同济大学附属东方医院李进教授分别领衔的两款ADC药物——MRG003和MRG002的I期临床研究同时入选ESMO ePoster,展示了乐普生物在ADC药物领域的深厚积累和创新能力。此次,普特利单抗接连两个适应症的 NDA 申请获受理也为乐普生物布局的 PD-1 联合治疗奠定基础,根据 ASCO 和 CSCO 上免疫联合化疗/靶向或免疫联合 ADC 前期临床数据的公布,使得免疫联合 ADC 产品的机制逐渐被验证,乐普生物将通过普特利单抗联合 ADC 药物为肿瘤患者后续的联合治疗提供新的方向。




























