复制、剪切、粘贴,生命的字符就是如此朴实无华。
在实现基因的“读”之后,对遗传密码的“写”成为基因组学研究的下一个方向。早在1996年,第一代技术ZEN就为人们打开了基因编辑的大门,然而包括TALEN在内的前两代技术都没有办法实现精准编辑、解决脱靶问题,直到CRESPR技术的出现。
2014年,加州大学伯克利分校、哈佛大学、麻省理工大学的科学家们创造了CRESPR技术。该技术的诞生改写了科学家们对遗传工程的理解,使得基因的编辑成为了轻松且精确的事情。
在这之后,基因编辑就成为了一把精准“魔剪”,CRESPR技术也一跃成为成为全球领域的投资热点,不仅吸引了Jennifer Doudna、Emmanuelle Charpentier、Geroge Church 、张锋等技术大牛进行创业,同时也让辉瑞、诺华等跨国药企争相布局,盖茨基金会、谷歌风投、ARCH Venture等全球一流投资机构更是持续重仓。
如果遗传物质比作一本书,那么基因编辑就是书中对一个个文字,基因编辑就是修改里面对某个字、某句话,甚至整段话。在这项技术对推动下,基于基因编辑对各项应用研究得以飞速发展,研究方向覆盖医疗、农业、环境、海洋等领域。2021年,Allied Market Research曾指出全球基因编辑产业规模将在2030年将超过360亿美元,约合人民币2448亿元。。
在医疗领域,包括但不限于细胞治疗、基因治疗、再生医学、异种移植、合成生物学等等,针对肿瘤免疫、眼科疾病、器官衰竭的颠覆性疗法出现。每一个细分领域,都是近些年全球医疗投资的热门风向。
谈及基因编辑在医疗中的应用,首先想到的自然是癌症的治疗。比如2018年,诺华和宾夕法尼亚大学团队利用嵌合抗原受体T细胞免疫疗法(CAR-T)成功治愈一名患有白血病的女孩Emily。
这一类通过基因编辑手段,对人体免疫细胞进行改造和增强对方法叫做细胞免疫疗法。其治疗过程大致是从人体内分理处具有活力的免疫细胞,在体外进行改造(或不改造)和扩增后在回输到病人体内。这些回输的细胞具备更强的免疫力,能够给予癌细胞更强的打击,从而达到疾病治疗的目的。除了前文提到的CAR-T细胞,类似的还有TIL细胞治疗、TCR-T细胞治疗、CAR-NK细胞治疗等选择。
1CAR-T细胞疗法
作为国际上研究最为火热的肿瘤免疫治疗方法, CAR-T疗法在白血病、淋巴瘤、多发性骨髓瘤的治疗中展现出惊艳的治疗效果。目前全球一共有8款CAR-T治疗产品上市,这些产品主要针对CD19和BCMA两个靶点。此外,全球范围内等一众公司也在积极探索CD123、CD33等新靶点,对应等研发管线也在迅速扩张,目前全球已经有多家公司等实体瘤项目推进到临床晚期阶段。
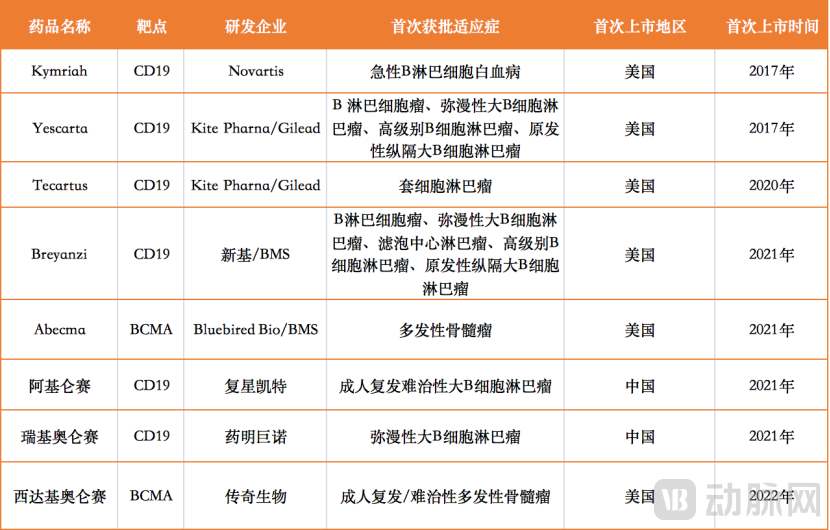 全球已上市的 CAR-T细胞治疗产品,数据来自动脉橙
全球已上市的 CAR-T细胞治疗产品,数据来自动脉橙
2TCR-T 细胞疗法
通过筛选和鉴定能够特异性结合靶点抗原的TCR序列,采用基因工程手段将其转入到患者外周血来源的 T 细胞中( 或异源 T 细胞) ,再将改造后的T细胞回输至患者体内,使其特异性识别和杀伤表达抗原的肿瘤细胞,从而达到治疗肿瘤的目的。
目前基于TCR-T的实体瘤研究包括肝癌、卵巢癌、胶质母细胞瘤、肺癌和间皮瘤等。目前全球范围内获批上市的TCR-T 细胞疗法仅一款,即Immunocore公司研发的免疫疗法Kimmtrak,该疗法被批准用于HLA-A*02:01 阳性的无法切除或转移性葡萄膜黑色素瘤(mUM)成人患者。此外,Adaptimmune、TCR2 Therapeutics等公司也备受关注。
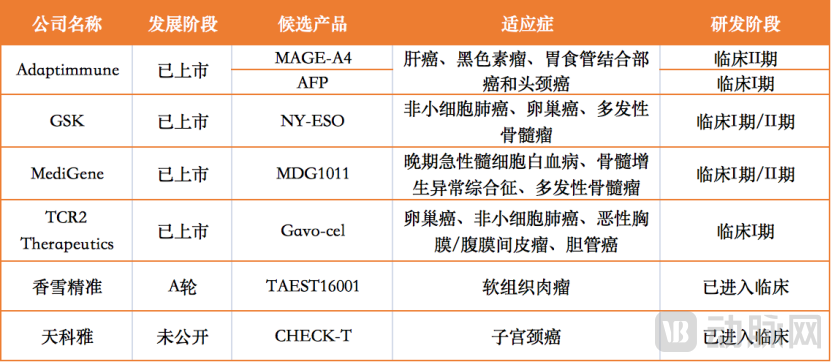 全球领域 部分TCR-T细胞治疗产品,数据来自动脉橙
全球领域 部分TCR-T细胞治疗产品,数据来自动脉橙
3TIL 细胞疗法
在肿瘤组织内浸润了大量 T细胞,这些细胞中存在部分针对肿瘤特异性抗原的T细胞,是能够深入肿瘤组织内部杀伤肿瘤的免疫细胞。基于这一特性,TIL 疗法将肿瘤组织中的 T 细胞分离出,在体外进行刺激扩增后,回输到患者体内,从而扩大免疫应答,治疗原发或继发肿瘤。
与其他细胞免疫治疗不同,TIL 疗法不需要对免疫细胞进行改造。新一代TIL疗法增加了定向筛选过程,确保只扩增识别肿瘤细胞的免疫细胞。TIL不仅分离出的免疫细胞更对口,而且扩增的时候会再筛选,确保只留下针对癌症的免疫细胞。
TIL疗法目前主要作为二线治疗进行临床试验。其中,Iovance Biotherapeutics的LN-145处于临床II期阶段,该产品在2019年被FDA授予突破性疗法,用于治疗复发性转移性或持续性宫颈癌。这一领域,国内亦生机勃勃。
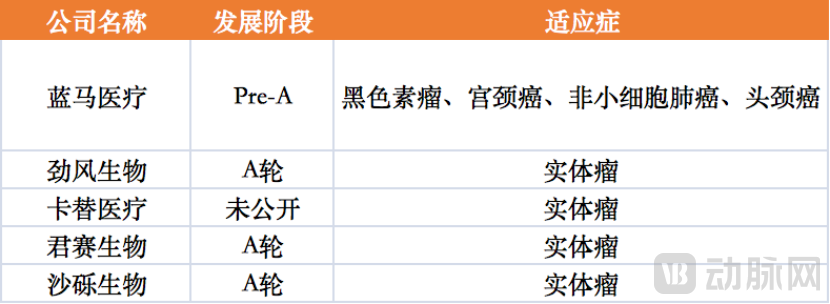
国内部分TIL细胞治疗企业,数据来自动脉橙
4CAR-NK 细胞治疗
NK 细胞即自然杀伤细胞,具有强力杀伤肿瘤细胞的能力,且不具 MHC 限制性。CAR-NK 过继细胞疗法是指将 NK 细胞经过 CAR 基因修饰,赋予 NK 细胞靶向识别肿瘤细胞的能力,经过体外扩增后注入人体从而达到肿瘤治疗的效果。目前临床上使用的 NK 细胞主要有五种来源:人外周血、脐带血、人胚胎干细胞、诱导多能干细胞以及 NK-92 细胞系。
相较于CAR-T细胞疗法,CAR-NK有以下几点优势:
1、来源更广,更加适合进行体外培养和基因改造,有潜力开发异体来源的细胞治疗产品;
2、对于MHC表达下调的细胞,NK依然可发挥杀伤作用,实体瘤方面更有优势;
3、安全性异体输注基本不会引发GVHD,细胞因子风暴发生的风险较低;
4、CAR-NK制作过程更加简单,有望实现大规模工业化生产。
目前,无论是中国、日本还是美国,NK细胞培养技术都已经非常成熟。
 全球领域部分 CAR-NK细胞治疗产品,数据来自动脉橙
全球领域部分 CAR-NK细胞治疗产品,数据来自动脉橙
目前大部分细胞治疗产品都是利用患者自身细胞来进行改造和扩增,属于个体化产品。然而患者之间存在个体差异,定制细胞是一个昂贵且耗时的过程。因此,为了提高灵活性,科学家和产业界一致的解决方案是探索通用型细胞治疗产品。CAR-NK细胞治疗产品在实现工业化生产上的潜力也让它成为CAR-T细胞治疗大势初定后,各家争夺的新赛道。
不过,CAR-NK走向更大规模的应用还有几个技术难点需要攻克。比如NK细胞体外扩增培养比较困难,需要摸索合适的培养条件。同时,现有的CAR设计是从CAR-T疗法延用而来,针对NK细胞的CAR还需要开发。另外NK 细胞对冻融过程敏感以及对基因工程的抗性也是需要关注和解决。这些问题的突破或将基于NK细胞优秀的抗肿瘤血统,为在CAR修饰的武装下为肿瘤治疗带来新的突破。
遗传疾病在某一种程度上也被成为基因病,大多说遗传学疾病来自繁衍过程中,DNA的延续。针对遗传疾病治疗主要包括了人类生殖系统的基因编辑和体细胞基因编辑。其中,针对人类生殖系统的基因编辑存在较多争议,这种改造影响的不仅仅是单独个体,这些改变可能随着个体的繁衍代相传,改变人类的遗传轨道。
(目前,针对生殖系统的基因编辑研究主要针对严重遗传病,如囊肿性纤维化、亨廷顿舞蹈症或者戴萨克斯症。这些遗传病都会造成使人衰弱的症状,预后情况都很不理想,而且都是由单基因突变导致的。或许在一个基因编辑安全有效的时代,这些疾病完全可以预防。)
这里我们着重谈针对的体细胞基因编辑研究。基因编辑目前已经能够进行高频率的基因修正,因此理论上可以应用于造血系统和免疫系统的数百种遗传病(如镰状细胞病、X连锁重症联合免疫缺陷和X连锁慢性肉芽肿病)。
当前,基于基因编辑技术的基因治疗主要包括体外编辑回输体内和体内编辑两类。与传统基因治疗方法相比,基因编辑技术能在基因组水平上对DNA序列进行改造,从而修复遗传缺陷或者改变细胞功能,使得彻底治愈白血病、艾滋病和血友病等恶性疾病成为可能。目前,基因编辑在基因治疗中的应用主要聚焦单基因疾病和眼科疾病。
单基因遗传病是指受一对等位基因控制的遗传病,如beta-地中海贫血症、杜氏肌营养不良(DMD)、血友病等。针对单基因疾病的基因治疗,是通过将正常基因倒入弥补缺陷基因。
传统技术手段通常采用病毒载体实现基因导入,尽管病毒载体可以将所需的目的基因整合到基因组,持久表达以替代缺陷基因,仍存在较多安全性问题。基因治疗研究仍然需要具备特异性和高效修复能力的工具。CRISPR基因编辑技术的出现犹如雪中送炭(当然,这里还有诱导多能干细胞发挥的价值)。
眼球体积较小,需要的治疗载体较少。并缺,眼部区域具有免疫赦免,这既可避免外源性物质引起的炎症和免疫反应。由于眼球独特的生理构造,基于基因编辑的基因疗法在眼科疾病治疗上具有明显优势。
多种严重的眼科疾病与基因突变存在密切联系,因此,眼科疾病的治疗对基因编辑疗法具有强烈对市场需求。这为基因编辑疗在眼科疾病治疗中对率先应用创造了条件。目前,针对10型Leber先天性黑矇产品已经上市。
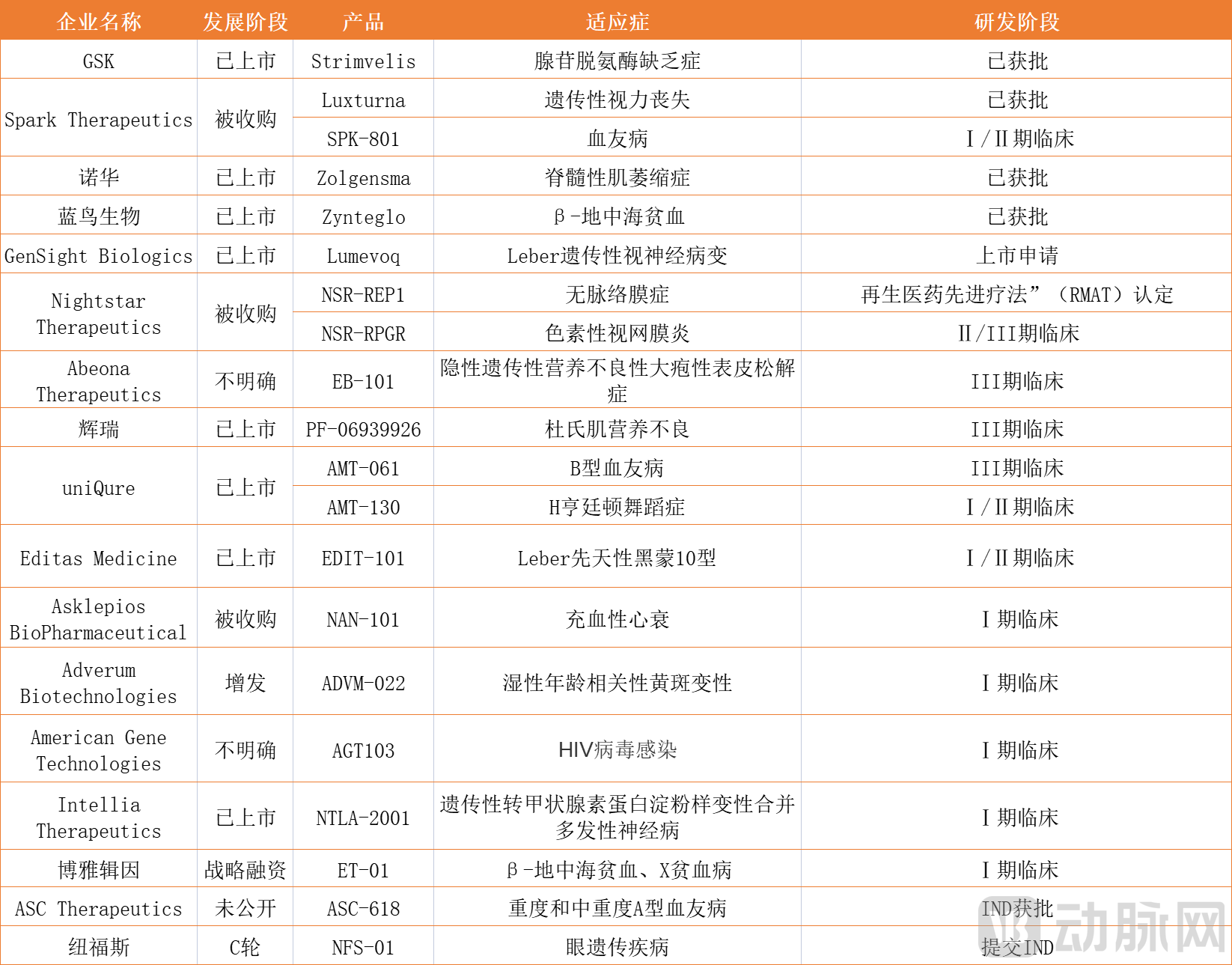
全球领域部分基因治疗产品,数据来自动脉橙
基因治疗药物通过两种方式发挥作用,一个是导入外源基因,一个是抑制内源基因,随着CRISPR基因编辑技术发发展和成熟,直接修复基因的基因编辑疗法,将为基因治疗带来全新的局面。
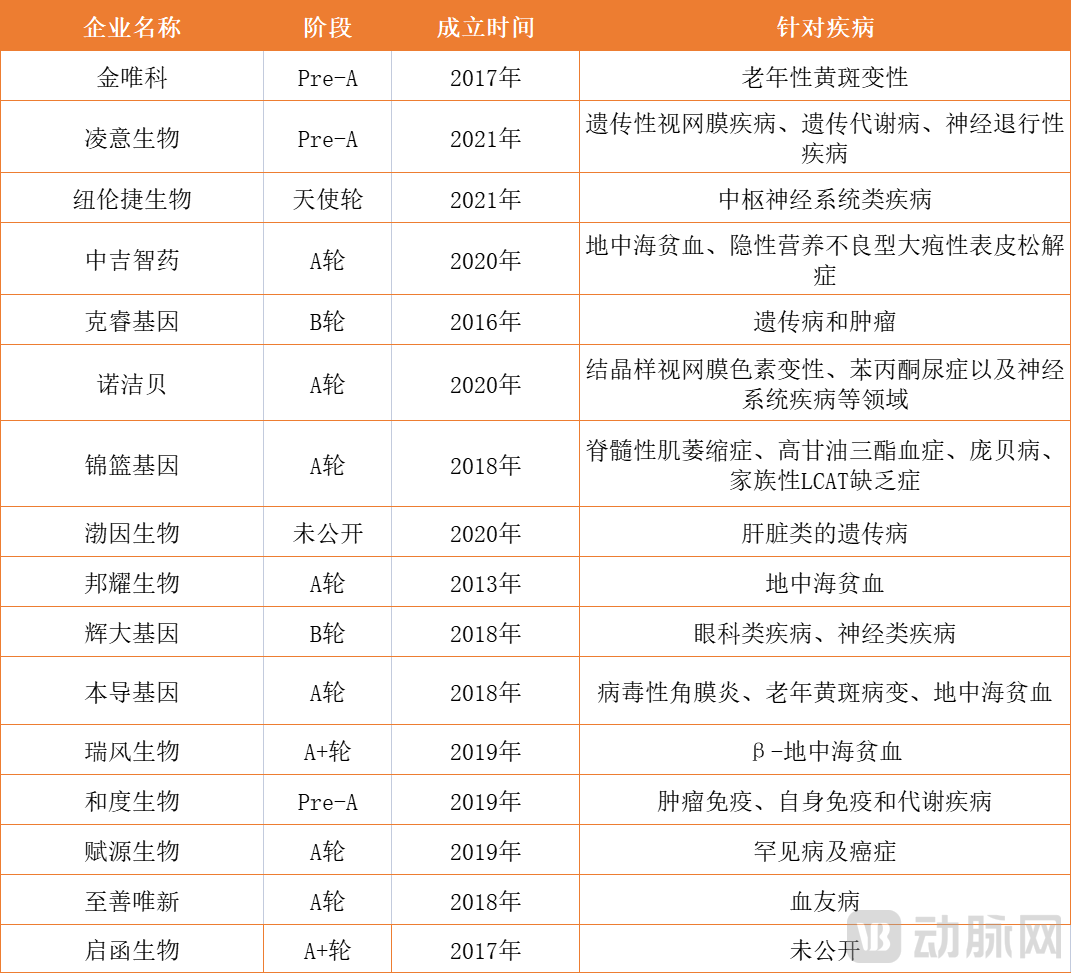 国内部分基因治疗创新企业,数据来自动脉橙
国内部分基因治疗创新企业,数据来自动脉橙
再生医学是根据组织的结构与功能,修复治疗受损组织器官的一门学科,其产生只在缓解器官不可逆损伤和移植组织器官紧缺的问题,并为疾病对治疗提供了新的思路。
再生医学研究中,稳定的细胞因子表达是组织器官再生的一个关键因素。目前,这一问题的解决方案是基因治疗,通过基因治疗产生种子细胞,从而持续稳定的分泌再生所需要的细胞因子,提供稳定的局部环境,最终实现组织修复效率的提高。
这是目前针对因细胞不可逆损伤而导致疾病的一种具有前景的治疗方案,具体的应用方向包括肝脏细胞、心肌细胞的修复。由于免疫排斥发生概率低、分化型号,且没有伦理问题,基于诱导性多能干细胞(Induced pluripotent stem cells,iPSCs)的再生医学研究被市场看好。
诱导性多能干细胞最初是日本科学家山中伸弥(Shinya Yamanaka)于2006年利用病毒载体将四个转录因子(Oct4, Sox2, Klf4 和c-Myc)的组合转入分化的体细胞中,使其重编程而得到的类似胚胎干细胞和胚胎APSC多能细胞的一种细胞类型。随后世界各地不同科学家陆续发现其它方法同样也可以制造这种细胞。
2012年10月8日,John B. Gurdon 与 Shinya Yamanaka 两位科学家因此获得诺贝尔生理学和医学奖。
iPS细胞的出现,在干细胞研究领域、表观遗传学研究领域以及生物医学研究领域都引起了强烈的反响。在基础研究方面,它的出现,让人们对多能性的调控机制有了突破性的新认识。
此外,iPS细胞在神经系统疾病、心血管疾病等方面的作用也日益呈现,iPS细胞在体外已成功地被分化为神经元细胞、神经胶质细胞、心血管细胞和原始生殖细胞等。在临床疾病治疗中具有巨大应用价值。
随着iPSC技术临床应用的逐步落地,日本作为iPSC的发源地快速推进了一系列由研究者发起的临床试验。而在iPSC疗法的商业化方面,美国目前则处于前列,多家企业均有产品进入临床试验阶段。
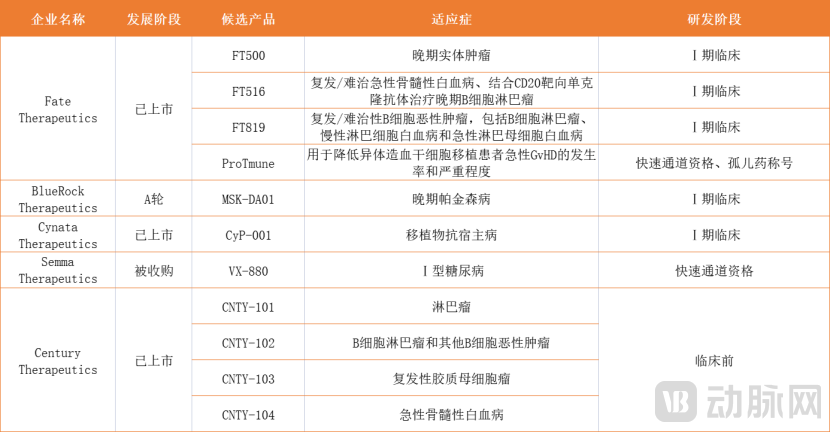
国外部分iPSC细胞治疗产品,数据来自动脉橙
其中,来自美国的Fate Therapeutics是全球iPSC细胞免疫治疗的领头羊。这家公司成立于2007年,并2013年于美国纳斯达克上市(NASDAQ:FATE)。在其上市的前七年,公司股价表现一直不温不火,2020年3月还曾陷入股价不足20美元的低谷期。可随后的不到一年时间中,Fate的股价持续上长,2021年1月14日Fate迎来了其股价的最高峰121.16美元,巅峰时期市值超过100亿美元。
国内,启函生物、霍德生物、艾尔普再生医学、士泽生物等,较快的产品已经逼近临床,并且各自的应用场景各有侧重,分别覆盖几个关键性的治疗领域。
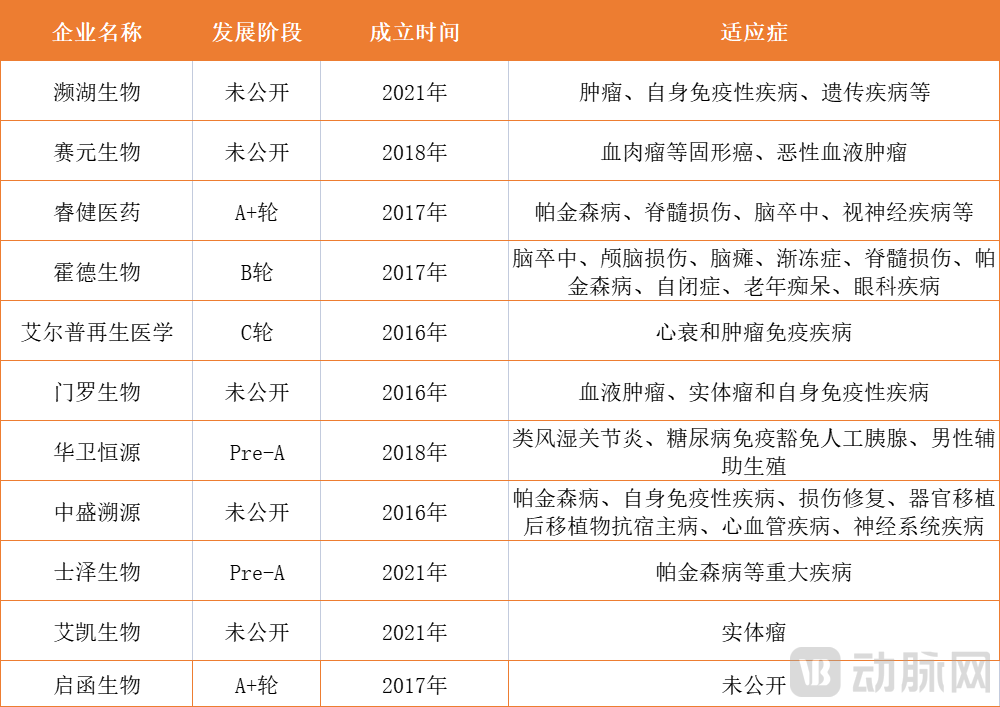
国内部分iPSC细胞治疗创新公司,数据来自动脉橙
在iPSC赛道上,国内外企业几乎没有太大差距。
再生医学领域另一发展路线则是异种移植。
当人体当某种器官遭受严重病变,器官移植往往是唯一延续生命的办法。但器官但合法来源只能依靠志愿者捐赠。全世界大约只有不到10%但患者能等到合适的器官,他们中的90%都只能在排队等候的过程中绝望而逝。
几十年前,有科学家提出了动物器官移植的假设,以此来克服供体紧缺的问题。由于器官组织结构、生理功能和大小与人类器官相近,猪被视为器官移植供体的最佳动物之一。但物种之间存在超急性排斥反应,如果直接将动物器官进行人体移植,患者势必会因超急性免疫反应死亡。
超急性排斥反应是物种保持种系延续的天然防御机制。数十年间,科学家们尝试研究一些药物来控制这一反应,但都没有取得成功。基因组学都发展使得人们能够从分子层面认识免疫排斥反应的发生,也为人们提供了解决异种移植免疫排斥反应的另一种思路。
猪的器官可能携带多种对人类致病对致病基因,且灵长类动物体内存在对一些抗体会对猪器官的某些蛋白进行攻击,从而导致免疫排斥反应。这两点是目前猪器官异种移植的技术障碍,如果从基因层面对这些致病基因和蛋白的表达基因进行剪切和修饰,是否实现安全且有效的异种移植?
然而猪体内约有100,000个基因,要在这些基因中寻找到需要的片段且精准编辑,则需要强大的基因编辑手段加持。无疑,CRISPR技术的出现再次让理想照进现实。
2022年1月7日,美国马里兰大学医学院完成全球首例转基因猪心脏移植手术,患者大卫·贝内特术后三天情况良好,实现由猪心脏泵血。贝内特在接受移植手术前已不支持人源心脏移植,于是手术得到了美国FDA的紧急授权。贝内特在2022年3月9日去世,尽管只延长了2个月的寿命,但在术后几周内,移植心脏都运转良好,没有出现排斥反应,他在临床前几个小时仍能与家人交流。
目前,马里兰大学医学中心尚未公布患者死因。但这一例手术证实了经过基因编辑的动物心脏在人体内可以正常运作,不会立即发生排异反应。对异种移植领域而言,这是划时代的医学进步。
除了心脏移植外,全球领域还有多项针对猪器官异种移植展开的研究和试验,主要研究方向包括胰岛、肝脏、肾脏异种移植。
合成生物学这一概念由波兰科学家W. Szybalski于1978年首次公开提出,它是将生物科学与工程学相结合的学科。20世纪90年代,基因组学与系统生物学逐渐兴起,为合成生物学的诞生奠定了技术基础。21世纪初,科学家们尝试在现代生物学与系统生物学的基础上引入工程学思想和策略,诞生了学科高度交叉的合成生物学,成为近年来发展最为迅猛的新兴前沿交叉学科之一。
合成生物技术是综合了科学与工程的一项崭新的生物技术,借助生命体高效的代谢系统,通过基因编辑技术改造生命体以设计合成,使得在生物体内定向、高效组装物质和材料逐步成为可能,该技术应用于生物材料、生物燃料、生物医药等多个领域。
生物合成法通常通过对现有生物系统的改造,或者从头人工合成基因组并重构生命体的方式来得到新的代谢途径,并通过这个新的代谢途径来得到新的代谢产物。从理论上看,通过生物合成技术可以合成绝大多俗化合物,甚至还可以合成传统化工法不能合成的新材料。在医疗领域,这项技术被用于获得医药原材料、催化剂、中间体等。
在这个场景中,大麻素是全球领域的合成热点。全球约有40家从事生物合成大麻素的企业,根据大麻市场研究公司New Frontier Data 的一项新分析,全球大麻消费市场价值3440亿美元。大麻素市场增长的一个关键原因在于大麻素的其他价值(例如医用价值)正在越来越多被应用,而以发酵合成生物学方式进行低成本和高纯度生产大麻素的公司将拥有更多机会。
另一面,而医药中间体也是合成生物学在医疗场景下最主要的应用之一。弈柯莱生物、酶赛生物、百葵锐生物在国内都有从事医药中间体的开发,其中弈柯莱生物开发的丁酸作为西格列汀开发的中间体,西格列汀是一种口服降糖药(抗糖尿病药);另外开发的2,4-二氟苄胺则作为热门的抗艾滋病药物度鲁特韦的中间体,已经列入WTO、盖茨基金会等慈善机构的采购目录。同时,弈柯莱生物与酶赛生物除了自主开发医药中间体外,也提供相应的生物催化领域的定制研发服务。
此外,中国另外一家合成生物学公司华恒生物则专精于生物合成各种小品种氨基酸产品,其中以丙氨酸为代表的系列产品其生产规模已经位居国际前列。这种以微生物细胞工厂为核心的发酵法生产工艺替代了传统化学合成工艺的重污染生产方式,生产成本更低,生产过程更为安全、绿色、环保。
由于合成生物技术更多围绕微生物、细菌展开,所以在生物医药领域合成生物学的另一大应用场景聚焦于肠道菌群的“合成设计”。例如,美国生物技术公司Novome Biotechnologies通过对食品中常见的乳酸乳球菌进行工程设计,使其具备抗炎特性,作为控制克罗恩病和溃疡性结肠炎等疾病的有效治疗方案。
当然,合成生物学领域也面临两个难点。第一点是上下游产业链的打通,这一点可以参考华熙生物。
华熙生物母在1998年便实现了透明质酸的生物合成,最早原料生产为主要业务。成立之初,公司前后投入近千万,一度处于持续亏损状态。2010年,华熙生物开始向下游产业链做相关产品的开发与延伸。公司先后“润百颜”、“润致”,“夸迪”、“米蓓尔”、“BM肌活”“黑零”、“水肌泉”、“海力达”、“海视健”等品牌,打通医美、医药、日化和功能性食品等下游产业链吗,最终成功构建起自己的“透明质酸王国”。
另一个难点则是技术上的工艺放大。细菌的获取和改造仅仅是生物合成的第一步,在发酵完成后,在一罐混合物中进行产品的分离提纯直接影响到产物的质量;对发酵程度和温度的控制直接影响发酵效率;从实验大小的发酵罐到工业发酵罐的方法生产.....这些都将是生物合成从小试、中试到大规模工业化必须迈过的门槛。
不过,在关键性技术突破和数十年研究的加持下,合成生物学在技术转化和产业化方面都取得了了不起的成就。尤其在生物制作和医疗应用方面,更是展示出了无与伦比的潜力。基于目前合成生物学的发展趋势,我们可以预见全球合成生物学产业集群的行成与壮大,以及对未来制造业的革新与颠覆。
以上为基因编辑作为工具类技术在医疗产业的部分应用。它的出现让人们多年以前关于DNA分子的设想走进现实,颠覆了人们对疾病的治疗、诊断的认知,对动物模型构建方式的理解,甚至还改变了人类“造物”的方式。在CRESPR技术诞生的不到十年间,人们对基因的改写从笨拙走向灵活,以至于人们用“上帝之手”来形容它。
不过,目前中国的基因编辑行业也面临比较明显的短板,即缺乏具备自主知识产权的基因编辑技术。基础科学的突破和取得核心专利是领域发展的关键,对基因编辑领域来说,也是如此。尽管近年来我国在基因编辑方面取得了长足进步,论文数量和专利数量均已居国际第二位,但与美、欧等发达国家和地区相比,我国基因编辑不仅存在原始创新缺位的尴尬。大部分研究都以基因编辑的应用研究为主,但从基因编辑技术本身到应用研究的公司和研究人员凤毛菱角。
此外,国内对基因编辑应用研究的伦理学、监督管理和法律法规也还需加强。应用研究的出发点应该是造福生态、造福患者,而不应该是个人的炫技和满足好奇心。我们很难想象这项技术的天花板在哪里,但可以肯定的是,我们需要时刻铭记——科技一直都是把双刃剑。




























