2022年6月5日,新加坡细胞治疗公司Tessa Therapeutics(以下简称为Tessa)宣布完成1.26亿美元的A轮融资。此次融资由Polaris Partners领投,Temasek、EDBI、Heliconia Capital和Heritas Capital跟投。同时,Polaris Partners的管理合伙人Amy Schulman和Darren Carroll加入了Tessa的董事会。
获得大型医疗保健投资者的亿元融资,是Tessa近期发展的一个重要里程碑,基于其CAR-T疗法2期临床试验结果数据的积极表现。在此之前,Tessa还于2018年完成由Temasek领投,EDBI、Karst Peak Capital、Heliconia和Heritas等投资者跟投的1.3亿美元融资,这笔资金主要用于建设该公司的病毒特异性T细胞(VST)平台和推进其临床试验。
在技术壁垒高且竞争加速的细胞治疗市场,Tessa能够在几年内连续获得两家大型投资机构的亿元级投资,这家公司有什么核心的竞争力?
Tessa正在开发的是一系列针对癌症的下一代细胞疗法。
免疫细胞治疗技术是通过采集人体自身免疫细胞,经过体外培养,使其数量扩增,增强靶向性杀伤功能,然后再回输到患者体内,从而杀灭血液及组织中的病原体、肿瘤细胞和突变细胞。嵌合抗原受体T细胞(Chimeric Antigen Receptor T cell, CAR-T)治疗方法最近引起科学界与临床应用的广泛关注。
CAR-T被认为是近年来癌症免疫治疗领域的重大突破之一,在血液系统恶性肿瘤的治疗中体现了巨大优势。但目前的技术也存在一定的局限性:自体CAR-T疗法面临时间成本、制造成功率、细胞效力和生产成本等问题;同种异体CAR-T疗法面临移植物抗宿主疾病(GvHD)和患者体内T细胞持久性问题。
CD30是一种跨膜蛋白,在健康组织中基本不存在。它是经过充分验证的淋巴瘤靶标,在经典霍奇金淋巴瘤和非霍奇金淋巴瘤的多个亚群中表达稳定且一致,即使在CD30靶向治疗和再治疗后出现耐药或复发时也有效。并且,CD30仅在活化的T细胞和B细胞上表达,使得靶向这种抗原不太可能发生重大的脱靶相关不良反应。更重要的是,临床前数据显示,CD30靶向有助于转到活性T细胞,进而改善细胞的扩增和持久性。
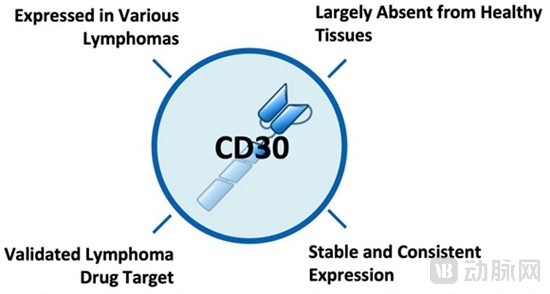
Tessa通过自建的CD30-CAR- T平台正在进行TT11 CD30-CAR-T疗法的临床试验,主要针对的是经典霍奇金淋巴瘤(cHL)和非霍奇金淋巴瘤。该疗法采用自体细胞疗法,通过设计针对CD30的CAR-T细胞定向杀死CD30阳性的HL细胞1-2系。贝勒医学院(试验编号:NCT02917083)和北卡罗来纳大学(试验编号:NCT02690545)对复发或难治性CD30阳性霍奇金淋巴瘤患者进行的两项独立的CD30-CAR细胞I/II期研究显示,TT11 CD30-CAR T细胞在高度预治疗的霍奇金淋巴瘤患者中具有良好的疗效和较低毒性特征。
病毒特异性T细胞(VSTs)是在病毒感染期间产生的高度特化T细胞。这些细胞有能力识别并杀死被感染的细胞,同时激活免疫系统的其他部分以作出协调反应。早期实验证明,未经基因改造的异体VSTs具有良好的安全性和疗效,并且表现出很低的GvHD等严重排斥反应。
利用CD30对淋巴瘤的精准靶向性、对细胞扩增和持久性的改善,以及VSTs对GvHD的风险性,经过科学联合创始人Malcolm Brenner 博士及其贝勒医学院团队对病毒特异性T细胞(VSTs)性质长达数十年的研究和开发,Tessa打造了CD30-CAR-VSTs治疗平台。该平台能够实现精准靶向,迄今为止,Tessa已经在第三阶段的临床试验中成功制造交付了150多种VST疗法。

科学联合创始人兼科学顾问Malcolm Brenner 博士
目前,Tessa通过CD30-CAR技术将爱泼斯坦巴尔病毒特异性T细胞(EBVSTs)进行增强,提高了VST细胞的持久性和扩增性。目前Tessa正在与贝勒医学院合作,在美国对这项技术进行I期临床试验评估。
目前的CAR-T细胞疗法在实体瘤患者身上取得的临床成功有限。CAR-T细胞治疗实体瘤的一些障碍包括:实体瘤中癌症抗原表达的异质性导致逃逸变体的生长;器官中肿瘤抗原的低水平表达导致目标外肿瘤活性;限制免疫细胞进入的物理障碍;免疫抑制微环境的发展等。Tessa认为,准对实体瘤的CAR-T细胞治疗迫切需要变革创新。
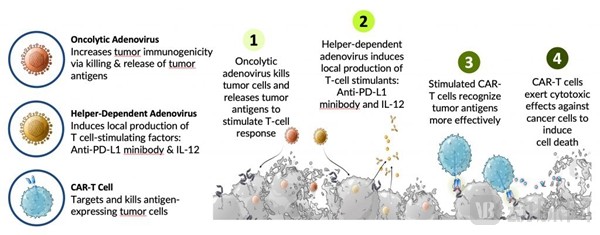
Tessa的实体肿瘤靶向疗法
Tessa克服在实体瘤中应用CAR-T细胞的挑战的方法是将CAR-T细胞和二元溶瘤病毒疗法相结合。这种疗法的施用分为两步,首先将由溶瘤病毒和辅助性腺病毒组成的腺病毒局部施用到肿瘤中,然后全身输注肿瘤抗原靶向的CAR-T细胞。瘤病毒直接杀死肿瘤细胞,同时产生一个炎症性的肿瘤微环境,让CAR-T细胞更易“浸润”。CAR-T细胞进入后开始进行第二次的肿瘤杀伤。
Tessa与贝勒医学院合作,将HER2-CAR-T细胞和二元溶瘤病毒治疗相结合,靶向ER2阳性实体瘤,其临床I期试验在美国进行。
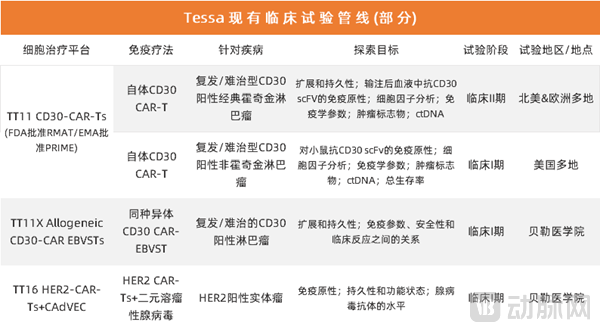
Tessa三个细胞治疗平台涉及的临床管线
Tessa总部位于新加坡,拥有占地13.4万平方英尺的亚洲顶尖细胞疗法生产设施。其拥有全面的细胞治疗处理技术、分析测试能力、工艺/分析开发、培训设施和IT GxP平台,能够支持Tessa自体和异体细胞及基因治疗产品的临床试验和商业生产。鉴于优秀的技术研究能力和生产制造水平,Tesssa收获了贝勒医学院、北卡罗莱纳大学、圣裘德儿童研究医院、新加坡国家癌症中心、新加披科学技术研究机构(IMCB)等一系列战略合作伙伴。
接下来,Tessa将利用本次融资的资金继续推进TT11 自体CD30-CAR-T疗法和异体TT11X-CD30-CAR-EBVST疗法的临床开发,相关临床耗材将在刚刚完成商业获批的cGMP设施中制造。
CAR-T作为细胞疗法的热门赛道,国内外已有不少企业加入。据动脉橙数据库统计,目前全球共有五款靶向CD19的CAR-T细胞产品获批上市,分别是诺华的Kymriah、Juno Therapeutics的Breyanzi、吉利德科学的Tecartus和Yescarta,以及药明巨诺的瑞基奥伦塞注射液,皆用于治疗淋巴瘤。目前CAR-T领域的研发管线几乎占据了全部免疫细胞治疗管线的一半,其中以CD19靶点最为热门,适应症分布较为集中,已出现赛道拥挤趋势。
Tessa目前的临床开发多针对淋巴瘤,下阶段将开发异体CD30-CAR-VSTs平台针对多个癌种的治疗,以应对赛道的激烈竞争。





























