编者按:数字生物标记物(Digital Biomarkers)作为当今医疗领域的前沿,所面临的最大挑战是如何建立可量化、具有临床可解释性的客观标准,并将其用于发现、解释或预测疾病走向。而我们欣喜地发现,上海织生科技有限公司(织生科技)作为国内「数字生物标记物」方向的新创医疗科技企业,我们有幸对他们的创新技术解决方案做一个分享。
阿尔茨海默病(Alzheimer’s Disease,AD)归属于中枢神经退行性疾病。截止目前,我国已确诊的患者有着将近1000万,而如果将AD的前驱期——轻度认知障碍(Mild Cognitive Impairment, MCI)也囊括在内,认知障碍高风险及患病人群的数量在我国就已经接近5000万大关[1]。并且伴随着人口结构老龄化和平均寿命的提升,相关风险人群的数量还在不断快速攀升。
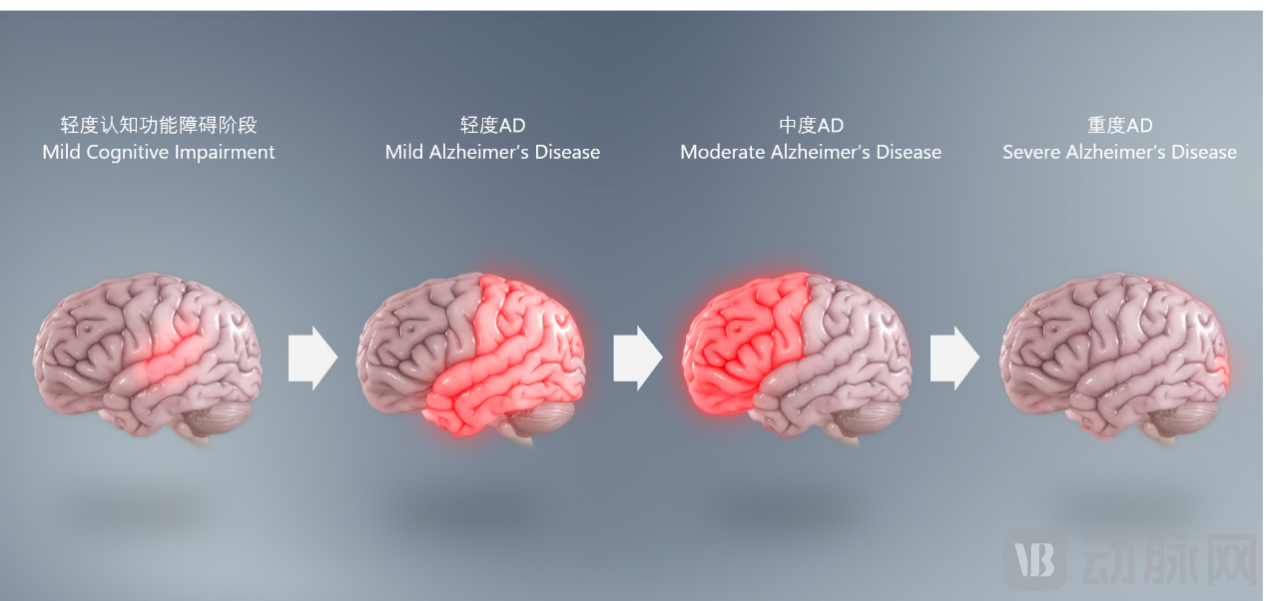 AD不同阶段最主要受损脑区示意图[2]
AD不同阶段最主要受损脑区示意图[2]
作为现有国人致死病因排名第五的[2]阿尔兹海默病,其发病是渐进式的,从部分脑区发展到全脑区,症状从轻度发展到重度,病程相对较长,一般确诊后的预后约为5-10年。
● 轻度认知功能障碍阶段(Mild Cognitive Impairment, MCI)
核心症状是情境性的记忆能力下降和执行功能下降,比如忘记谈话和最近发生的事情,无法完成过去熟练的事情或做出决定。
● 轻度AD阶段(Mild Alzheimer’s Disease)
在这个阶段,患者很可能反复问同样的问题,把他们的物品放错地方,在计划和决策方面出现困难,要么性格变得冷淡,要么表现出异常的暴躁。
● 中度AD阶段(Moderate Alzheimer’s Disease)
记忆或思维出现严重问题,工作或社会生活收到显著影响,像处理金钱、言语表达和组织思想等变得困难。病症开始扩散到言语理解区域和视空间处理区域,这导致言语表达困难和时间空间感知混乱。
● 重度AD阶段(Severe Alzheimer’s Disease)
大部分的大脑皮层被严重损坏,除了全局性认知功能障碍,个人的精神状态出现异常,身体机能和运动能力的影响也越来越大。病人在吃饭、穿衣、上厕所和所有其他日常自理工作方面需要全面的帮助。最终,甚至失去吞咽和控制膀胱和肠道功能的能力。
关于阿尔茨海默病的病因,目前相对主流的看法认为β-淀粉样蛋白(Amyloid-β,Aβ)和过度磷酸化的Tau蛋白(p-Tau)是致病元凶[3]。现有处于研发阶段的新药也大多针对上述靶点。但是这些异常变性蛋白的聚集并不一定会导致认知功能异常。而发生认知功能障碍后,再清除这些变性蛋白对症状改善也非常有限。例如2021年推出的针对Aβ的单抗药物aducanumab,后期因为效果不佳,并且伴有脑水肿等副作用,最终被限制了使用范围,甚至在有些地区未被批准其上市。
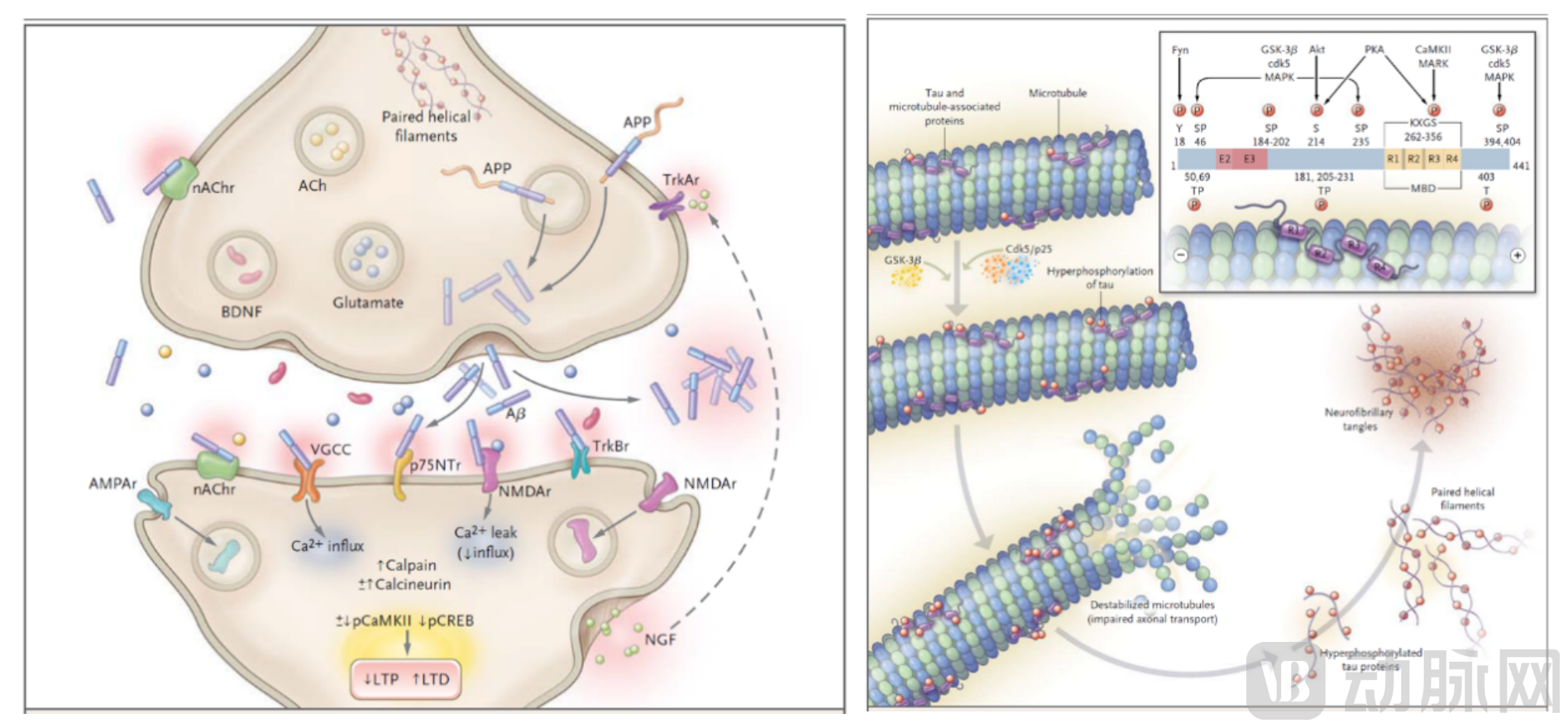 β-淀粉样蛋白(左图)和过度磷酸化的Tau蛋白(右图)的致病机理[4]
β-淀粉样蛋白(左图)和过度磷酸化的Tau蛋白(右图)的致病机理[4]
看来,Aβ和tau蛋白假说并非是最终的答案。而各种其他致病假说也层出不穷,如神经炎症假说和肠脑假说等。时至今日,阿尔茨海默病的致病机理尚未得到最终的证实,从而导致该疾病从诊断阶段就面临着巨大的挑战。
因为AD的致病原因尚不清楚,因此在临床上做AD诊断都要结合生化影像检测和行为学量表评估来综合判定[5]。现有的AD生化影像检测(生物标记物检测)抑或是侵入性的,例如腰椎穿刺脑脊液样本,患者本身的痛苦以及患者家属的诸多顾虑对诊断构成了重重阻碍;抑或是代价极为高昂,例如fMRI影像和PET-CT影像,动辄成千上万的检测费用也无形中成为了制约患者检测意愿的巨大门槛。基于血液的生物标记物检测也在研究中,相比脑脊液侵入性更小,相比脑影像成本更低,然而现在对血液中的生物标记物作用机制尚不明确,上千元的检测费用也限制了其成为通用普筛的工具。而门槛更低的行为学量表又存在着主观的(被试者对于问题理解差异)和客观的(教育水平,年龄,疾病史等)因素的影响,致使评估的准确率和客观性都值得怀疑,特别是在未受过专业培训的基层服务机构。
在一系列因素的综合影响下,我国高达93.98%的病人尚未得到临床诊断,剩下约6%的患者中,仅36.79%在一次就医后被成功确诊。[6]
因为现有评估诊断技术的种种局限,AD早筛早诊的理念与应用落地上,存在着巨大的落差,一个兼具客观性和便捷化的诊断评估工具是当务之急。经过大量与长期的研究,织生科技将注意力集中到「眼-脑」模型。
眼睛,是人体最重要的感受器官,大脑接收的外部信息90%来自于眼睛。眼睛获取的信息传递给大脑,从而支配着人体的外部行为;同样,大脑处理完的信息,也会影响眼球的运动和状态。眼脑之间的这种相互的联系,为我们通过眼睛探究大脑的提供了一条路径。在先前的研究中已经发现,通过眼睛运动和瞳孔状态,我们能够评估情绪状态和大脑的疾病状态。
在眼脑的生理学关系上,研究发现脑区的病变和脑内的神经递质水平和眼部的运动和状态有着高度关联。眼球运动的主要方式包括凝视、扫视、视动性眼震、前庭眼动等,主要由大脑皮层、上丘、基底节区参与眼动的控制,脑干核团参与眼动生成,小脑参与眼动调节。
在眼脑的行为学关系上,研究发现人类的注意力位点变化与眼动变化是高度一致的。人类视网膜结构中,中央凹(foveal),是视网膜中视觉最敏锐的区域。大脑通过调整眼睛的角度来将视觉信号投射到中央凹以获得视觉信号的精确化加工。因此,当大脑需要注意到某个物体时,便通过调整眼睛的角度(瞳孔或头部的角度)来将目标区域的画面映射到视网膜中央凹。而其中,眼跳(saccade)是眼动最重要的行为参数之一。研究表明,眼跳和注意发生时,被激活的脑部区域高度重叠。这说明注意和眼动过程不仅在外在行为上,而且在神经生理机制上有着高度的相关。简而言之,我们可以通过眼动的运动来追踪注意力位点的变化。
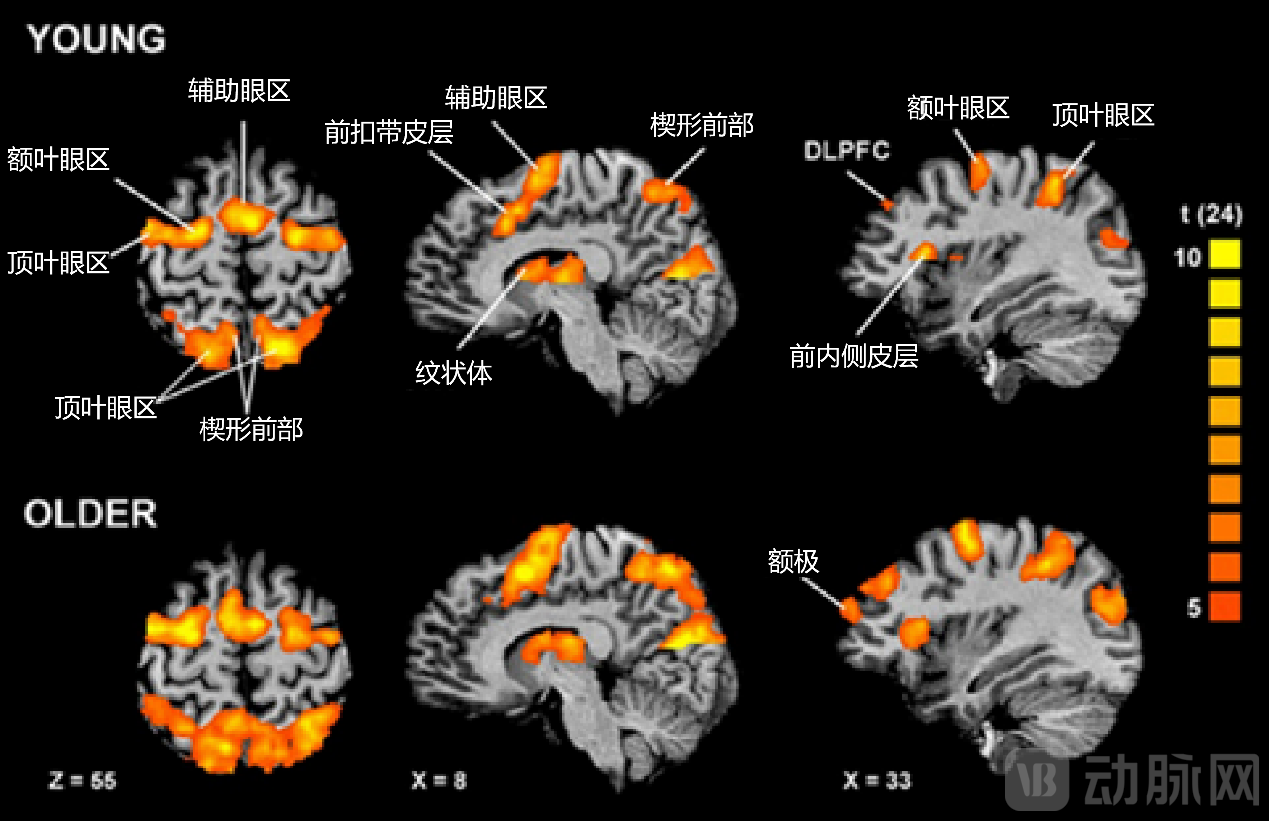 眼跳与反向眼跳任务下激活的脑区[7]
眼跳与反向眼跳任务下激活的脑区[7]
脑功能成像研究表明,眼跳的产生需要多个大脑区域的参与,上丘被认为是眼跳的指令发出者,眼跳同时会激活多个大脑皮层,包括扣带回(cingulate gyrus)和脑岛(insula)以及皮层下的苍白球(globus pallidus)、纹状体(striatum)和丘脑(thalamus)。研究发现,在执行反向眼跳过程中,额叶-纹状体-视丘-皮层回路(fronto-striatothalamo-cortical circuits)这两个重要的区域参与其中。[8]
有研究表明,执行特定眼跳任务的脑区回路与阿尔茨海默病早期受损的脑区重叠。因此,它可以作为鉴别早期阿尔茨海默病类型和评估严重程度的一个指标。例如,2019年一篇发表在《Aging》杂志上的研究中,作者研究了反向眼跳任务鉴别遗忘型(aMCI)和非遗忘型(naMCI)轻度认知功能障碍患者的能力。结果发现,反向眼跳任务的结果可以显著区分两种类型的MCI。这项工作为眼动追踪作为一种有用的诊断性生物标志物在痴呆评估中提供了进一步的支持。[9]只通过眼动的反应,而不再需要复杂的题目理解和操作,这一切为更加客观准确地诊断阿尔茨海默病乃至轻度认知障碍打开了一扇全新的窗户。
织生科技是全国首家以AI视线追踪技术驱动的神经系统疾病数字生物标记物的研发创新型公司,形成了以阿尔茨海默病为切入点的,认知功能障碍领域全新诊断方法和技术解决方案。公司团队来自欧洲顶尖神经研究所、MIT、剑桥、上海交大等顶尖机构,依托多年脑科学和人工智能技术储备与跨学科背景推出的「视线追踪算法模型」,使得任何一部具有摄录功能的智能设备都能具备过往专业仪器才能达到的眼动追踪功能,而且已达到临床级应用级别的精度。与现有心理学和神经生理学研究中领域内使用的动辄十几万的传统近红外线眼动仪方案相比,织生科技的方案首先不再需要专业的外接硬件和配套的专业分析软件,这将大大降低了操作和应用的门槛。其次,在测试的过程中,也不再需要固定被试者的头部,即使被试者佩戴眼镜,也不会影响识别的准确性。而最为重要的一个细节是,任务的过程不需要一系列前期复杂的矫正流程。


传统眼动仪(上图)VS 基于AI摄像头眼动追踪技术演示(下图)
通过观测和分析受试者在完成任务时的眼动参数,织生科技开始触碰到阿尔茨海默病的「数字生物标记物」。想象一下,在观看一段视频的几分钟里,通过我们的「视线追踪算法模型」,结合相关的「数字生物标记物」参数,我们就能评估出受试者的认知功能,并对其罹患认知障碍的风险做出判断。
这一方式的先进性在于,织生科技不仅能运用于阿尔茨海默病(AD)的前期诊断,并且能涵盖包括主观认知下降(Subjective Cognitive Decline, SCD)、轻度认知障碍(Mild Cognitive Impairment, MCI)在内的阿尔茨海默病(AD)前驱症状的诊断。而通过后续的一系列临床试验,我们希望推动眼动「数字生物标记物」作为认知功能障碍检测的专家共识,未来纳入临床诊断标准,从而使得这一兼具客观性、准确性和便捷性的解决方案最终像血压检测一样“飞入寻常百姓家”。
得益于「视线追踪算法模型」这一创新性的技术,兼具准确性和便捷性的AD早期评估和诊断将得以实现。在织生科技的后续规划中,既有提供给专业医疗机构使用的专业医疗器械级产品,也有面向个人用户的辅助评估产品。建立AD的「数字生物标记物」,只是我们征程中的第一步,而通过「视线追踪算法模型」研究的进一步深入,诸如帕金森病(Parkinson’s Disease, PD)、注意缺陷与多动障碍(Attention Deficit and Hyperactivity Disorder, ADHD)、自闭症(Autistic Spectrum Disorder, ASD)的「数字生物标记物」序列也将最终被确立。
目前织生科技针对阿尔茨海默病(AD)前驱症状的诊断产品已完成前期研发,已具备大规模收集临床数据的能力。推动中枢神经系统疾病以及神经发育障碍领域「数字生物标记物」序列的建立,将是织生科技在接下来相当长一段时间内的主要工作。面向神经系统疾病的技术研发和应用,是「织生科技」探索大脑这片星辰大海的第一步。
参考文献
[1] Jia, L, et al., (2020). Prevalence, risk factors, and management of dementia and mild cognitive impairment in adults aged 60 years or older in China: a cross-sectional study. The Lancet. Public health, 5(12), e661–e671.
[2] Dan, Siddhartha & Sharma, Deeksha & Rastogi, Kartikey & Ojha, Himanshu & Pathak, Mallika & Singhal, Rahul & shaloo,. (2021). Therapeutic and Diagnostic Applications of Nanocomposites in the Treatment Alzheimer's Disease Studies. Biointerface Research in Applied Chemistry. 12. 940-960. 10.33263/BRIAC121.940960.
[3] Zhou, M., Wang, H., Zeng, X., Yin, P., Zhu, J., Chen, W., ... & Liang, X. (2019). Mortality, morbidity, and risk factors in China and its provinces, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. The Lancet, 394(10204), 1145-1158.
[4] Masters, C., Bateman, R., Blennow, K. et al. Alzheimer's disease. Nat Rev Dis Primers 1, 15056 (2015).
[45] Dubois, B., Villain, N., Frisoni, G. B., Rabinovici, G. D., Sabbagh, M., Cappa, S., ... & Feldman, H. H. (2021). Clinical diagnosis of Alzheimer's disease: recommendations of the International Working Group. The Lancet Neurology, 20(6), 484-496.
[6] 中国老年保健协会阿尔茨海默病分会,中国阿尔茨海默病患者诊疗现状调研报告2020
[7] Fernandez-Ruiz, J., Peltsch, A., Alahyane, N., Brien, D. C., Coe, B. C., Garcia, A., & Munoz, D. P. (2018). Age related prefrontal compensatory mechanisms for inhibitory control in the antisaccade task. Neuroimage, 165, 92-101.
[8] Zhu DANG. Antisaccades and Its Experimental Paradigm, Mechanisms and Influence Factors[J]. Psychological Science, 2012, 35(1): 16-23.
[9] Wilcockson, T., Mardanbegi, D., Xia, B., Taylor, S., Sawyer, P., Gellersen, H. W., Leroi, I., Killick, R., & Crawford, T. J. (2019). Abnormalities of saccadic eye movements in dementia due to Alzheimer's disease and mild cognitive impairment. Aging, 11(15), 5389–5398.





























