Informa统计数据显示,2021年全球医药研发投入2001亿美元,相比2016年增长27.7%。医药研发投入并未受到疫情影响,尤其国内新药研发投入上涨明显。
2020年,国内新药研发投入相较2019年增加54亿美元,占全球增加总额的61.4%。2021年,国内新药研发投入相较2020年增加65亿美元,占全球增加总额的75.6%。
新药研发热度持续增长,中国新药研发市场更是在加速成长。临床试验作为新药研发的重要环节,占据总研发时长约60%的时间。近年来AI技术在药物发现阶段的应用发展迅速,有效压缩了临床前的研发时间,使临床试验阶段的时长占比进一步扩大。
追求整体新药研发提速,提升临床试验效率已成为必然趋势。
疫情的突然来袭,使得国内数字化程度还相对较低的临床试验行业一时不能做出快速应对。
“我们一开始想要做的是帮助临床试验能够在疫情下快速恢复运作,随着工作的不断推进,我们发现其实疫情并不是唯一的影响因素,在这个协同方丰富、信息交互需求巨大、纸质化办公原始的行业,如果能真正实现数字化,那对整个行业都是一次很大的提效。”新视焰创始人兼CEO金杰飞先生在采访中讲到。
新视焰成立于2020年7月,是目前国内领先的临床研究数智化基础设施提供商。截至目前,与新视焰建立合作的大型医院超过50家,申办方/CRO企业超30家,并已完成两轮融资。Pre-A轮融资由泰格医药投资;Pre-A+轮由红杉中国种子基金领投,杭州和达生物医药产业基金跟投。
新视焰以远程监查为入口进入数字化临床试验赛道,通过沟通客户体验不断打磨产品,现已切实的完成了超2000项来自合作方的产品需求。
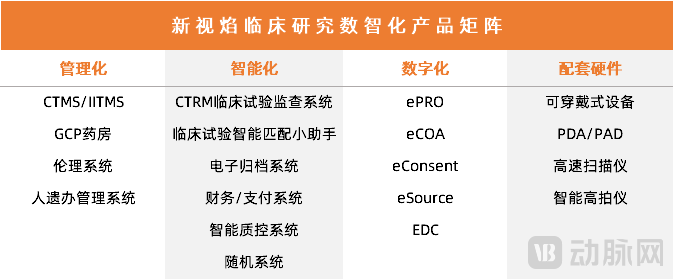
新视焰临床研究数智化产品矩阵
新视焰产品矩阵覆盖医院、CRO、SMO、监管部门、受试者、物流公司等等角色,以临床监查为提升行业数字化程度的基础,联通各协作方。
以临床监查员(CRA)为例,由于临床病历不能随意调离医院,CRA需要去到各医院实地查看病历内容,路途奔波且差旅费用成本高是每个CRA的痛点,加之疫情的影响,均严重阻碍CRA的工作进度。
新视焰通过将受试者管理权限进行线上管理,让项目CRA在远程进行受试者医疗病历的查看,免去路途成本,提高CRA管理临床试验项目数量的可能性,从速度与体量等方面提高CRA工作效率。
新视焰以其“保守”的技术方案深受合作医院欢迎。以“数据不出院”为宗旨布局其数据管理权限功能,在提供系统维运等售后服务中,新视焰相关工作人员也需遵守规定开启无间断全过程录屏。
这样的设计,不仅确保产品及服务的专业性,更是提高了合作医院户对产品、对新视焰的信任,提高客户留存率。
稳固好医院与自身的合作连接,也是提升该医院临床试验的抗风险能力,进而获得药企对该医院临床试验水平的亲赖,从而增加更多新的合作。
在创立新视焰前的近20年,金杰飞先生曾在辉瑞有过11年的工作经验,期间担任辉瑞中国创新药事业部数字营销负责人,同时也曾参与创新医疗企业的创业。
结合头部药企与创业公司的丰富经验,金杰飞带领在GSK、诺华、太美医疗等企业拥有丰富工作经验的创始团队,在成立第二个月便拿下与浙医二院的合作,同年完成远程监查产品落地,次年达成与恒瑞医药的合作。
新视焰目前已成为远程监查领域的领导者。
目前,与新视焰开展合作的医院共计超过50家,遍及全国近30个城市,三甲医院占比90%,包括北京朝阳医院、中南大学湘雅医院、华中科技大学附属同济医院等。签约医院对应I-IV期项目数近6000项,占到中国临床试验份额约10%。
“我们公司的文化里很坚持的一个事情,是:承诺兑现。”金杰飞表示,之所以在新视焰成立之初就有合作医院愿意提供宝贵意见,并且在发展中也源源不断地获得合作方的信任与认可,是因为他们切实做到了对用户真实需求的响应。
对客户承诺的兑现,既是赢得客户信任的关键,亦是打磨产品、历练技术的精准途径。通过这种双赢的模式,新视焰为打造一个使用方便、标准合规的远程监查产品创造了机会。
“去中心化临床试验(DCT)”与“真实世界临床研究(RWS)”,已是国际公认的临床研究未来发展方向。
新视焰的产品发展方向也将以现有远程监查为基础,继续扩大合作,倾听客户反馈、完善现有功能。在合作方逐渐丰富后,新视焰也将打造全新的产品,为临床试验的数据互联互通打下基础,通过合规应用为临床试验的效率提速创造条件。
单点打透,由点及面,“匠心精神”在一个行业的任何发展阶段都值得肯定。
期待新视焰能够坚持“助力中国临床试验的效率和质量领先全球”的使命与初衷,打造领先的临床研究数智化基础设施,帮助中国早日实现临床试验全面数智化!





























