让打针治疗糖尿病成为历史。
这正是电子科技大学医学院王轶教授所希冀的。在生活中,人们之于糖尿病并不陌生,根据国际糖尿病联盟数据,截止到2021年,在20-79岁的人群中,共有5.37亿糖尿病患者,而中国糖尿病患者数排名第一,总人数超过1.4亿人,市场规模达到746亿元。
作为一种尚无完全根治方法的疾病,目前大多数1型糖尿病患者都必须终身注射胰岛素,这非但不足以控制血糖,还会导致副作用和进展性并发症,如肾脏损伤、神经病变等疾病。
打破科研桎梏,王轶教授专注于微囊化异种胰岛移植研究,并提出一种全新的胰岛微囊化技术,避免了免疫排斥反应。近日,受“科创中国”第二届生物医学高价值专利项目评选活动的邀请,动脉橙果局与王轶教授团队聊了聊胰岛微囊化技术的一二事。
胰岛移植疗效很“美”,但迈向临床很难
所谓胰岛移植,就是指将供体捐献的胰腺,在符合产品生产质量管理规范(GMP)的实验室中通过消化、分离、纯化等步骤,获得高纯度的胰岛细胞团,并移植给患者的手术。
完全不同于创伤较大的实体器官移植(胰腺移植),胰岛移植仅需在局部麻醉下,借助超声及数字化处理血管造影(DSA)的影像引导,穿刺注射到患者体内,术后,患者借助新的胰岛细胞,能够在体内重新分泌胰岛素和胰高血糖素,进而达到长期脱离胰岛素和稳定血糖的效果。
不仅做到微创,胰岛移植治疗晚期糖尿病的疗效还很“美”,整体效果接近胰腺移植。
据2014年世界移植大会资料显示,胰岛移植后5年无需使用外源性胰岛素的患者比例已经达到60%左右,一次注射脱离胰岛素的患者,最长时间可以达到16年。
可以说,胰岛移植是目前唯一通过微创治疗即可实现晚期糖尿病根治的临床治疗手段。
但挡在“拳头”技术进入临床的前面有两座大山:
一是可用供体器官严重短缺,胰岛供给链随之断裂。据悉,2021年中国糖尿病相关死亡人数接近140万人,而接受胰岛移植的患者不到50人,这意味着全国胰岛供给不足0.003%;
二是胰岛细胞早期排异丢失及药物不良反应。一方面,胰岛细胞的缺氧和炎症反应可能导致高达60%的胰岛细胞坏死和凋亡;另一方面,针对胰岛移植后的免疫排异反应,虽然口服免疫抑制药物能在局部发挥抑制作用,但免疫制剂本身也会引起许多不良反应,同样可能导致胰岛细胞凋亡。
目前来看,国际上虽然有公司已经进行了1/2期临床试验,术后6名糖尿病患者不需要接受糖尿病治疗,但是患者未能做到免疫隔离,还需要长期服用免疫抑制剂。
“理想与现实还隔着一道鸿沟。”王轶这样感叹道。
尽管胰岛移植对于糖尿病具有很好的疗效,但它并没有想象中那样普及。在无药可医的现状下,王轶看准了胰岛微囊化技术,通过降低包囊材料以及包囊内容物的免疫原性,改善移植胰岛生存环境。
全新的胰岛微囊化技术打出“免疫隔离”
用类似于药物胶囊制剂的外壳材料将胰岛包裹起来,做成一个“胰岛胶囊”,来模拟天然胰岛的微观和宏观环境,这就是胰岛微囊化技术,也称为胰岛封装技术。实际上,这是一种免疫隔离的策略,即保护移植的胰岛细胞。
具体来说,将移植胰岛细胞包封在半透性的微囊中作为机械屏障,实现移植胰岛与宿主分离,保护移植胰岛免受免疫细胞以及抗体介导的排斥反应,这样一来,就能达到两个效果:
一是可以使用动物胰岛(猪胰岛)作为供体来源,进行异种胰岛移植;二是移植后,患者无需长期使用免疫抑制剂,无相关不良反应,生活质量更高。
“这项技术在临床应用方面有许多优势,除了能解决供体短缺的问题,还能通过减少或消除排斥反应,避免移植的胰岛减少。”王轶表示。
相比未封装的胰岛,微囊封装的胰岛具有良好的机械性能、生物相容性和半透膜性。先说机械性能,即胰岛细胞运输到体内后,受压迫不会变形;再来说生物相容性,能规避免系统的识别攻击;最后说可控的半透膜性,微囊孔径允许葡萄糖、氧气、营养物质、代谢废物和信号分子通过微囊双向扩散,同时阻止免疫细胞、免疫活性物质等对移植胰岛细胞的攻击。
值得注意的是,以上三大优点背后是构成微囊的材料在支撑。
目前,制造微囊的水凝胶材料分为天然水凝胶与合成水凝胶。“天然水凝胶(海藻酸盐、琼脂糖、壳聚糖、胶原蛋白、聚L-赖氨酸)具有良好的生物相容性和较低的生产成本,但在生理条件下,其稳定性较弱。”王轶认为。
而合成水凝胶(如聚乙二醇、聚甲基丙烯酸甲酯)则在孔径大小、机械强度和弹性等方面更胜一筹,能实现对材料性能的控制,使得其具有更适宜的孔隙、更高的机械阻力和弹性。
1+1>2,目前王轶团队通过将天然水凝胶和合成水凝胶进行结合,以彼之长,补己之短,中和两者优劣势,最终研发出完美的YCQ-01微囊,其完美性表现在两方面:
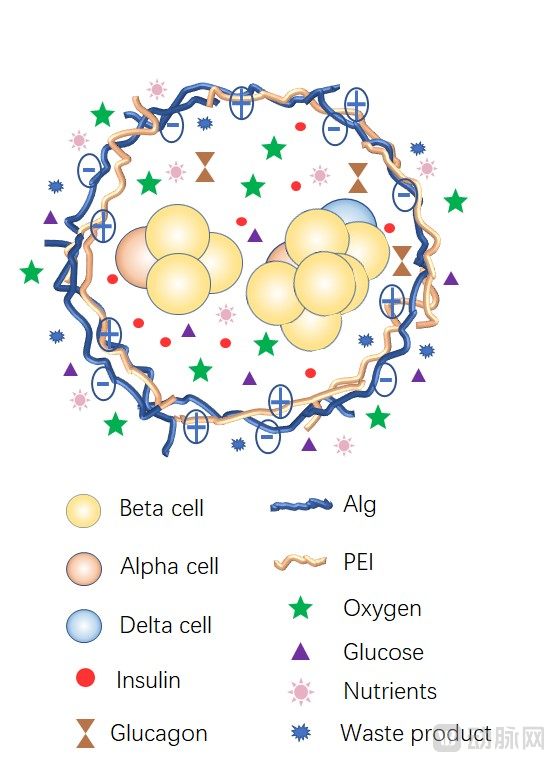
图为YCQ-01微囊模型
首先是国内唯一一家实打实的动物试验数据,在无免疫抑制药物条件下,移植胰岛细胞存活及发挥功效时间均居全球第一梯队。测试结果表明,在140天(半年)的观察期内,糖尿病动物术后不需要使用胰岛素,也不需要采用免疫抑制剂。
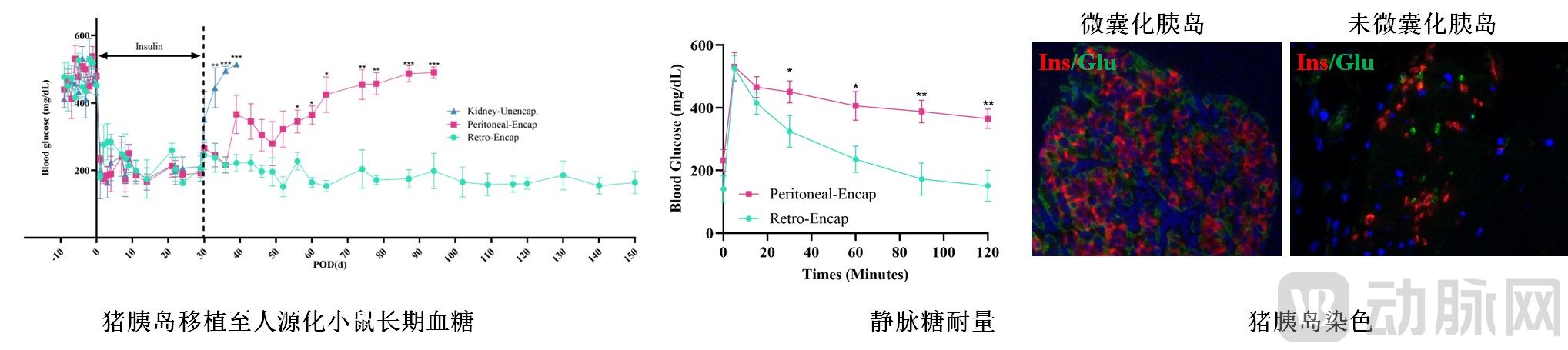 注:有效存活的胰岛细胞可被染色(红、绿等颜色)
注:有效存活的胰岛细胞可被染色(红、绿等颜色)
其次是微囊均一的纳米级孔径,可以说是细胞移植微囊的最佳尺寸,据悉,机代谢物的直径在0.05—1纳米,而球状蛋白质的直径在2—10纳米,这意味着孔径在保证功效物质排出、营养互换的同时,有效避免移植细胞免疫损伤。
“材料的孔隙必须是最佳尺寸,以便允许营养交换但防止免疫反应的发生。”王轶表示。
除了专注胰岛微囊化技术的研发外,王轶还在积极寻找新的移植部位。
团队成员透露,目前已知的肝门静脉和腹腔内并不是微囊化胰岛移植的理想部位,而寻找免疫豁免区域作为微囊化胰岛移植部位,可以有效解决免疫排异所致的胰岛功能丧失和纤维化的形成。
教授掌舵公司,已申请多项专利
2022年1月21日,成都易查擎生物科技有限公司(以下简称为易查擎生物)正式成立,这家未满周岁的初创企业,却在多方面做了周密布局。
首先是以教授带头的全球顶级技术积淀,联合王轶教授、Leo Buhler教授突破前沿技术,申请了多项发明专利。其中Leo Buhler教授专注于异种移植超过30年,是全球第一个包裹式猪肝细胞的异种移植专家,发明了将肝细胞异种移植到人体的临床研究,被认为是医学史上的一个里程碑。
其次是团队组建,成员行业经验丰富,配置完善。在整体战略规划、公司日常运营、外联、销售布局和运营等多方面上,都由专业人才把控。
最后是产品管线,长短期收益相结合。以微囊化胰岛细胞手术为优先发展产品管线,并同步推进“微囊化肝细胞移植”管线,据悉,我国患者人数高达2亿,终末期肝病患者的有效治疗率不足5%,又由于器官移植供体肝脏资源紧缺,无法满足临床需求,肝细胞移植成为患者的救命稻草。
目前,易查擎生物正处于融资阶段,下一步计划完成标准实验室的建立和运营、推动微囊化胰岛移植的灵长类动物及人体临床试验,并以YCQ-01微囊为企业发展基础,努力让打针治疗糖尿病成为历史。