CXO行业的增长态势往往依托于其所服务的新药研发行业。
NewBiologix就是在基因与细胞治疗(CGT)这一前沿浪潮下诞生的一家瑞士生物技术服务公司。今年5月,NewBiologix公布完成5000万美元A轮融资,投资方为Recipharm。这笔资金将用于其细胞系原型的Beta测试。预计到2026年,NewBiologix可将其病毒生产细胞系商业化。
关于本轮融资,NewBiologix联合创始人兼首席执行官Igor Fisch博士表示:“随着临床和市场中基因和细胞疗法的数量持续增长,生物制药公司需要改进病毒载体的制造。而我们的使命是为这些公司提供创新技术和解决方案,帮助他们快速且更具成本效益地提高病毒载体的产量和功效。”
一家名不见经传的瑞士公司凭什么获得资本青睐?我们要从CXO背后的CGT赛道看起。
早在20世纪70年代,基因治疗的概念就被提出。到2012年,欧洲批准首个基因治疗药物Glybera上市。2015年,美国第一款基因治疗产品IMLYGIC上市。Kymriah、Luxturna、Zolgensma等里程碑药物陆续上市。经过近半个世纪,基因疗法已从概念变为现实。如今全球已有超过40款基因治疗药物上市,用于治疗癌症、遗传性疾病等。
根据弗若斯特沙利文数据,2016年至2020年,基因治疗市场从约5040万美元增长到20.8亿美元,预计到2025年,全球基因治疗市场规模将达到近305.4亿美元。
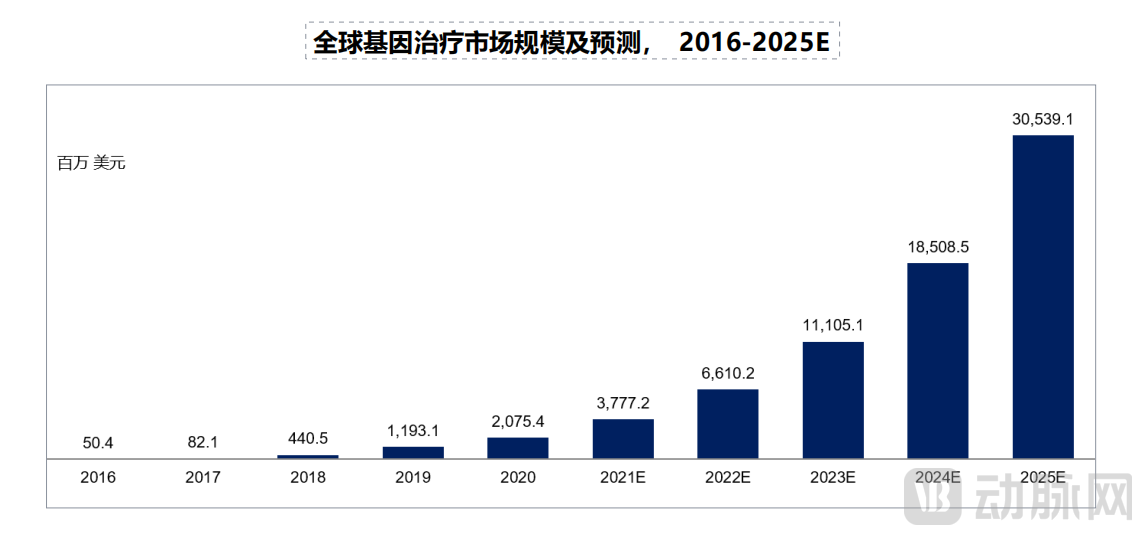 图源:弗若斯特沙利文
图源:弗若斯特沙利文
随着CGT成为全球最具潜力的前沿医药领域之一,CGT CXO市场的春天同步到来,尤其是CGT CMO和CGT CDMO。根据弗若斯特沙利文分析,随着细胞治疗相关研究和临床试验的扩大,到2025年,全球细胞和基因治疗CMO/CDMO市场将达到101亿美元,2020年至2025年的复合年增长率为34.9%。
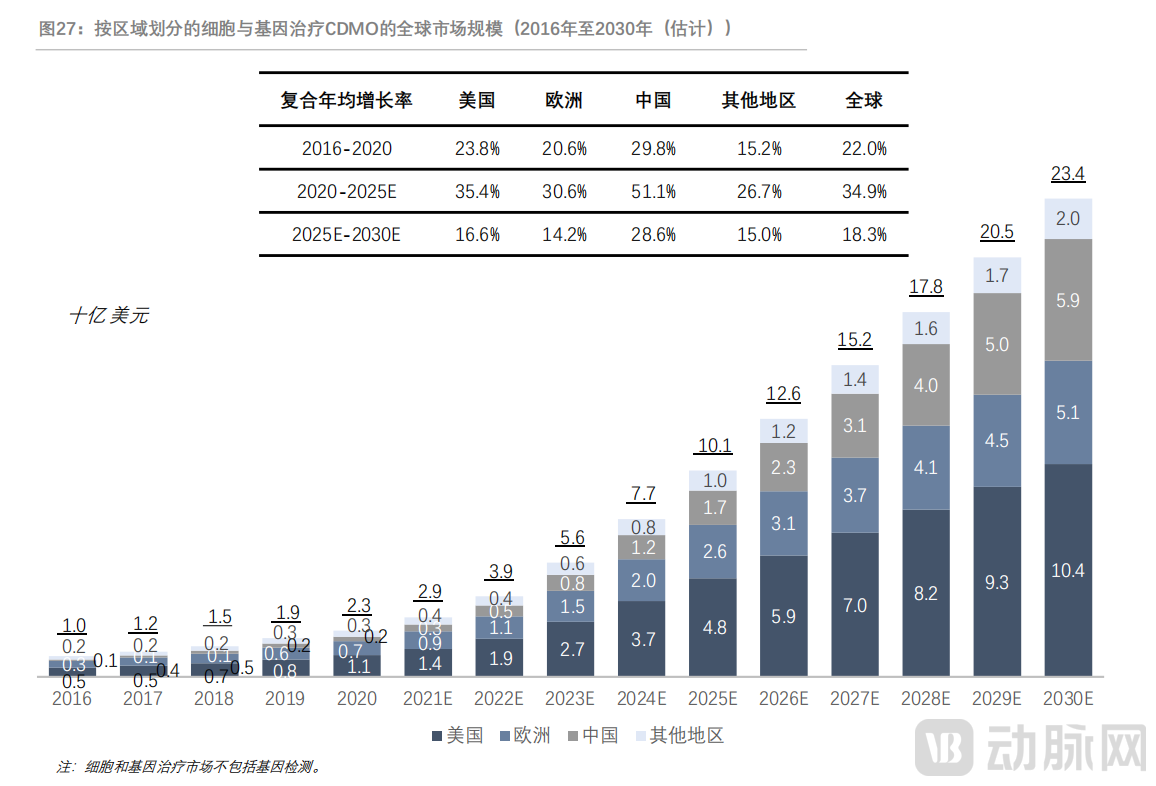
图源:弗若斯特沙利文
CGT CDMO公司通常拥有大型细胞或载体库,可以帮助药企选择适合的细胞或基因编辑病毒载体,并进行定制编辑和优化,减少药企试错成本,提高研发成功率。同时,其生产工艺、质检措施和监管处置可以帮助药企减少商业化成本,加速药品研发进程。
基因治疗是指利用载体将遗传物引入靶细胞,通过纠正或补充缺陷基因来预防和治疗疾病。基因治疗可通过体外(ex vivo)或体内(in vivo)策略来实现。体外策略使用从患者身上获取的靶细胞,经基因改造后注入患者体内。体内策略则类似一般药物,通过载体将遗传物质直接送入患者的靶器官或组织,以达到治疗效果。
在这其中,CGT的关键步骤在于有效地将基因递送到目标组织或细胞中,因此病毒载体尤为重要。腺相关病毒(AAV)是目前载体基因治疗的主流病毒载体。
AAV是一种小型无包膜细小病毒,作为递送系统具有许多优势,如无致病性、高效持续表达、易于操作、免疫原性低等。AAV载体携带的治疗基因(gene of interest,GOI)进入细胞后,将转录翻译为功能蛋白,达到治疗一系列疾病的目的。
重组腺相关病毒(rAAV)是经改造的AAV载体。改造后,AAV单链脱氧核糖核酸基因组中编码调节蛋白(Rep)和结构蛋白(cap)的DNA序列被剔除,替换成为所需的GOI表达载体。
目前,rAAV是推动基因治疗中长期治疗基因表达的最安全、最有效的基因输送载体。但作为一种由病毒基因组和多种结构蛋白组成的复杂生物制剂,rAAV产品的上游开发以及下游生产过程都面临着许多技术挑战。
一方面,上游开发聚焦如何提高rAAV的载体靶向性和特定细胞类型的转导能力。另一方面,下游生产关注如何实现无杂质载体生产的可扩展性和经济性。
产生rAAV最常见的方法是HEK293细胞中质粒DNA的瞬态转染。但存在一些局限性,包括有限的可扩展性,高昂的生产成本,可预测性和可复制性低,大规模生产未实现,以及空壳率高,有效性和安全性受影响等。
NewBiologix开发了专有DNA集成平台,其搭载的NewBiologix系统正致力于改善这些问题。
工程HEK细胞系降低空壳率
空壳率主要指的是rAAV载体制备过程中产生的大量空病毒颗粒。这些空病毒颗粒可能会影响rAAV载体的有效性和安全性。rAAV载体的免疫原性可能会因此增加,增加免疫毒性的风险。另外,空病毒颗粒会通过竞争细胞表面受体结合位点、内吞作用及胞内过程,影响rAAV转导效率。
NewBiologix系统由稳定工程的HEK细胞系组成,集成了rAAV生产所需的所有基因。悬浮液生长到高细胞密度,采用密度梯度离心法(DGC),使空病毒颗粒(不含DNA基因组)和含有部分DNA的病毒颗粒在较低的密度区间聚集,达到分离效果。
同时,NewBiologix系统将病毒载体基因整合到预定义的基因组位点中,以实现可预测性和可复制性,产生稳定、安全的高rAAV载体。
基因表达克服细胞毒性
内毒素释放发生在细菌死亡自溶、粘附在其他细胞及正常细胞生长和分裂过程中。载体内毒素可能诱导宿主产生免疫反应,对细胞产生毒性,还可能导致机体发热,引起全身性炎症反应,最终导致死亡。因此,制备过程中内毒素控制至关重要,也是其生产质控中的一大难点。
rAAV载体制备过程中,质粒DNA、转染的293T细胞、生产环境均有可能引入内毒素。在载体内去除内毒素有一定局限性,成本高且回收率差。
NewBiologix系统创新了内毒素控制方法——诱导基因表达,克服部分病毒蛋白的细胞毒性。这一方法具有可预测性和可复制性,同时绕开载体内去除肉毒素的高成本,达到降本增效的目的。
创新可诱导rAAV生产系统
大规模rAAV载体生产是保证临床需求、降低产品价格和提升研发效率的关键一环。但迄今为止,大规模生产仍然是rAAV未攻破的技术壁垒。
为达成这一目标,NewBiologix系统采用不同的衣壳蛋白,优化载体血清型,提高包装效率。针对不同靶向组织和细胞,系统可制备更高特异性和传导效率的rAAV,大大扩展了可满足的研发治疗需求范围。
适应度高的工程HEK细胞系、基因表达降低的内毒性、预定义的基因组位点,多项技术创新构建起一个可实现大规模产量和成本可控的生产平台。
在细胞治疗领域,NewBiologix也布局了生物信息学平台和基因安全港识别技术。
传统T细胞免疫治疗容易引起移植物抗宿主病,导致患者死亡。因此,科学家们采用基因工程制备出一种能够特异性靶向肿瘤细胞的T细胞,即目前领跑细胞治疗研发的明星产品CAR-T。
CAR-T中外来基因通过病毒载体完成转入,使其能够契合抗原受体修饰,克服肿瘤细胞的免疫逃逸。这一结合了细胞治疗与基因转移的技术成功后,正在被推广至更多的新型疗法研发,例如TCR-T、CAR-NK。
但是这项新技术伴随着一定风险。在基因工程制备CAR-T过程中,转基因整合到基因组是一种随机方式。这可能会引起安全问题,包括基因表达不稳定、内源转录中断和致瘤性。
针对这一技术风险,一种理想的解决方案是识别确定“基因组安全港(GSH)”,并将转基因转入至确定的GSH位点。这一方案能够提升工程细胞安全性,继而大大提高细胞治疗的安全性和有效性。
一个理想的GSH不能干扰功能性细胞基因,允许细胞类型的特异性表达和活性转录有效,免受沉默机制影响。因此其预定义基因组位点的识别确定具有一定挑战性。NewBiologix利用基因转移与NGS相结合,通过实验验证来确定可应用的稳健GSH。
同时,NewBiologix也开发了一个专有生物信息学平台。该平台基于细胞和病毒载体制备RNA/DNA库,利用NGS技术(包括短链阅读、长链阅读、光学映射)进行生物信息分析,进而形成高覆盖的生物信息序列库。这一技术方案可以应用在多个生物信息学层面,包括探索基因组可塑性、转录组学、表观基因组学、转基因完整性、完整细胞系表征、克隆评估等。
这一生物信息学平台将在细胞系开发过程中提供数据驱动决策,在安全性和监管要求中提供数据支持,最终与研发试验相结合,改进病毒载体的生成和制备。
NewBiologix联合创始人兼首席执行官Igor FischIgor Fish博士拥有20多年的生物技术和细胞系开发经验,曾在诺贝尔奖得主Sir Gregory Winter教授的实验室进行博士后研究。Igor Fish博士还是瑞士环诺曼第(Romandie)创新孵化器Fongit的现任总裁,致力于孵化生命科学初创企业。
公司联合创始人兼研发高级副总裁Nicolas Mermod博士具有20多年的分子生物技术研发经验,拥有日内瓦大学博士学位,并在美国加州大学伯克利分校进行博士后研究,后成为洛桑大学生物技术名誉教授、全职教授和生物技术研究所所长。Nicolas Mermod博士拥有多项关于表现遗传学调控原件和基因转移的专利。他的分子生物技术实验室团队发表过100余篇期刊论文,在真核基因表达控制领域获得认可。
这并非Igor Fish和Nicolas Mermod的首次合作。早在2001年,两位联合创始人共同创立了Selexis SA。Selexis SA是一家由高校学术成果转化而来的CXO公司,专注哺乳动物细胞系生成和蛋白质表达领域。
时隔21年,Igor Fish和Nicolas Mermod再次合作,联合创立NewBiologix。坚持技术创新,改变细胞系生产制备,正是两位联合创始人二十年不变的理念。
根据弗若斯特沙利文预测,中国细胞和基因治疗CMO/CDMO将是全球增长最快的市场,2020至2025年的复合年增长率为51.1%。
2022年3月,和元生物在上交所科创板正式挂牌上市,成为科创板基因治疗CDMO第一股。以和元生物为代表的生物技术公司,业务长期聚焦CGT,目前多以扩张产能为主要方向。
另一类进军CGT领域的是头部CXO企业。在看到CGT药物研发崛起后,此类公司以增加产线或收购并购的方式,布局基因与细胞治疗CDMO。
药明康德在2017年成立了无锡生基医药(药明生基),专注于细胞和基因疗法的CTDMO(合同测试、开发、生产外包服务)。2021年,药明康德又收购了OXGENE,在欧洲布局CTDMO。
康龙化成则通过收购产线成熟的CDMO公司Absorption Systems和Allergan Biologics Limited,打开其细胞和基因产品服务市场。
博腾股份走的是内生发展道路。2018年始博腾布局基因细胞治疗CDMO,后成立子公司苏州博腾生物制药。这一产线发展迅速,在质粒、慢病毒载体、细胞治疗三个领域的工艺技术都达到了国际前沿水平。公司财报显示,2022年基因细胞治疗CDMO增速达443%,并完成了5.2亿元B轮融资。
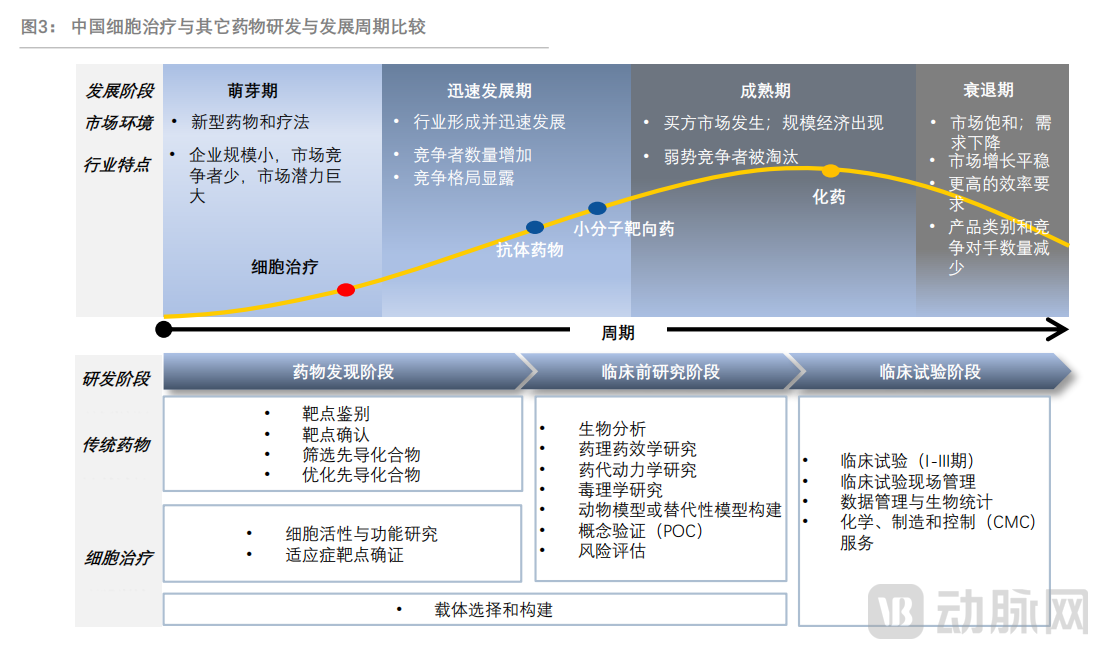 图源:弗若斯特沙利文
图源:弗若斯特沙利文
2022年以来,资本寒冬仍在影响药企的研发与生存。短期而言,这对于CDMO发展是个机遇。许多创新药企为降低成本、分散风险选择与CDMO合作,为其带来了短期业务增长,但同时也带来国内CDMO赛道内卷,甚至陷入价格战怪圈。
长期而言,赛道兴盛才能打造可持续发展的产业生态。CDMO需要创新技术、更新产能、提升工艺,才能够实现自身的长期发展。正如Igor Fish博士所说,面对未来,科学和创新将是取胜根本。





























