药物在人体内的效果取决于靶点的选择。在已经上市的药物中,所针对的最主要靶点可粗略归为5类:G蛋白偶联受体(GPCR)、离子通道、激酶、核激素受体和蛋白酶类。这其中,GPCR和离子通道都属于膜蛋白。
膜蛋白在细胞信号传导和物质运输中发挥了关键作用,不仅调节类别众多的生理学过程,还包括很多位于细胞表面的可成药靶点,可用于疾病诊断及药物治疗领域。单就人体内最大的膜蛋白家族GPCR来说,据不完全统计,FDA批准的靶向GPCR的药物总计475种,占所有FDA批准药物的34%。
GPCR是膜蛋白药物开发领域的重要靶点,与中枢神经系统疾病、心脏病、糖尿病、癌症等重大疾病密不可分。然而,由于GPCR结构不稳定、低表达等原因导致了GPCR蛋白获取难度较大,大多数GPCR的结构目前仍未被解析,进而难以基于结构设计GPCR药物,实现药物对于GPCR功能的准确调控。根据文献报道,在约800个潜在的GPCR靶点中,仅有134个被开发。也就是说,目前只有不到17%的潜在靶点被“药物化”。
此外,GPCR药物开发还面临更多其他挑战:GPCR结构和功能关系不明确、GPCR相关疾病的病理机制不清晰、GPCR测活技术难、药物开发的多目标优化及GPCR抗体药物开发难等。上述需求与挑战呼唤业界对这些受体进行深入研究。沃臻生物就是这样一家躬身入局的公司。
师从国内结构生物学奠基人,深耕膜蛋白领域20年
“从膜蛋白结构生物学的角度来说,我们大概经历了三个阶段。”沃臻生物创始人廖军博士说。
“第一阶段是上世纪80年代中后期,Harmut Michel、Johann Deisenhofer和Robert Huber三人因为解析了光合作用反应中心复合体的三维结构,获诺贝尔化学奖。拉开了膜蛋白结构生物学的序幕。尽管如此,当时的膜蛋白主要是从天然组织中获得,效率低下。”
第二阶段是90年代末,Roderick Mackinnon和Peter Agre等在膜蛋白异源表达、纯化和结晶方面取得突破,系统性解决了获取膜蛋白X-射线晶体结构的问题,并获得了2003年诺贝尔化学奖。
在国际上膜蛋白基础研究取得重大突破的同时,廖军也正在中国科学院生物物理研究所开展研究生训练,师从“中国结构生物学奠基人”梁栋材院士和常文瑞院士,从事结构生物学研究,夯实结构生物学的理论和实践。
2004年,廖军前往美国德州西南医学中心进行博士后研究,导师姜有星教授正是2003年诺贝尔化学奖成果“钾离子通道蛋白和离子选择性运输的原子基础”的主要贡献者之一。“这个成果促使我们加深了对阳离子通道选择性通透机制的了解,也标志着膜蛋白结构生物学研究可以系统化和常规化,离商业更近了一步。”廖军补充。
随着计算及技术和硬件设备等的突破,更为灵敏的电子显微镜及更智能的软件应运而生,能够捕获更加清晰的分子结构,解决了冷冻电镜分辨率低的困境。2013年,加州大学利用冷冻电镜实现了对膜蛋白结构近原子级解析,开启了冷冻电镜的新阶段,也使膜蛋白结构生物学进入突飞猛进的第三阶段。
从学术到产业,廖军已经在膜蛋白结构生物学中深耕超过20年。回国后廖军先后在上海科技大学担任教授及博导、中科院生物化学与细胞生物学研究所苏州研究院担任兼职研究员、以及在GE(上海)及其它生物科技公司担任科技顾问,专长于多次跨膜蛋白的表达和结构解析。
2022年,廖军全身心投入到实业中,创办了沃臻生物,致力于以多次跨膜蛋白和有挑战性的激酶为靶标,为全球药企和生物技术公司提供多次跨膜蛋白的表达、纯化和结构解析等技术服务。“尽管冷冻电镜已经可以实现高分辨率,但仍然有许多靶点不适合通过冷冻电镜进行解析,特别是很多成药性好的小分子量GPCR靶点。”廖军提到。
基于此,廖军及沃臻生物核心团队进行潜心研究。今年6月,沃臻生物发布突破性的MegaR技术,该技术能够实现此前无法解析的小分子量GPCR及这些GPCR与配体/药物形成的复合物的结构解析。
MegaR技术:无需GPCR处于激动状态,GPCR跨膜和膜外区域保持天然构象
“首要的问题是,膜蛋白一旦脱离天然的膜环境,很容易失活或改变功能特点”。冷冻电镜被大规模应用在GPCR靶点结构解析后,第一个挑战便是高质量蛋白样品的制备与纯化。
在膜蛋白的纯化过程中,首先需要选择适合的去垢剂才能使膜蛋白本身保持空间构象和活性;摸索到合适的去垢剂之后,将膜蛋白从细胞膜萃取出来,通过层析方法纯化。很多膜蛋白在去垢剂萃取后,稳定性变低,蛋白质工程技术的改造往往可以增强膜蛋白的稳定性。
“其次,数百个GPCR分子量在~37-50kD范围,例如占据80%的GPCR的rhodopsin-like家族,其自身分子量不适合冷冻电镜技术进行研究。通常的解决办法是促使GPCR处于激动状态,从而能够与下游信号通路的G蛋白形成复合物而获得冷冻电镜结构。但问题再次出现,利用冷冻电镜技术分析拮抗剂药物与GPCR的相互作用时,无法通过GPCR与下游信号通路的G蛋白形成复合物来获得。这个困难阻碍了拮抗剂药物的开发。”廖军说。据不完全统计,已经上市和正在研发的GPCR药物中拮抗剂的比例高达45%以上。
经过多年攻关,沃臻生物正式对外发布MegaR技术。据介绍,MegaR技术能够有效增大GPCR的分子量,且无需使GPCR处于激动状态,从而解决了拮抗剂与GPCR分子复合物的高分辨率冷冻电镜结构分析难题。MegaR技术的优势在于加速了多种亚家族GPCR与不同配体或药物之间相互作用的研发。
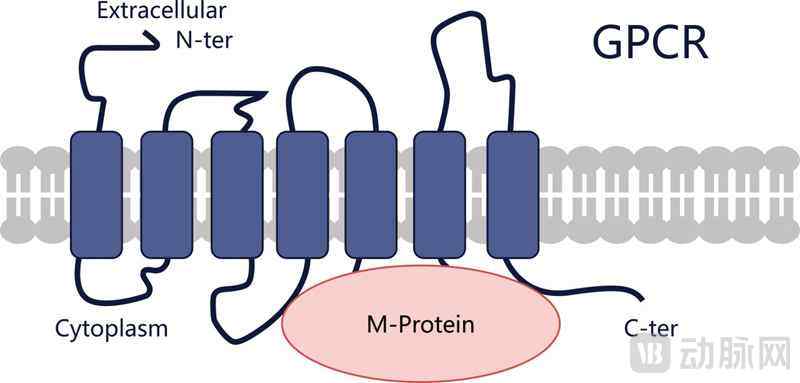
MegaR技术平台 受访者供图
MegaR技术通过基因工程技术在GPCR上融合长度仅为30个氨基酸的标签,最大限度减少了工程化改造对GPCR表达和正确折叠的影响。“融合标签不会与GPCR的跨膜螺旋形成连续螺旋结构,不改变GPCR跨膜螺旋的天然构象,保持了改造后GPCR蛋白的稳定性,且利于解析构象差异的各种类型的GPCR结构。纯化过程中加入的另外两个蛋白与这个30个氨基酸的标签形成紧密的复合体,并从两侧把它包裹在中间。通过调节标签与GPCR之间连接肽段的长度,可以使这两个蛋白与GPCR的其它部分形成更多的相互作用,蛋白颗粒整体呈现出具有较强刚性的空间结构。”廖军介绍到。测试结果表明,改造后的GPCR分子量可提高至90 kD以上,满足冷冻电镜结构解析的要求。
“MegaR技术在GPCR药物研发中同时还具有稳定性及先进性等优势。”廖军说。据介绍,经MegaR技术改造后形成的GPCR融合蛋白物能够在哺乳动物细胞中高效表达,极具稳定性,且在纯化过程中不容易解离,无需对形成复合物的纯化条件和电镜样品优化进行大量摸索。更具有突破性的是,MegaR技术能够对多种表达和纯化困难的GPCR及其配体或药物形成的复合物结构进行解析。截至目前,沃臻生物是目前世界上唯一解析了CCR8和GPRC5D结构的公司。
成功解析CCR8和GPRC5D的电镜结构,助力多种肿瘤突破性药物研发
趋化因子受体CCR8是一种7次跨膜的GPCR,其主要配体是CCL1。近年来,肿瘤免疫疗法在癌症治疗领域取得革命性突破。研究表明,通过抑制或清除特异性表达CCR8肿瘤微环境中的 Treg细胞,可以促进免疫疗法。目前全球尚无靶向CCR8药物上市,在研管线四十余条,竞争十分激烈。
“对蛋白的结构解析及与其单克隆抗体的复合物解析会为靶向CCR8的治疗性抗体开发提供有价值的信息。由于CCR8过小的尺寸,其表达和纯化也极为困难,致使其三维结构迟迟得不到解析,从而延缓了部分药物的开发进度。“借助MegaR技术,在增大CCR8的分子量后,我们以3.24Å的分辨率解析了CCR8在apo状态下的冷冻电镜结构,这会大大提升靶向CCR8药物的研发速度。”廖军说。
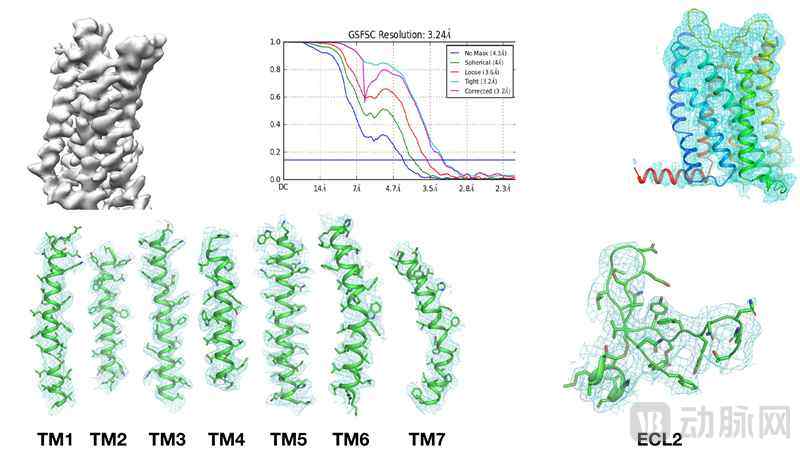 MegaR技术用于CCR8冷冻电镜结构解析 受访者供图
MegaR技术用于CCR8冷冻电镜结构解析 受访者供图
GPRC5D也是一种7次跨膜蛋白,属于孤儿受体。有关论文显示,GPRC5D在原代发性骨髓瘤细胞表面高表达,而在正常组织的表达仅限于毛囊区域,且65%的多发性骨髓瘤患者中GPRC5D有超过50%的表达阈值,其表达水平与靶点BCMA相对独立。因此,GPRC5D已成为治疗多发性骨髓瘤的靶标。
目前,靶向GPRC5D在研抗体管线有三十条,目前只有强生的Talquetamab今年1月份获批上市,其他部分领先的进入临床II期阶段。然而,这些抗体与GPRC5D靶点是如何结合的?抗体与靶点蛋白结合的亲和力如何进一步优化?这些问题的答案需要从GPRC5D与抗体复合物结构中得到解答,但由于GPRC5D是一个小分子量的孤儿受体,其结构一直没有得到解析。利用MegaR技术,沃臻生物成功解析了这个膜蛋白的结构,接下来解析受体与抗体复合物的结构将为上述问题提供清晰的答案。
“在成功表达、纯化和解析CCR8和GPRC5D两个高难度膜蛋白结构后,沃臻生物还将会进行技术迭代,以对GPCR家族更多膜蛋白结构进行解析,同时对离子通道、转运蛋白等跨膜蛋白和有挑战性的激酶进行深入研究。”廖军说。
“结构生物学不仅是极大地帮助人类在分子层面上理解复杂的生命活动,更为现实的意义在于,通过结构帮助我们设计出阻止或增强其作用的药物。特别是,基于结构的药物设计可以大大提高药物的精准性和特异性,最终造福全人类。”廖军补充。





























