偏头痛,一种复杂的神经系统疾病,其特征是反复发作的、通常是单侧的搏动性剧烈头痛,并常伴随恶心、呕吐以及对光线和声音的敏感。2021年,全球偏头痛患者总数已达约 11.6亿人,占全球人口的 14%~18%。
不仅如此,偏头痛的危害远超“头痛”本身,它是一种高致残性神经血管性疾病,长期反复发作会对身体、心理、社会功能造成多维度、深层次的损害,还可能与卒中、癫痫、抑郁、认知障碍共病,引发严重后果。
1999年,西交利物浦王旻艳教授到英国开展科研工作,并于次年在英国偏头痛基金的资助下进入偏头痛研究领域开始博士课题。她告诉橙果局,自上世纪60年代开始,人们逐渐从医学和生物的角度试图解释偏头痛的源由,随着80-90年代神经影像学的发展,人们终于意识到神经血管网络是潜在的发病机制。但即便如此,目前科学家对该疾病分子致病机制的认知依然甚少,临床上,能安全有效地预防和治疗偏头痛的药物依然寥寥无几。
“疾病致病机制的研究和药物研究是相辅相成的,需要尽量做到匹配。”她如是说道。
“补赎神学”到神经血管假说
偏头痛的发病机制,经历了从“神论”到科学的历史变迁。
12 世纪盛行的“补赎神学”,疼痛被视为模仿基督受难、净化灵魂的途径。人们把偏头痛认为是上帝的暗示。修女希尔德加德终生受周期性视觉先兆与单侧搏动痛困扰。但她在《认识主道》中把典型的锯齿状闪光描述成“闪耀的火轮”“活的光网”,并称这是“上帝用光在我灵魂里写字”。
到了17世纪,现代神经学之父托马斯·威利斯提出血管学假说,认为是血管舒张刺激神经造成了头痛。这一时期,阿司匹林、麦角胺等非甾体类抗炎药问世。尽管这类药物至今仍被用于疼痛管理,但最早却并非为偏头痛治疗研发。
并且,尽管血管学假说将偏头痛与神经末梢网络连接起来,但仍难以解释常伴随头痛出现的诸多先兆反应,如视觉障碍、恶心呕吐等。后来另一位医生爱德华·利文提出了“神经风暴”的理论。她发现偏头痛发作前的症状大多受到丘脑和迷走神经等影响,认为偏头痛是由于源发性神经紊乱而导致的。
遗憾的是,人们后续的研究过程中发现偏头痛的先兆反应并不是由丘脑和迷走神经等触发的,而是受到更复杂的中枢神经活动的影响。在接下来几十年的时间里,偏头痛都没能获得新的突破。直到19世纪影像学的发展对偏头痛发病机制的研究产生了革命性影响,推动了从“血管假说”向“神经血管理论”的根本转变。
通过功能性影像(fMRI、PET)等技术,患者在发作时存在血管扩张的同时,存在脑干、下丘脑和大脑皮层等中枢区域持续激活。这提示了人们,偏头痛的核心机制在于中枢敏化与神经调控异常。
通过PET 技术,科研人员发现在偏头痛发作初期,中脑导水管周围灰质(PAG)、缝核(raphe nuclei)等区域脑血流持续升高,即使疼痛缓解后仍存在激活,提示这些区域可能是偏头痛的“启动器”或“发生器”。
fMRI 研究进一步发现,下丘脑在发作前48小时即被激活,与昼夜节律、激素波动等功能紊乱密切相关,提示其在偏头痛前驱期起关键作用。
fMRI 实时成像显示,视觉先兆患者的枕叶皮层活动,与皮层扩散性抑制(CSD)的生理特征高度一致,首次在人类活体中验证了CSD是偏头痛先兆的神经基础。
此外,高分辨率 MRI还发现,慢性偏头痛患者存在白质与灰质微结构改变,如神经元突密度下降、轴突损伤等,提示长期反复发作可导致脑结构适应性或病理性重塑。这些改变与病程长度、发作频率呈正相关,说明偏头痛不仅是“发作性疾病”,也可能是一种慢性进展性脑网络疾病。
与此同时,偏头痛治疗的药物也在陆续问世。
第一代偏头痛药物的研发从上世纪70年代末,九十年代获美国FDA批准。这一类药物以曲普坦类药物为主,目前在国内是一线治疗药物。
第二代是特异性靶向CGRP和其受体类药物,从2018年以来陆续获FDA批准,这一类药物主要根据偏头痛神经血管理论进行研发,它的问世给偏头痛患者带来了巨大福音。
曲普坦类药物主要用于急性偏头痛治疗。由于大量使用往往会导致心血管收缩和过度使用性头痛,不适用于慢性偏头痛。
现有的CGRP和其受体类药物主要依赖外周血管作用。由于无法穿过血脑屏障,其中枢作用能否体现则取决于药物是否能够穿越血脑屏障进入中枢神经系统。
根据国外临床试验的数据,无论是曲普坦类药物还是CGPR类受体药物,其药效依从性均不足30%。目前对偏头痛治疗的临床需求依然未得到满足。
“慢性偏头痛, 以及青少年、孕妇等特殊群体的用药都还没有得到有效解决。”王旻艳教授表示。尽管在近些年偏头痛药物研发领域发展迅速,但在诊断层面,该疾病还缺少生物标记物。王旻艳教授认为更需要重视药物对中枢层面血管动态变化的作用,这是目前偏头痛研究领域仍然存在的研究局限。
25年“追光”之路,搭建中国偏头痛研究全链条平台
在过往的25年中,针对偏头痛的发病机制,王旻艳教授从致病机制、分子靶标、药理、药效等多个方向进行了探索。她告诉橙果局,科研人员在很多时候需要探索从无到有的工作,尤其是偏头痛这样研究起步晚、无实体病灶的疾病研究领域。
“你要研究它,就需要有自己的临床前研究平台,需要能够匹配临床症状和病理机制的模型,需要建立药理学和药效学的复杂系统。”她向橙果局解释。作为一种复杂的神经血管性疾病,偏头痛的研究必须是从多角度、多维度展开的。
这份工作从她博士期间开始,一直延续到她成为独立PI,以及回国后继续搭建更为综合性的偏头痛研究平台。她的团队构建了独特的基于偏头痛神经血管疾病的多元化动物模型, 充分体现偏头痛的‘偏‘和‘神经血管’,多维度的神经血管偶联监测为国际首次、且目前国内唯一,能够解决偏头痛评价模型不足的研发瓶颈, 提高预测准确率、缩短研发周期、加速偏头痛新药开发进程。
基于团队优于国内行业常规方法的优势,她长期专注于偏头痛发病机制与药物靶点研究,在偏头痛分子机制、精准医疗方向、以及新药靶点发现方面取得了多项突破。
2014年起,带领团队与美国爱荷华大学Russo教授合作针对CGRP的中枢调控机制开展了深度合作,并联合发表了多篇论文。基于CSD作为偏头痛的关键致病机理的研究发现,CSD通过激活大脑皮层和杏仁核CGRP合成机制,揭示了CSD后这些脑区持续敏化和情绪变化的关键机制。他们还提出CGRP依赖性中枢敏化和脑血流变化的耦联。这些成果为第二代靶向CGRP药物的药理作用奠定了坚实的基础。


2016年起,她带领团队成功揭示了对应激压力因素敏感的TRPA1离子通道通过激活SFKs 和ERK2促进大脑皮层扩散抑制的传播和相关的脑血流变化这一偏头痛发作的关键神经电生理活动;此外,TRPA1还促进中枢和三叉神经炎性以及诱发小鼠畏光等行为。该研究为TRPA1作为新型药物靶点提供了理论支持,拓展了偏头痛中枢机制的研究视野。

同期,她的团队与英国利物浦大学、澳大利亚莫道克大学合作,还发现Src家族激酶(SFKs)的激活在CSD、神经炎症、偏头痛畏光等机制中具有重要的调节作用。其中SFKs 具有性别特异性调节作用。这是关于畏光敏感分子基础的重要进展。该项研究突出了SFKs在偏头痛病理生理学中的作用,揭示了性别特异性的影响,并提出了新的精准医疗预防和治疗方向。值得关注的是,这些重要发现已成功入选偏头痛领域核心著作 ——《偏头痛疼痛管理》(2024 年 10 月)的六大偏头痛药靶。该结论出自为该书撰写的第九章 “Src family kinases in migraine”。


2025年,王旻艳教授团队首次揭示了一个从NEAT1到microRNA,再到痛觉相关基因的“连锁反应”过程。这是首次从分子机制层面解释偏头痛中的光敏症状如何产生。这项研究发现阻断NEAT1或Trpm3蛋白表达可显著减轻小鼠的光敏感反应,提示该通路是偏头痛畏光症状的关键机制。
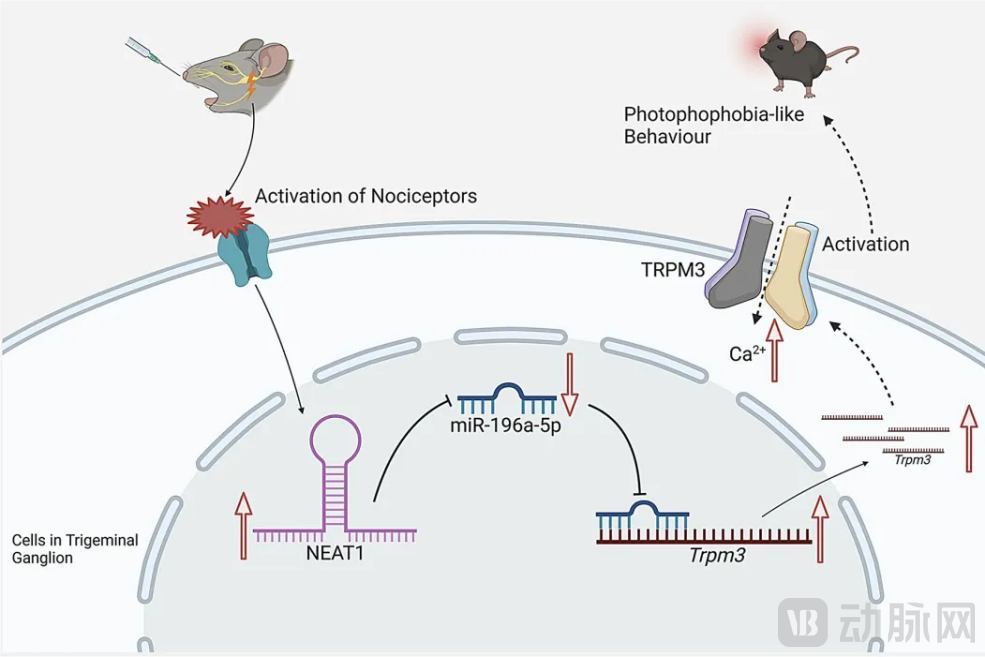
这不仅加深了对偏头痛机制的理解,还意味着NEAT1可能成为未来治疗光敏感症状的新靶点。
“这项研究为解释偏头痛中令人困惑的光敏症状提供了新的视角,也为未来开发针对性的治疗手段打开了可能性。”王旻艳教授在当时的采访中这样说,“它让我们更深入地理解大脑中发生了什么,并指明了可能的干预点。” 此项研究成果获选为《头痛杂志》(Journal of Headache and Pain)2025年5月的特色文章,并于同年举行的国际头痛大会上由团队作了学术报告。。
她和团队的研究涵盖了从分子、细胞到行为等多个层面,系统性地解析了偏头痛的关键机制,尤其在畏光和中枢敏化等领域做出了开创性的贡献,强调性别差异和个体差异在偏头痛中的重要性。
一路走来,王旻艳教授为发现偏头痛热门药靶CGRP,新型靶点TRPA1, SFKs等做出了许多贡献,为开发新型抗偏头痛药物与未来精准医疗指明了方向。
在国际合作与平台建设方面,王旻艳教授于2013年创建了西浦神经生物学研究中心,构建了系统的偏头痛研究平台,并与英国利物浦大学等国际机构保持长期合作,为英国医学研究基金会(MRC)和英国研究创新基金会等评委,显著提升了我国在该领域的国际影响力。

王旻艳教授实验室主要研究内容
被低估的15%,偏头痛从“冷门”推向“主战场”
20余年的沉淀,王旻艳教授已成为我国偏头痛基础研究领域具有国际影响力的学者之一。她的研究不仅推动了偏头痛分子机制的科学认知,也为临床精准治疗和新药研发提供了坚实的理论基础。
但在她看来,这些仍然不够。
不同于肿瘤、老年痴呆症这些比较棘手的问题,偏头痛没有那么大量的创新药公司去投入,也没有那么大量的科研人员群体。在学术层面,这个研究领域的学者数量、研究项目也远不及前两者。
王旻艳教授告诉我们,她同期的博士中一直从事这个领域的人并不多,大多转行,继续活跃在这个领域的人越来越少。二在临床、政府,甚至患者和家属角度,偏头痛所造成的社会经济负担和身体负担一直被忽视。
但实际上,偏头痛的发病率很高。世卫组织公布的偏头痛发病率大概在15%,即每10个人中,越有1.5个人正在忍受偏头痛。但事实上,由于诊断技术的缺乏和社会的忽略,偏头痛的发病率很可能更高。
“相比肿瘤和神经退行性疾病,偏头痛的研究是滞后的。”她这样表示。
过去,由于认知的匮乏,偏头痛的大量研究仅围绕疼痛这一表象。且由于无实际病灶,相关的分子机制、影响脑区和人群都难以确认。在各种资源匮乏的情况下,偏头痛的研究的进步一直相对缓慢。
随着国际头痛日的设立、各类学术会议的推动,以及社区层面宣传的不断加强,偏头痛这一疾病逐渐受到更多关注,相关研究队伍也日益壮大。目前,全球范围内已有数百个实验室专注于偏头痛的基础与临床研究。
组织层面上,除了Migraine Trust International Symposium(MTIS)这样的“老牌”学术会议,国际头痛学会(International Headache Society, IHS)每两年在全球轮流举办国际会议。王旻艳教授几乎每届都在参加。


(上为2025 IHC at Sao Paulo, 下图为2019 IHC at Dublin)
在中国,偏头痛的基础研究起步相对较晚。真正系统性地开展偏头痛机制研究的,几乎是从王旻艳教授实验室开始的。2024年,中国的偏头痛研究者们在重庆成功举办了第一届中国头痛大会。次年,第二届盛会在南京继续。

图片来自2025头痛大会
王旻艳教授认为,中国头痛大会的召开具有里程碑式的意义,它标志着中国学术界和医疗界对偏头痛疾病负担的重视达到了新的高度。
从辉瑞到本土管线,偏头痛创新药的中国时刻
2024年,辉瑞全新一代特异性偏头痛治疗药物Remegepant获得中国国家药品监督管理局批准,靶向CGRP受体,用于成年人有或无先兆偏头痛的急性治疗。这是目前在全球唯一在美国FDA和欧盟EMA均获批的,同时具备急性及预防性治疗偏头痛适应症的药物。它的获批不仅为偏头痛患者带来了全新的治疗选择,更是带动了国内对该疾病机制研究的关注。
“这款药物在国内的上市也促进了本土科研力量的生长,我们很欣喜的看到越来越多的研究团队、临床医生,以及产业力量开始加入这一领域,逐步形成了中国的学术共同体。这对于推动偏头痛研究、改善患者生活质量,具有深远意义。”她这样感叹。
更让她感到惊喜的是,在近年一次CPHI上,王旻艳教授还了解到国内已有创新公司在布局偏头痛靶向药的研究。
“我觉得非常欢欣鼓舞,在学术界外,还有创新公司在考虑偏头痛药物的产业化。”她这样表述。作为深耕偏头痛领域25余年的学者,王旻艳教授相信这一类药物在国内市场的潜力。这是一个未被挖掘的,充满潜力的蓝海市场。
“尤其是长三角和珠三角地区,这里有非常活跃的创新氛围,创新公司门对药物研发有非常前沿的认知,政府也积极支持相关产业的发展。”她这样感叹。她认为,在国内研发经验的赋能和国内政府对创新药的扶持下,中国的很快能够迎来自己的偏头痛创新药。
过往的研究中,王旻艳教授也时常与临床医生沟通疾病的临床诊疗现状,与国外企业进行药物靶标测定等创新研发合作。在她看来,临床-科研-产业,其实存在不可分割的关系。不同的角色承担的不同的工作,而正式这些工作的融合与链接,组成了医药研发到产业的闭环。
十年前,中国的医药研发以仿制为主,创新研究很难渗透。而随着中国创新药的发展,偏头痛药物研发的创新也逐渐找到了下游转化路径。
目前国内涉足偏头痛创新药研发的企业仍属极少数,在王旻艳教授看来,这些企业研究方向与偏头痛“神经-血管偶联”理论的契合度仍有待提升。从她的团队过往的研究成果来看,即便所开发的抗体类药物无法穿透血脑屏障,仍需系统评估其对神经-血管单元的影响。因此,药物研发不仅要关注外周血管的反应,更需要重视药物对中枢层面,尤其是与皮层扩散性抑制(CSD)相关的血管响应。
这要求研究模型必须贴近临床病理机制,优先采用基于神经-血管偶联理论构建的多元化动物模型,并在此基础上,结合慢性偏头痛的特异性模型进行验证与补充。
她强调通用模型应与疾病发作特异性适应症并重,从而提升新药研发的有效性与转化潜力。
接下来,王旻艳教授希望能够与创新药企有更多研发方向的合作,将多年在偏头痛研究领域的研究、建立的平台,以及模型转化到药物研发过程中去。过往,由于起步较晚,中国创新药企在选择研发靶点相对需要更为谨慎,在热门靶点上进行竞争的同时,也要考虑到药物应答率、国内市场容量等问题。
而随着部分本土创新企业的成功,王旻艳教授认为当下医药研发创新的主题是国际化和差异化竞争,因此中国药企需要更为前沿的尝试。
而回到中国偏头痛药物的研发,王旻艳教授认为中国人口基数大,患者群体数量多,但至今尚无一款原研药物上市。这背后是市场,也是患者的诉求。她希望能够通过产、学、研、医多方的共同努力,实现偏头痛原研药物零的突破。




























