2023年7月14日,纽约大学朗格尼医学中心的手术室里,一场特殊的手术正在进行。57岁的Maurice Miller因脑部肿瘤已经脑死亡,但他的身体即将承担一项前所未有的科学使命——接受来自一头经过基因改造的猪的肾脏和胸腺。Miller生前一直希望捐献器官,但因患有癌症而无法实现这个愿望。最终,他的家人决定将他的整个身体捐献给科学,让他以另一种方式延续生命的意义。
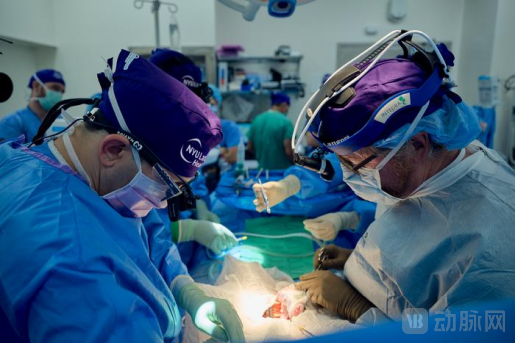
图:2023年的猪肾移植手术(来源:Joe Carrotta for NYU Langone Health)
在接下来的61天里,这位逝者成为了"历史上被研究得最深入的人类之一"。研究团队对他体内的猪肾进行了几乎逐日的监测,记录下免疫系统对这个跨物种器官的每一次反应。这不仅创下了基因改造猪器官在脑死亡人体内存活时间的最长记录,更重要的是,研究人员首次证明了一个此前被认为极其困难的命题:异种移植的排斥反应是可以被逆转的。
2025年11月13日,《自然》杂志同期发表了两篇重磅研究论文,详细披露了这项研究的完整结果。这两篇论文不仅为移植医学界带来了振奋人心的消息,更为解决全球器官短缺危机指明了一条可能的道路。
要理解这项研究的重要性,我们首先需要认识到器官短缺问题的严峻性。根据国际器官捐献与移植注册数据,全球有超过34万名患者在等待器官移植,其中至少有2.3万名肾脏移植等候名单上的患者因未等到器官而去世。更令人震惊的是,全球有超过266万名接受透析治疗的终末期肾病患者,但仅有5.65%的患者能获得器官移植的机会。
这个数字还在不断增长,以肾脏移植为例,随着人口老龄化以及糖尿病、高血压和肥胖等疾病的流行,使得终末期肾病患者持续增加。对于这些患者而言,透析是维持生命的唯一选择。更残酷的是,透析平均只能维持约5年的生命。
正是在这样的背景下,异种移植——将一个物种的器官移植到另一个物种身上——被寄予厚望。在过去三年中,医学界已经进行了十几例将猪器官移植到人体的尝试,涉及心脏、肾脏、肝脏和胸腺。但现实是这些器官大多数最终因功能丧失而被移除,部分接受者在移植后不久便离世。器官排斥反应就像一堵无形的墙,始终横亘在异种移植通向临床应用的道路上。
这项研究的成果以两篇论文的形式同时发表于《自然》杂志,它们从不同角度对同一项实验进行了深入剖析。
第一篇论文由Brendan J. Keating领衔,汇集了70多位研究者,采用了大规模多组学分析方法——包括转录组学、蛋白质组学、免疫组学和空间转录组学——对异种移植物和宿主血液进行了为期61天的全面监测。

(来源:Nature)
第二篇论文则由Robert A. Montgomery和Megan Sykes担任通讯作者,汇集了50多位研究者,从生理学和免疫学角度提供了首次针对猪到人肾移植的长期生理、免疫和传染病监测。

(来源:Nature)
两篇论文相辅相成,一篇聚焦于分子层面的详细机制,另一篇关注临床层面的生理表现和免疫动态,共同构建起了对这项61天异种移植实验的全景式理解。
一个关键的选择:最小改造策略
与许多研究者试图通过大量基因编辑来"改造"猪器官不同,Montgomery团队做出了一个大胆的决定:他们选择了最小基因改造策略。移植的猪肾只进行了单一基因改造——敲除GGTA1基因,这个基因负责产生一种叫做α-半乳糖(alpha-gal)的糖类抗原,它是引发人体超急性排斥反应的罪魁祸首。
过去的许多研究采用了多重基因改造和激进的免疫抑制方案,虽然在一定程度上延长了器官存活时间,但这些复杂的改造使得研究结果难以解读,也使得监管审批变得异常困难。Montgomery团队希望评估的是:仅做最小程度的基因改造,配合临床已批准的免疫抑制药物,是否就能让猪肾在人体内发挥作用?
答案是肯定的,而且比他们预期的要好。
除了肾脏本身,研究团队还做了另一个关键决定:同时移植猪的胸腺。这个小小的腺体在免疫系统中扮演着"教师"的角色,能够训练免疫细胞识别什么是"自我"、什么是"外来威胁"。研究者推测,猪胸腺可能帮助人体免疫系统学会将猪器官视为自身的一部分,而不是需要攻击的外来入侵者。
最初的惊喜:猪肾立即开始工作
手术后的最初几天,移植的猪肾带来了令人振奋的表现。它立即开始产生尿液,维持了稳定的血压和血流,电解质水平保持正常平衡。更重要的是,Miller的身体完全摆脱了对透析的依赖。这个看似简单的事实背后,蕴含着重大的科学意义:一个来自完全不同物种的器官,竟然能够在人体内履行维持生命的基本功能。
然而,真正的考验才刚刚开始。人体免疫系统是一个极其复杂而精密的防御网络,它不会轻易接纳任何"外来者",哪怕这个"外来者"正在帮助身体维持生命。
术后第10天的活检结果揭示了一些耐人寻味的现象。研究者在肾小球中发现了IgM和IgA抗体沉积,早期补体成分被激活,甚至出现了系膜溶解——这种免疫反应模式在传统的人对人肾移植中从未出现。
不过尽管早期出现了这些看似不祥的变化,肾功能却依然稳定,没有蛋白尿的迹象。这种独特的免疫环境特征提示:猪到人的异种移植可能遵循着与传统移植完全不同的免疫规律。
第33天:危机与转机
到了术后第33天,研究团队预料中的挑战终于来临。血清肌酐水平突然飙升——这是肾功能急剧下降的明确信号。活检证实了医生们的担忧:抗体正在攻击这个外来的器官,供体特异性IgG抗体大量增加,典型的抗体介导排斥反应(AbMR)正在发生。
如果无法控制这次排斥反应,研究可能就此终止。不过,这次危机也成为了验证治疗策略的绝佳机会。研究团队迅速启动了一套联合治疗方案:血浆置换清除循环中的抗体,类固醇抑制炎症反应,pegcetacoplan(一种C3/C3b补体抑制剂)阻断补体系统对猪细胞的攻击,兔抗胸腺细胞球蛋白(rATG)则进一步抑制免疫反应。
令人振奋的结果出现了:肾功能完全恢复正常。可以说,这是医学史上第一次证明异种移植的排斥反应可以被逆转。正如马里兰大学医学院的Muhammad Mohiuddin博士所评价的:"在我看来,这是如何逆转排斥反应的首个证据。"
第49天:又一次考验
然而,免疫系统并未就此罢休。到了第49天,活检显示了一种完全不同的排斥反应模式:这次不再是抗体在主导,而是大量炎症细胞浸润到了肾脏表面。这是一种细胞介导的排斥反应,与抗体介导的排斥反应合并发生,组织学检查显示T细胞受体出现了多样化,一种受限的TRBV2/J1克隆型正在扩增。
面对这次新的挑战,研究团队使用了一种破坏T细胞的免疫抑制剂。再一次,治疗取得了成功,肾功能又一次完全恢复。
到了第61天,研究团队决定结束这项实验,虽然此时那颗猪肾仍然功能良好,持续地产生着尿液,维持着Miller身体的生命支持功能。
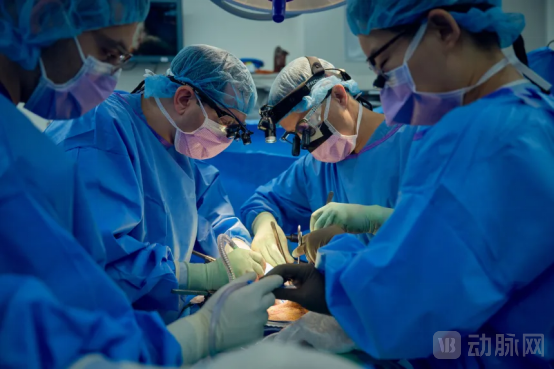
图:第61天研究人员通过手术切除被移植的猪肾(来源:Joe Carrotta for NYU Langone Health)

图:经过 61 天观察后取出的猪肾(来源:Joe Carrotta for NYU Langone Health)
61天的存活期不仅创造了纪录,更重要的是,这61天的每一天都被精心记录、深入分析,为科学界留下了一份关于异种移植免疫反应的详尽图谱。
揭开免疫系统的"作战地图"
这61天的密集监测,让研究团队得以前所未有地窥视人体免疫系统对异种器官的反应全貌。通过绘制5,100个表达的猪和人类基因图谱,精确定位体内的每一个免疫细胞,研究者们描绘出了一幅精细到"几乎逐日"的免疫反应动态图景。
术后第10天,血液中的浆母细胞、自然杀伤细胞和树突状细胞开始悄然增加,IgG和IgA类型的B细胞克隆开始扩增。
这些变化一直持续到第28天,为第33天的排斥反应埋下了伏笔。与此同时,从第21天开始,T细胞的频率也开始上升,移植物组织中出现了促纤维化的小管和间质损伤的早期迹象。
到了第33天排斥反应高峰时,研究者发现移植物中最丰富的人类免疫细胞是CXCL9阳性的巨噬细胞,它们在IFN-γ(一种关键的炎症因子)的驱动下,引发了I型免疫反应。更有趣的是,研究者首次观察到激活的猪驻留巨噬细胞与浸润进来的人类免疫细胞之间存在着复杂的相互作用。
在第21到33天期间,研究者还识别出了三个重要的组织损伤分子标志:S100A6、SPP1和COLEC11。这些分子的出现预示着促纤维化损伤正在发生,为将来开发早期干预策略提供了潜在靶点。
蛋白质组学分析则揭示了一个有趣的现象:人类和猪的补体系统同时被激活,就像两套防御系统在同一个战场上各自作战。而在使用pegcetacoplan进行补体抑制治疗后,人类补体成分明显减少,这解释了为什么联合治疗能够成功逆转排斥反应。
最关键的发现或许是关于T细胞的。深入的免疫学监测显示,Miller体内原本就存在一些对猪细胞有反应性的T细胞克隆。移植后,这些"沉睡"的克隆逐渐被唤醒、扩增,并获得了效应表型——它们变成了攻击移植物的"战士"。在第33天的排斥反应发生时,这些T细胞已经浸润到移植物内部。
这个发现揭示了一个重大挑战:即使使用了强效的免疫抑制药物,这些预先存在的异种反应性T细胞仍然难以完全控制。
但研究的价值不仅在于发现问题,更在于提供解决方案。通过识别血液中的早期生物标志物,研究者为未来开发预警系统指明了方向——如果能在肾功能下降之前就检测到排斥反应的征兆,临床干预将有更大的成功机会。
这项研究在医学界引发了广泛关注。加州大学旧金山分校肾脏和胰腺移植项目联合主任Minnie Sarwal博士虽未参与这项研究,但她对结果给予了高度评价。"61天的稳定肾功能是新颖的概念验证,这证实了基因工程猪肾可以在人体循环中维持生理功能。"
她还特别强调了这项研究的转化价值:"它弥合了我们之前在短寿命临床前模型上所做的工作与真正的临床可行性之间的差距,尽管这显然不是长期的,但61天比几小时或几天要好得多。"
作为免疫抑制药物设计领域的专家,Sarwal博士还指出了另一个重要发现:现有的临床治疗方案在异种移植模型中同样有效。"那部分并不具有突破性,但我认为非常令人欣慰的是,我们目前的治疗方法在该模型中会起作用,"她说。
研究负责人Robert Montgomery博士则对未来充满信心。"我们在这方面做得越来越好,我认为这就是我想传达的信息,会有起伏,任何值得做的事情都不会没有一些并发症。但都是可以解决的。"
值得一提的是,就在这项研究成果发表前不久,新罕布什尔州的Tim Andrews创造了一个更令人振奋的记录。作为美国第四位接受基因改造猪肾的活体患者,他体内的猪肾持续功能维持了271天。虽然最终因功能下降而不得不移除器官,但在那之前,Andrews的生活质量显著提高,他能够长距离步行,甚至在波士顿红袜队的比赛中开球。
这个案例也进一步证明,异种移植不仅在技术上可行,更能实实在在地改善患者的生活质量。
当然,科学界也清醒地认识到这项研究的局限性。毕竟这只是一例病例,61天虽然创造了纪录,但距离真正的长期移植仍有距离。更重要的是,研究揭示出的那些预先存在的异种反应性T细胞和针对未知表位的抗体,仍然是横亘在前方的重大挑战。
但Montgomery团队已经准备好了下一步行动。他们刚刚获得资金支持,计划在另外20名患者中进行类似的研究,以验证免疫反应的一致性并优化治疗方案。这不仅是对研究结果的复制验证,更是向临床应用迈出的关键一步。
更令人兴奋的是,这项研究识别出了多个潜在的免疫调节靶点。CXCL9阳性巨噬细胞通路、IFN-γ驱动的炎症通路、特异的补体激活途径、T细胞受体多样化机制,以及促纤维化损伤相关的分子标志(S100A6、SPP1、COLEC11),每一个都可能成为开发新型免疫抑制药物的"可药物化的分子检查点"。
这意味着,未来的治疗不再需要依赖广谱的免疫抑制,而是可以针对异种移植特有的免疫通路进行精准干预。
这项研究的意义也远不止于肾脏移植。可以说它为整个器官移植领域打开了一扇新的大门,心脏、肝脏、胰腺、肺,所有这些面临供体短缺的器官系统,都可能从这项研究的发现中获益。
当然,这条路并不平坦。科学上,仍需要识别和消除那些未知的免疫原性表位,找到控制预先存在的异种反应性T细胞的方法;伦理上,需要建立完善的异种移植伦理框架,确保感染安全性,制定严格的患者选择标准;社会层面,也需要提高公众接受度,解决医疗保险覆盖和成本效益等现实问题。
但正如Montgomery博士所说,这些都是可以解决的。关键是,现在我们有了一个明确的方向,有了扎实的科学数据,有了可行的治疗策略,还有了一个振奋人心的概念验证:猪的器官确实可以在人体内发挥作用,排斥反应确实可以被逆转。
可以说,这项研究不仅为科学界留下了宝贵的数据和见解,更为全球数以万计等待器官移植的患者点燃了希望。




























