信达在小核酸领域的布局思路日渐清晰起来。
11月10日,信达宣布了自圣因生物引进的siRNA药物IBI3016的首次人体临床Ⅰ期研究的主要结果,该结果在2025年美国心脏协会(AHA)科学会议数字化壁报专场展示。IBI3016表现出初步的降血压效果和较好的安全性。
此前不久(10月30日),信达还公开了siRNA的专利WO2025223537A1,专利涉及到INHBE靶点的小核酸药物研发情况。
在半个月的时间里,一款自研产品和一款引进产品同时取得了明显进展,这表明信达在小核酸领域的研发力度加大了。
最近一段时间,大家对信达的关注点都集中在GLP-1减重药玛仕度肽和双抗IBI363身上。如今信达的小核酸药物在半个月之内接连取得进展,这无疑向外界表明信达要在小核酸领域“大展拳脚”了。
信达在小核酸领域属于后来者。
2023年的12月27日,信达与圣因生物宣布达成战略合作协议,共同开发小核酸候选药物SGB-3908,用于治疗高血压。这是与小核酸有关的内容首次出现在信达的官方信息中。通过此次合作,信达将获得独家选择权并可在未来支付行权费以获得SGB-3908在全球不同范围内的独家开发、生产和商业化的权利。彼时市场上已有多款小核酸产品上市,在研管线也在持续增加。
信达上市之初(2018年),其在研管线以肿瘤产品为主,覆盖PD-1/PD-L1、VEGF、CTLA-4等多个靶点。另外,信达还有一款治疗高脂血症的产品IBI-306,靶向PCSK9。2023年8月,信达的IBI-306获批上市,用于治疗原发性高胆固醇血症及混合型血脂异常,信达在代谢与心血管领域的布局开始迎来收获。
此后不久,随着代谢与心血管领域的重磅产品玛仕度肽Ⅲ期临床试验接近完成,信达开始把目光延伸到新的研究领域。2023年,小核酸开始成为医药行业的“黑马”,诸多药企都开始关注这一领域。诺华siRNA新药Inclisiran获批后的快速放量,让创新药企开始意识到小核酸药物的潜力。
Inclisiran(商品名Leqvio),于2020年、2021年分别获欧盟、FDA批准上市,用于治疗成人高胆固醇血症及混合性血脂异常。凭借每年仅需2针的长效性优势,Inclisiran销售额迅速增长。2021年全年的销售额为1200万美元,2022年增长到1.12亿美元,2023年进一步增长到3.55亿美元,具备了成为重磅药物的潜力。
在Inclisiran的销售额快速增长的同时,其也将小核酸的应用领域成功从罕见病拓展到了慢性病领域,这为小核酸药物应用于更广泛的适应症打开了想象空间。而Inclisiran的靶点与信达的IBI-306一样,都是靶向PCSK9。Inclisiran的成功自然也引起了信达的关注。
为了快速切入小核酸领域,2023年12月27日,信达开始与圣因生物合作,共同开发治疗高血压的小核酸候选药物SGB-3908。信达的技术路线也开始不断扩展,从早期的单抗、双抗到ADC、融合蛋白,然后又切入了小核酸。可以看到,信达的产品布局密切跟随着前沿技术的发展路径。
信达牵手圣因生物之后,2024年初,小核酸领域又发生了两笔大的并购。2024年1月3日,瑞博生物与勃林格殷格翰达成总交易金额超20亿美元的合作,双方共同开发肝病治疗领域的小核酸创新疗法。2024年1月7日,舶望制药与诺华达成协议,涉及多款心血管疾病药物,诺华将支付1.85亿美元首付款,以及潜在总金额达41.65亿美元的后续费用。
短短十天之内,创新药企在小核酸领域的合作就被频频爆出,足以看出小核酸行业的热度之高。
与圣因生物合作之后,这款siRNA药物IBI3016(圣因生物研发代号:SGB-3908)进展也比较顺利。今年11月10日,IBI3016的首次人体(FIH)临床Ⅰ期研究的主要结果在2025年美国心脏协会(AHA)科学会议数字化壁报专场展示。北京大学第三医院王方芳主任作为演讲者现场口头汇报研究结果。
临床研究结果显示,IBI3016单次给药能持久强效降低AGT水平,最大降幅超95%,且在6个月内降幅稳定,在3个月时各剂量组均实现血压下降。在安全性方面,IBI3016在6个月内表现出良好的安全性和耐受性,未观察到重度不良事件(AE)或严重不良事件(SAE),无低血压事件发生。所有不良事件均为轻度至中度且可逆。IBI3016的临床Ⅰ期数据支持后续的产品开发。
在推进IBI3016的过程中,信达的小核酸开发经验也日渐丰富,其自研产品也开始浮出水面。
2025年10月30日,信达生物公开了siRNA专利WO2025223537A1,专利涉及到INHBE靶点的小核酸药物研发进展。
抑制素亚基βE(INHBE)是转化生长因子-β(TGF-β)家族的成员。INHBE主要在肝脏中表达,是一种肝脏因子,已被证明与人类的胰岛素抵抗和体重指数呈正相关。定量实时PCR分析也显示,胰岛素抵抗人体肝脏样本中的INHBE基因表达增加。
目前围绕着INHBE靶点,国内外有诸多企业参与:国外的小核酸企业Arrowhead和Wave Life临床进展居前;国内的企业中,圣因生物、大睿生物、默化生物、靖因药业、先衍生物等都有参与其中。据医药魔方统计,截至2025年12月4日,全球靶向INHBE的小核酸产品共有19款正处于临床Ⅰ/Ⅱ期及临床前阶段。

靶向INHBE的在研小核酸产品(资料来源:医药魔方)
从全球范围来看,临床进展领先的是Arrowhead的ARO-INHBE,这款产品于2024年11月开始全球的Ⅰ/Ⅱ期临床研究。此前针对ARO-INHBE的临床前研究取得了较好的结果:1)在食蟹猴模型中,ARO-INHBE在D1和D29以3mpk的皮下注射实现了INHBE转录物的深度敲低,持续时间至少为85天。2)在DIO和db/db小鼠中,每周服用ARO-INHBE替代物可显著抑制体重增加并减少脂肪量,维持体重和葡萄糖稳态。ARO-INHBE的潜在效果表明其有望与GLP-1类减脂药联合使用,在降低GLP-1类药物使用量的同时实现减脂不减肌的效果。
在国内市场,临床进展居前的是圣因生物的SGB-7342。临床前数据表明,这款产品具有较好的降脂潜力。
信达在INHBE靶点的在研产品设计思路与Alnylam专利WO2023003922中的AD-1708473.1比较接近。信达的产品采用了GalNac-L96递送技术,靶向肝脏组织。这一递送体系通过长链状结构一端与GalNac(N-乙酰半乳糖胺)相连,另一端连接寡核苷酸片段。
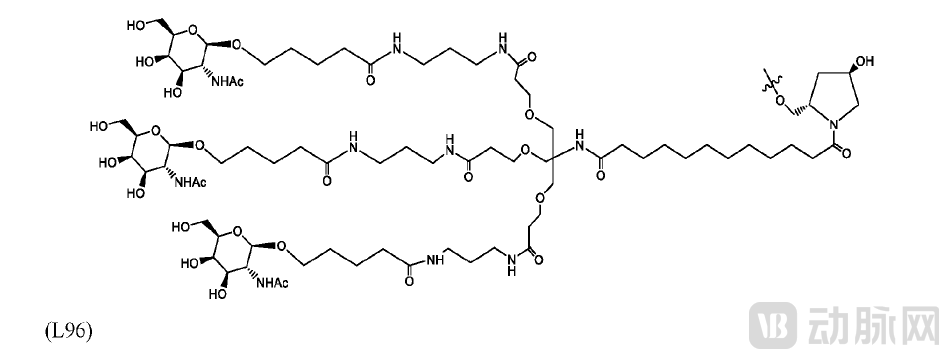
GalNac-L96递送体系(资料来源:信达生物专利)
早期数据显示,信达的这款产品在体重和脂肪量下降方面要好于Alnylam的同类产品。
但是不能忽视的是,目前围绕INHBE靶点的小核酸药物开发,竞争十分激烈,而信达又处于进展相对落后的位置,后续的开发压力比较大。
虽然信达是从单抗/双抗、ADC这些领域切入到小核酸领域里来的,起步比其他专做小核酸的企业晚了一些,但一款产品成功与否还要依赖临床推进的速度和后续的商业化能力。在临床推进和商业化方面,信达的优势无疑十分明显。
在竞争激烈的PD-1领域,信达靠着适应症的不断拓展和商业化推进,把信迪利单抗这款产品的销售额持续做起来了。2024年,信迪利单抗的销售额已经达到了38亿元左右,剑指50亿的门槛。信达3000人左右的销售团队,覆盖全国320多个城市、约5100家医院的商业化网络成了实现这一成果的重要支撑。
由此可见,虽然INHBE靶点的小核酸产品竞争十分激烈,但信达仍有反超的能力。
在国内市场,目前还没有本土企业自主研发的小核酸药物上市。国内本土企业在研的小核酸管线进入临床Ⅱ期的产品仍以肝病适应症为主,并逐步向心血管领域拓展。从头部创新药企来看,恒瑞的HRS-5635以及正大天晴的TQA3038也都是用于治疗慢性乙肝的siRNA产品。由此可见,国内小核酸领域的研发同样处于适应症扩展的阶段,即临床进度居前的产品以肝病适应症为主,而心血管、代谢疾病领域的产品多处于早期研究阶段。小核酸药物在更广阔适应症的应用还处于发展初期。
从研发的角度来看,我们认为信达后续仍有可能持续推出小核酸管线,目前只是走出自研的第一步而已。
小核酸行业当前进入了爆发初期,递送技术的突破和适应症的拓展为小核酸行业提供了极大的发展空间。用佑嘉生物总经理王猛的话来说,当前小核酸领域的发展阶段如同“汽车驶上了高速入口,刚刚进入提速阶段”。面对这样一个新兴的技术领域,信达后续持续推进在这一领域的开发是大概率事件。
梳理一下信达在小核酸领域的布局过程,我们可以看到信达谨慎、务实、步步为营的推进逻辑:先与圣因生物合作,试水一款产品;然后在作用机制比较明确的INHBE靶点上采用成熟的GalNac递送平台开发自研产品。随着这两个环节都取得了阶段性进展,信达后续有可能尝试开发新的靶点或者新的递送技术,持续拓展产品的应用领域。
对于新药研发来说,选定研发方向只是起步,能不能开发出产品以及后续以多快的速度推进临床和商业化考验的是团队的执行能力。而信达在短短半个月之内就先后在小核酸领域取得两大突破性进展,这无疑向外界表明信达要在小核酸这一新兴领域大力布局了。





























