1月9日,宜联生物宣布与罗氏就YL201项目达成一项新的独家许可协议,将联合推进该款靶向B7H3的候选创新抗体偶联药物(ADC)在多种实体瘤适应症中的开发和商业化。
根据协议条款,宜联生物将授予罗氏在全球范围内(不包括中国大陆、香港特别行政区和澳门特别行政区)独家开发、生产和商业化YL201项目的权利。宜联生物将获得5.7亿美元(约合人民币39.79亿元)首付款及近期里程碑付款,并有权获得额外的开发,注册和商业化里程碑付款,以及YL201在海外获批上市后基于净销售额的分级特许权使用费。
交易管线已进入Ⅲ期临床试验
YL201项目是依托宜联生物自主开发的肿瘤微环境可裂解的喜树碱类毒素连接子平台(TMALIN)开发的一款靶向B7H3的抗体偶联药物。
据悉,传统ADC药物仍有许多缺点。首先,在ADC发挥疗效的过程中,抗体需要被细胞内吞,因此ADC药物的抗体选择受限。此外,ADC的有效载荷释放需要经历多个环节,如肿瘤细胞内吞和溶酶体溶解,其中每个环节都可能导致治疗无效或耐药。然后,当ADC分子量较大时,肿瘤富集速度慢,通透性低,靶抗原表达低,很难发挥良好的治疗效果。
宜联的TMALIN技术平台可以解决现有ADC技术的缺陷。其一,该平台具有独特的酶切特性,具有在肿瘤微环境中胞外裂解的能力,无论抗体是否可被内吞,ADC都仍具有较高的抗肿瘤活性,大大拓宽了抗体的选择范围;其二,特殊的毒素-连接子设计使ADC能够在肿瘤微环境中富集,增加肿瘤中有效载荷的比例和血药浓度,并具有较高的治疗指数;其三,该平台的酶切特性和肿瘤富集特性,使有效载荷在肿瘤组织中大大富集,产生较强的旁观者效应,在抗原表达低甚至无抗原表达的肿瘤中产生良好的抗肿瘤作用。
此外,TMALIN技术形成的ADC还具有诸多优点:具有极高的全身循环稳定性,可减少有效载荷在非靶组织中的脱落所引起的“脱靶”毒性;具有优异的溶解性和化学稳定性,不存在传统ADC中马来酰亚胺连接方式引起的可逆Michael加成反应,可得到高均一性的、定点定量的ADC偶联(DAR=8);偶联效率高(≥90%)。
YL201的顺利推进是TMALIN技术平台的最好验证。目前,YL201项目正在全球范围内开展针对多种晚期实体瘤的临床研究。在中国,YL201已进入用于小细胞肺癌和鼻咽癌适应症的两项Ⅲ期注册性临床试验阶段。在二线小细胞肺癌患者中的早期临床数据已展现出优异的客观缓解率和生存获益。2025年6月,美国FDA授予YL201一项突破性疗法认证,用于治疗小细胞肺癌,此前, YL201已获得美国FDA授予的三项孤儿药资格认证,包括小细胞肺癌、鼻咽癌及食管鳞状细胞癌。
70%管线已达成BD
事实上,这不是宜联生物第一次与罗氏达成合作。早在2024年1月,双方就宣布将合作开发靶向间质表皮转化因子(c-MET)的下一代ADC候选产品YL211,用于治疗实体瘤,合作总额超10亿美元。根据协议条款,罗氏将获得宜联生物YL211项目在全球范围内的开发、制造和商业化的独家权益。宜联生物将与罗氏中国创新中心(CICoR)共同合作推动YL211项目进入临床I期试验阶段,并交由罗氏负责后续全球范围内进一步开发和商业化工作。
与大多一次性、偶然性的BD不同,这种“回购式”BD超越了单次交易,表明罗氏对ADC赛道以及宜联生物的整体研发能力、技术平台生产力及团队执行力的高度认可。除了罗氏的“回购”之外,宜联生物官网显示,其在研10条管线中,有7条都达成了交易。
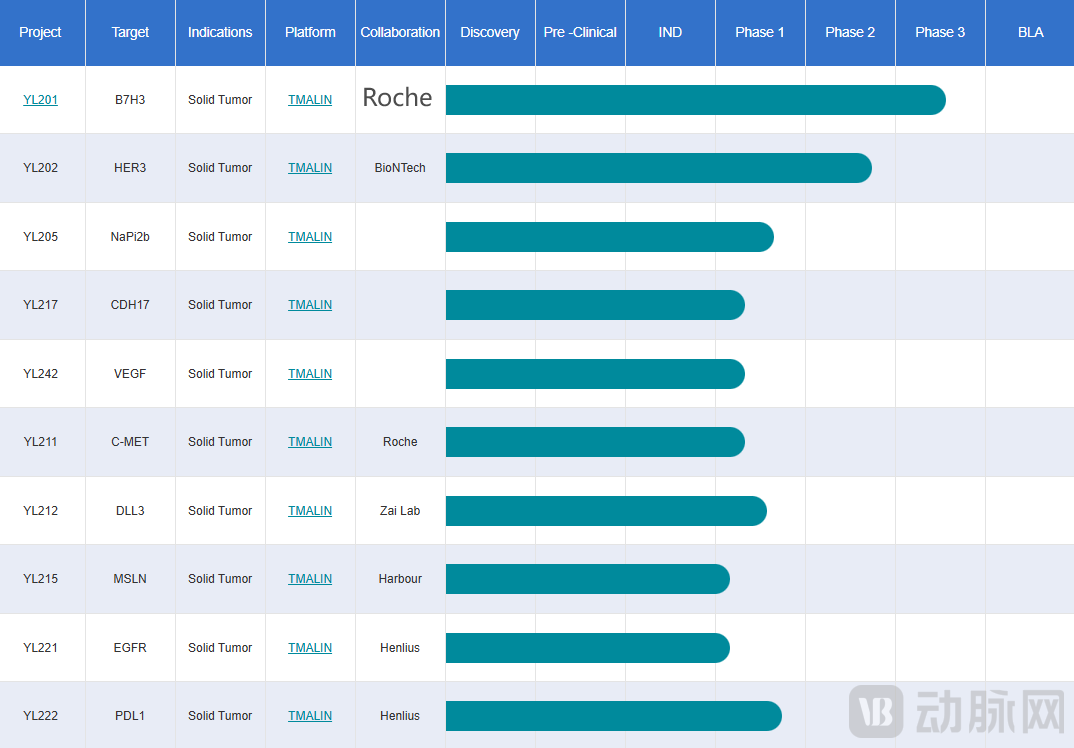 宜联生物在研管线
宜联生物在研管线
宜联生物能够不断获得同行的认可,有多重原因。
从宜联生物本身来看,其TMALIN技术平台在开发ADC领域的优势前文已述。此外,基于技术平台,宜联生物选择了不一样的ADC打法,在布局管线时更多选择的是B7H3、HER3、DLL3这类新兴靶点,而不是在HER2等热门靶点领域中去挖掘ADC的存量价值。
从全球ADC发展来看,这一细分赛道还存在大量的蓝海市场。首先,现有ADC药物的治疗窗口还比较窄,远远没有达到人们所期望的“魔术弹头”应该有的安全性,所以有很大的提高空间。另一方面,ADC各个方面都可以改进和提高,包括抗体的特异性结合、毒素作用机理多样性、linker的特异性裂解释放等。另外,ADC在非肿瘤疾病中的应用也是一个待挖掘的新方向。
等待挖掘的蓝海市场,加上此前已经在部分疾病领域被验证的临床疗效和不断拓宽的治疗范围,让ADC的商业想象空间呈指数级增长,其市场潜力也得到了行业的重新评估。在这一赛道中,以中国为代表的创新力量正在崛起。Beacon Reports显示,截至2025年11月28日,中国已成为ADC创新热土——占全球ADC资产28%。重要的是,中国已成为ADC临床试验实际上的“第一”:2023年以来,全球超50%临床试验、75%Ⅲ期联合试验落地中国。十年间国内ADC市场潜在交易值增至240亿美元,年增长18%。
不难看出,中国ADC已从“单靶点、单分子”的跟随式创新,跃升为具备“平台级输出”能力的全球BD高地。此外,宜联生物不断获得认可,也揭示出当前ADC赛道的价值评估范式:一家Biotech的发展巅峰不是单产品的销售峰值,而是取决于谁能把技术做成可持续产出与溢价的平台。近年来,宜联生物从B7-H3、c-MET到HER3等多靶点分子的连续成功对外授权,再到最终其技术平台本身获得巨额交易,正是其从单个项目的价值兑现,迈入到平台化能力获得全球顶级伙伴认可的事实体现。





























