当创新药不断沿着小分子、抗体到核酸与细胞治疗等路径演进,主流技术体系始终建立在“天然分子”的延展之上。而在这一成熟框架之外,一类基于化学合成、具备高度结构可控性的分子形态,正逐渐进入研究与转化视野——人工合成高分子药物。
与依赖生物体系表达的抗体或核酸药物不同,高分子药物的核心特征在于“可设计性”。它的分子骨架、功能单元、体内分布、半衰期乃至作用模式,都能通过聚合化学精准调控,让新药研发真正从“在天然分子中筛选”,迈向按临床需求主动设计功能分子的全新阶段。
也正是在这一判断之下,2025年底在深圳成立的珞方生物,将高分子药物作为核心切入方向,并希望通过平台化能力,推动这一技术路径从科研探索走向临床转化。
当传统技术赛道日趋拥挤、同质化竞争加剧,珞方生物的选择,也抛出了一个关乎行业未来的核心命题:人工合成高分子药物,是否有可能成为下一代重要的药物形态之一?
从全球探索到国内空白,高分子创新药迈入早期窗口期
如果说前文揭示的是一种新型分子形态的潜力,那么更关键的问题在于:在当前创新药迭代的节点上,高分子药物为何开始受到关注。
从现有药物体系来看,各类技术路径在不断成熟的同时,也逐步显现边界——小分子药物具备口服与生产优势,但在作用机制与靶点拓展上存在天然限制;抗体药物靶向性强,却面临结构复杂、成本高及体内分布调控困难等问题;核酸药物虽具潜力,但递送效率、稳定性与免疫原性仍待突破。
在既有路径逐渐逼近能力上限的背景下,行业开始寻找能够补位的新分子形态。高分子药物的意义,不仅在于提供新的药物来源,更在于引入从结构出发的开发逻辑——通过聚合化学(Polymer Chemistry)进行分子构建,使结构与功能可以按需设计,从而在药代动力学与作用机制层面实现更高可控性。这一特性,使其在慢病等需要长期给药与稳定控效的场景中具备独特潜力。
从全球来看,高分子药物并非全新方向。自上世纪80年代进入临床探索以来,FDA已批准司维拉姆(Sevelamer)、考来维仑(Colesevelam)等产品上市,并在肾病、高血脂等慢病领域实现商业化。与此同时,基础研究持续升温。PubMed数据显示,以“polymer therapeutics”为关键词的研究文献近年来持续增长、整体稳步上升。
但整体来看,该领域仍处于“学术活跃、转化有限、产业体系尚未成型”的阶段。这也意味着,高分子药物正处在一个关键窗口期——技术路径已被验证具备可行性,但系统化开发能力仍有待建立。
值得注意的是,国内在这一方向几乎处于起步阶段。当前创新药资源主要集中于小分子、抗体与核酸赛道,而围绕高分子药物的分子设计、合成、表征到成药性评价与临床开发的完整体系,尚未真正建立。
“这不是单一技术的缺口,而是整个开发链条尚未成型。”罗智指出。
在这一阶段,珞方生物率先搭建面向产业化的技术体系,尝试将高分子药物从分散的科研探索,推进至系统化研发与工程化开发。
锚定平台型Biotech定位,以体系化能力切入高分子赛道
对于珞方生物而言,切入高分子药物并非偶然,而是基于长期科研积累形成的产业判断。
团队在高分子科学与药物递送领域的研究中逐步意识到,高分子在医药领域长期被局限于辅料或载体,其作为“药物API”的潜力尚未被系统开发。基于这一认知,公司在成立之初即明确定位为专注高分子创新药的平台型Biotech。
这一定位也决定了其发展路径:不以单一项目为起点,而是优先构建底层技术体系。高分子药物研发具有显著的体系依赖性,从分子设计、可控合成、结构表征到成药性评价与体内研究,各环节高度耦合,难以通过单点突破实现持续产出。只有建立完整的研发框架,才能稳定推进候选分子向转化端演进。
围绕这一目标,公司搭建了多学科交叉团队,覆盖高分子科学、药物化学、生物医学工程及临床开发等方向,形成从基础研究到临床转化的连续能力。其中,研发团队中博士占比超过70%,主要来自清华大学、瑞士洛桑联邦理工学院、华中科技大学等国内外顶尖院校。
创始人罗智的经历体现了这一技术路径的延续性:其本科毕业于清华大学高分子材料专业,后在瑞士EPFL及ETH药学院完成博士及博士后研究,长期从事创新药与递送系统开发,兼具分子设计与成药转化经验。此前参与创立的多肽药物递送公司OBaris AG已于2025年被强生收购,证明其具备从科研走向产业化的实践基础。
在这一团队结构与路径选择下,珞方生物并未从单一产品切入,而是围绕“持续产出分子”的目标搭建平台,并在此基础上推进管线开发,为后续研发与产业化奠定基础。
国家重点研发计划驱动,多学科融合构建研发闭环
在明确平台路径后,珞方生物开始将高分子这一跨学科方向,转化为可持续产出候选药物的研发体系。
这一体系源于国家级科研项目的技术积累。2022年,罗智牵头承担国家重点研发计划“高端功能与智能材料”专项研究。在此基础上,团队将科研阶段形成的关键能力持续工程化,逐步搭建起覆盖“设计—合成—筛选—转化”的研发闭环。
这一闭环的核心,在于围绕关键问题形成协同运转:在设计端,通过计算模型与结构分析构建候选分子,并基于数据预测其性质,从源头提升有效性;在合成端,依托聚合化学实现结构可控的分子制备;在筛选与验证环节,结合体外模型与器官芯片(Organ-on-a-chip),在更接近真实生理环境的条件下评估功能与安全性,并推进至临床前研究。
高分子资源的积累进一步提升了体系效率。公司已自主构建包含超过2000个候选分子的高分子药物库,使研发不再依赖线性“设计—合成”路径,而是可以基于既有分子进行筛选与优化,从而缩短早期发现周期。同时,持续沉淀的数据也为算法模型提供训练基础,形成“数据—模型—设计”的迭代关系。
在此之上,多学科能力被进一步整合为统一体系:聚合化学、AI建模、大科学装置与器官芯片围绕具体研发问题协同运转。其中,通过引入同步辐射与中子散射等手段,团队得以在更接近真实环境的条件下解析高分子结构,弥补传统表征手段的局限,从而提升对结构与药效关系的理解。
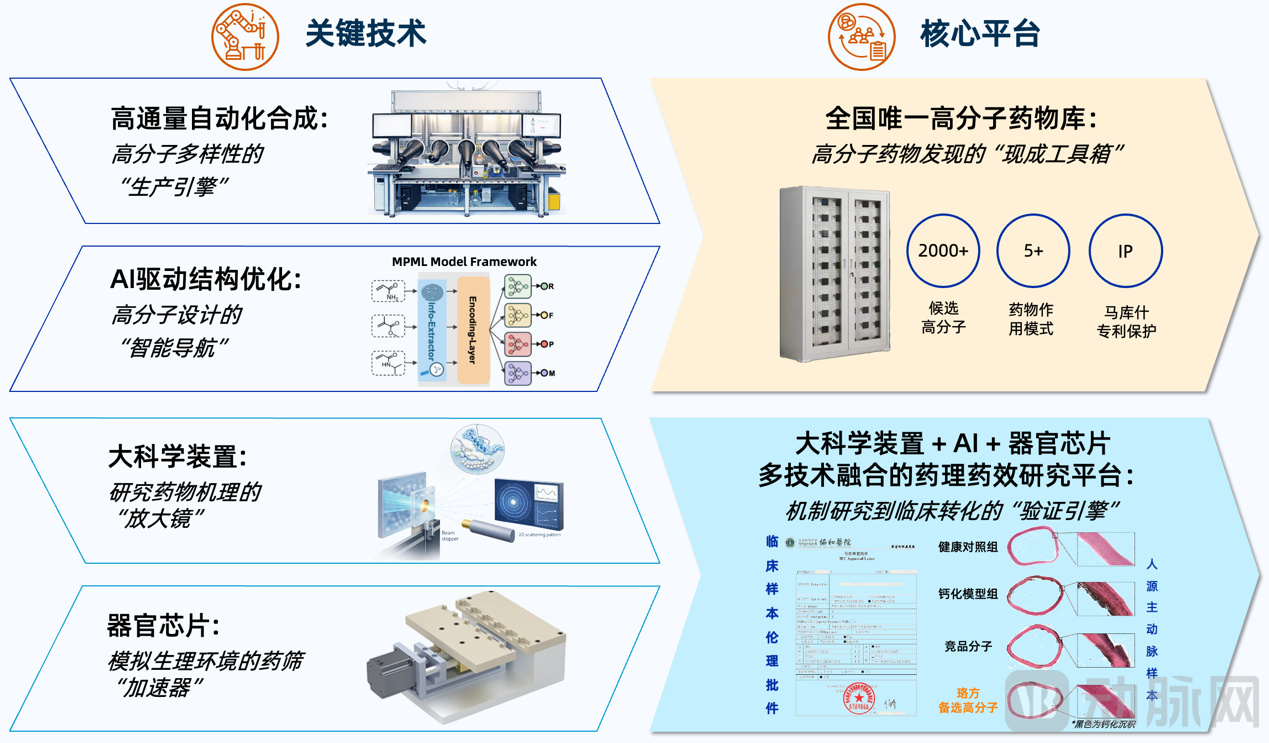
珞方生物核心技术平台
在这一体系支撑下,珞方生物具备了持续产出候选分子的能力,使高分子药物研发从单点探索走向可重复的系统化运转。
锁定慢性病长期管理,以高分子药理机制优势构筑管线矩阵
平台能力的价值,最终需要通过高潜力的管线生态来体现。
在适应症选择上,珞方生物系统性地聚焦于存在巨大未满足需求的慢性疾病及复杂疾病领域。这类疾病的核心治疗需求是长期、安全、稳定、便捷,对药物的安全性、耐受性、给药频次提出极高要求。而高分子药物的体内行为可通过结构设计精准调控,能够延长半衰期、降低给药频率;更重要的是,由于其大分子特性,多数高分子不进入细胞,系统性毒性更低,恰好适配慢病长期管理的临床场景。
依托高分子药物的这一药理优势,珞方紧扣慢性疾病“稳态失衡”这一共性特征,在心血管、过敏、代谢及自免等方向实现了管线系统性布局。所有管线均由公司自主构建的高通量及表征平台驱动,形成高效协同、可快速复制的First-in-class慢病创新药管线矩阵。
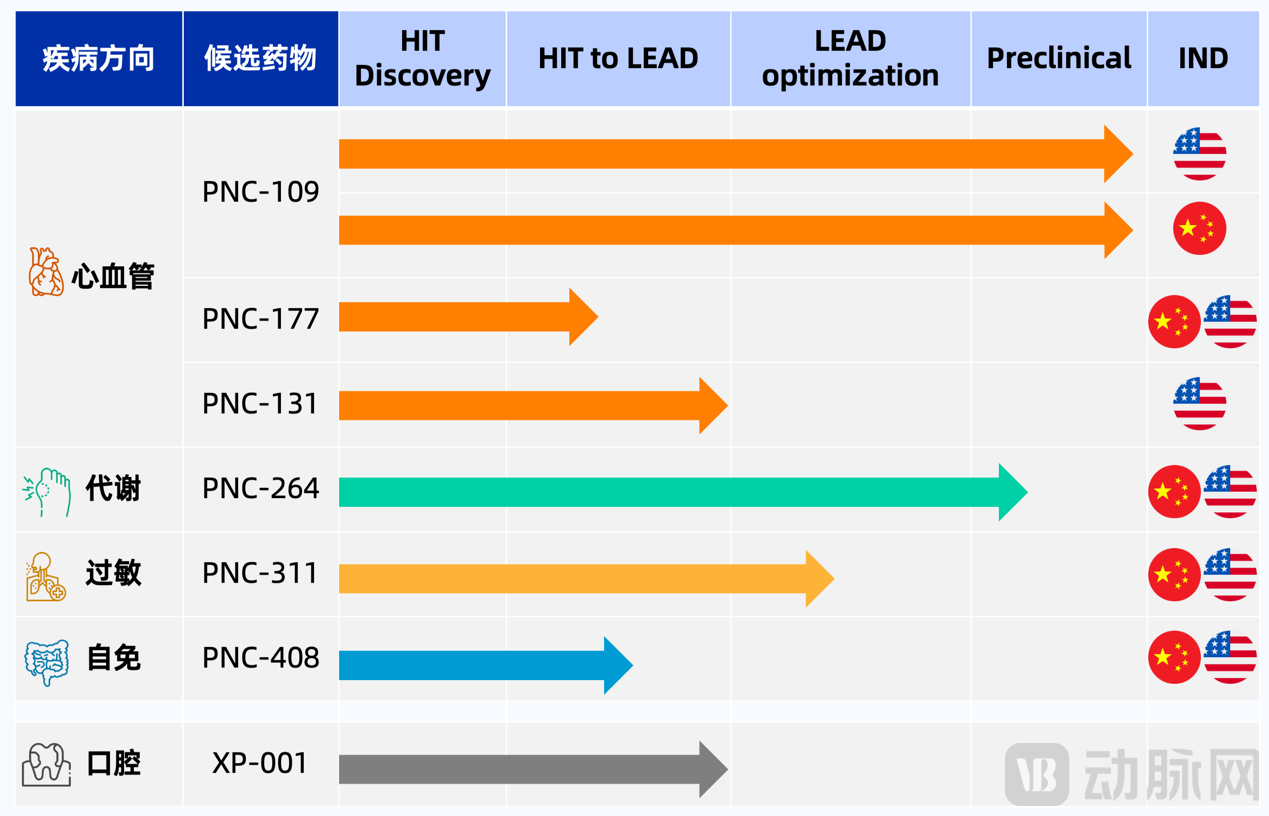
珞方生物慢病管线布局
以原创资产为核心,迈向临床验证关键阶段
从底层技术到管线布局,珞方生物的核心始终围绕平台能力展开。随着技术体系日趋成熟,公司也明确了自身的价值实现路径:围绕临床实际未满足需求,用关键临床数据验证技术价值。
未来3—5年,将成为珞方生物的重要跃迁期。一方面,平台仍将持续迭代,提升分子设计与筛选效率;另一方面,首发管线进入临床后,有望逐步释放验证信号,使技术路径迈向“可验证”。
放在更宏观的坐标系中,高分子药物正处于持续拓展的发展阶段,其产业边界也在不断被探索与定义。在创新药由“靶点驱动”逐步向“分子形态驱动”延展的过程中,这一路径的潜在价值,有望随着临床与商业化进展的推进而逐步显现。
在这一过程中,企业所扮演的角色,不再仅是产品开发者,更是技术路径的探索者与推动者。“我们并不是只做一个产品,而是希望验证一种新的分子形态是否能够持续产生临床价值。”罗智表示。
从国家级科研项目起步,到企业化平台的搭建,再到具体管线的推进,珞方生物所实践的,是将一条前沿技术路线逐步推向可验证、可转化的产业路径。对于仍处发展阶段的高分子药物赛道而言,这类围绕平台能力展开的系统性探索,正在成为推动行业演进的重要力量。
也正是在这一进程中,开篇提出的问题开始获得现实层面的回应:人工合成高分子药物,是否有可能成为下一代重要的药物形态之一?答案或许尚未完全揭晓,但真正的创新,往往始于边缘,最终汇入主流。珞方生物正手握着开启高分子药物大门的钥匙,为全球庞大的慢病患者群体,带来新的期待。




























