
在初春的天津,一场关于血友病A的基因治疗药物的临床研究者会议正在举行。这场会议定下了一年之约,用来观察一款中国本土原创的,由临床专家与科研团队共同推动,有望成为领域类Best in class的基因治疗药物的未来命运。

中国医学科学院血液病医院(血液学研究所)教授张磊是这场会议的核心人物。他向在场的十余家参研单位宣布:由他牵头进行临床研究的血友病A基因治疗药物GS1191-0445注射液,其三期临床试验的57例受试者已全部入组,正式进入为期52周的关键随访期。
这意味着,这款由中国临床专家与科研团队自主研发、协同推进的基因治疗产品,距离完成最终的疗效验证又近了一步。而这场会议的目标,就是希望在未来一年,为产品的上市申请积累扎实可靠的数据。
就在一个月前,大洋彼岸传来一则震动行业的消息:全球首款获批上市的血友病A基因疗法Roctavian,其研发公司拜马林制药(BioMarin)宣布,将该产品从全球市场撤出。
诚然这款药物存在疗效不够持久的弊端,但其撤市的根本原因或许不能排除昂贵支付的因素——单次治疗定价高达290万美元,全球各国医疗支付体系均无力承载。在销售不佳的情况下,拜马林制药试图剥离管线寻找买家,但却始终无人愿意接盘,最终导致这款增被寄予厚望的产品不得不黯然退场。
同样的科学梦想,一个在东方加速推进,一个在西方无奈退场。这不仅是两家公司的不同命运,更折射出全球基因治疗领域一个日益尖锐的核心矛盾:当一次性的“治愈性”疗法成为可能,谁来为它买单?
GS1191-0445提供的答案,或许就藏在它的一项核心临床数据里:在早期研究中,它实现同等甚至更优疗效所需的临床给药剂量,仅为国际同类产品的约1/20。
更低的剂量,远不止是一个科学指标。它意味着更高的安全性、更低的成本,以及从根本上被重塑的“定价-支付-可及性”等式。当西方同行在“天价”与“市场”之间进退维谷时,中国药企希望能探索出“有效”和“可及”之间的新的平衡。
天价疗法的“困境”
Roctavian的退市,在行业里并不是一个完全意外的消息。
细胞与基因治疗(CGT),尤其是以腺相关病毒(AAV)为载体的体内基因治疗,曾被寄予攻克众多单基因遗传病的厚望。通过一次治疗,使患者体内的缺陷细胞尽可能恢复正常功能,从而从根源上纠正缺陷,实现长期乃至终身的治疗效果。
然而,科学与商业现实之间横亘着一道巨大的鸿沟:成本与价格。
细胞与基因疗法的研发过程漫长且复杂,涉及病毒载体设计、生产工艺开发、临床验证等多个环节的高投入。更关键的是,与传统药物不同,基因疗法理论上是一次性治疗,这意味着企业的收入窗口期极短,无法通过长期销售来分摊研发成本和获取持续利润。
这种商业模式倒逼出了一个定价逻辑:将天文数字般的研发、生产和商业化的成本,分摊到每一位患者身上,并在此基础上追求投资回报。
于是,我们看到全球已上市的基因疗法定价屡创新高:诺华治疗脊髓性肌萎缩症的Zolgensma定价212.5万美元,蓝鸟生物治疗β地中海贫血的Zynteglo定价280万美元,而拜马林的Roctavian更是标出了290万美元的价格。
但现实情况是,罕见病患者群体本就有限,而数百万美元的价格,远超全球绝大多数国家医保体系和患者个人的承受极限。即便在医疗支付体系最为发达的欧美国家,保险公司和医保系统也对如此高昂的一次性支出望而却步,更由此衍生出了复杂的按疗效付费、分期付款等创新支付模式。即便如此,这类疗法的销售仍然持续不及预期。
Roctavian退市被业内视为一个标志性事件:它意味着,即便技术获得成功,如果无法跨越“支付”这道坎,产品依然无法实现其应有的社会价值,商业上也难以为继。
细胞与基因疗法,陷入了“技术成功,商业崩塌”的“困境”。
中国解法:从源头上“降本增效”
就在Roctavian退市消息引发行业反思之际,中国药企提供的另一种解题思路。
华毅乐健生物科技有限公司(下称“华毅乐健”)自主研发的GS1191-0445,瞄准的同样是血友病A。这是一种由于凝血因子VIII缺乏导致的遗传性出血性疾病。患者需要终身、频繁地输注外源性凝血因子来预防出血,经济负担沉重,生活质量低,关节损伤还会不断累积。
GS1191-0445的设计目标,是通过单次治疗,将编码凝血因子VIII的基因递送至患者肝脏细胞,让身体恢复自主生产凝血因子的能力,从而摆脱对外部输注的依赖。
然而,它的路径与国际同行有着显著差异,是临床医学、基础科研与产业化能力协同推进下形成的一条中国路径。而这种不同,来自于基础的科学设计。

“这项由国内团队自主研发的基因治疗药物,采用了优化的腺相关病毒(AAV)载体包埋DNA序列,在启动子、增强子优化设计下,以Roctavian二十分之一的剂量获得了更高的FVIII因子表达。”中华医学会血液学分会主任委员胡豫教授,在天津的这场研究者会议上这样介绍。
通俗地说,就像优化了送货的卡车和货箱里的安装说明书,让送货效率更高,说明书指令更清晰,最终用少得多的“货物”(病毒载体),就能在体内启动高效的生产线(表达凝血因子)。

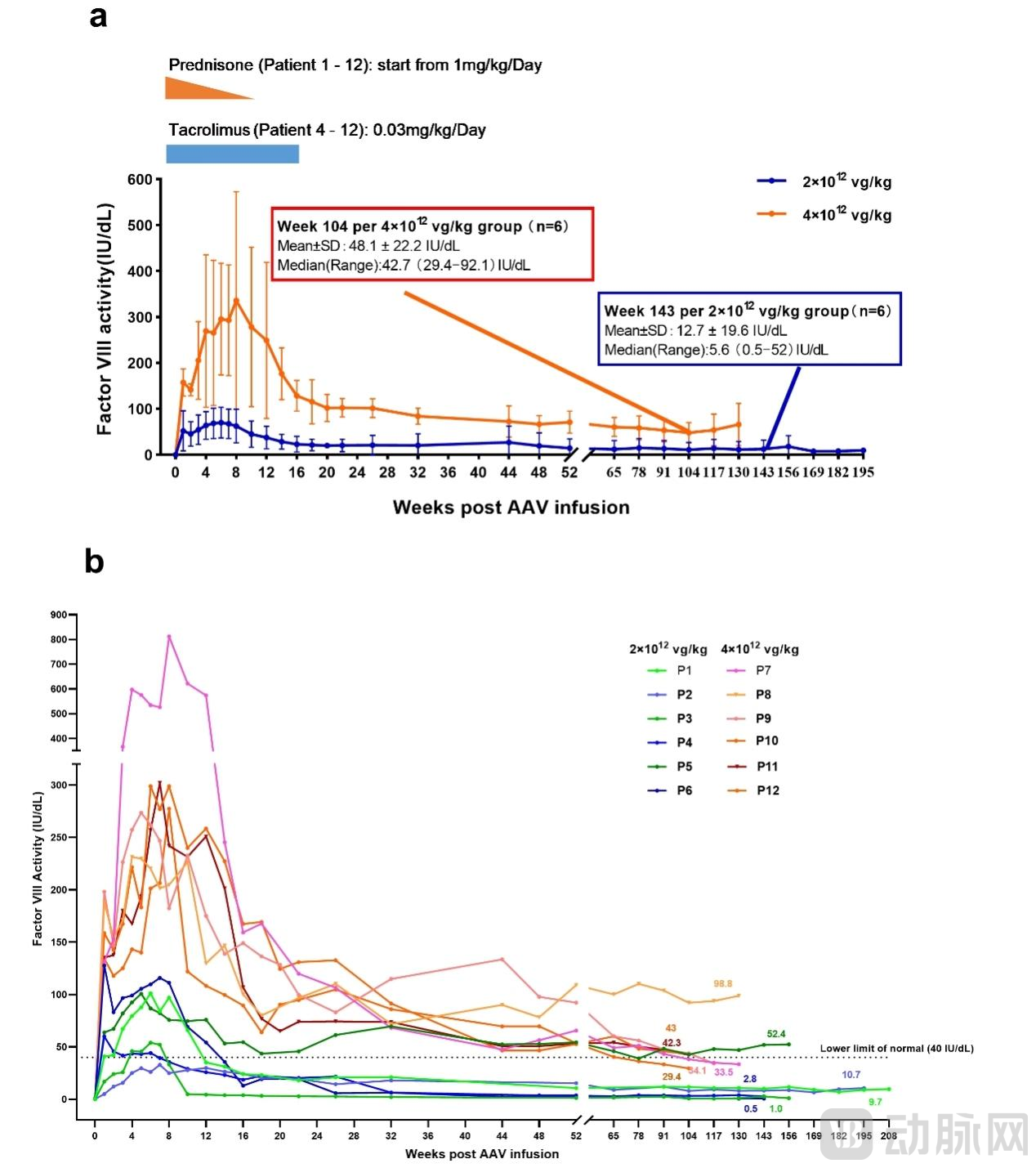
临床数据支撑了这一技术路径创新。根据2025年美国血液学会(ASH)年会公布及后续在《信号转导与靶向治疗》(STTT)期刊上发表的研究结果,在接受GS1191-0445治疗的中国成人重型血友病A患者中:
高剂量组(4×10¹² vg/kg)患者,在中位随访123.5周时,体内凝血因子VIII活性均值达到48.1 IU/dL(健康人约为50-150 IU/dL),成功脱离“血友病状态”;低剂量组(2E12 vg/kg)患者凝血因子活性长期维持在5%以上(达到临床“不出血”状态);患者的年化出血率最高降低99.4%,凝血因子替代治疗使用量大幅减少。
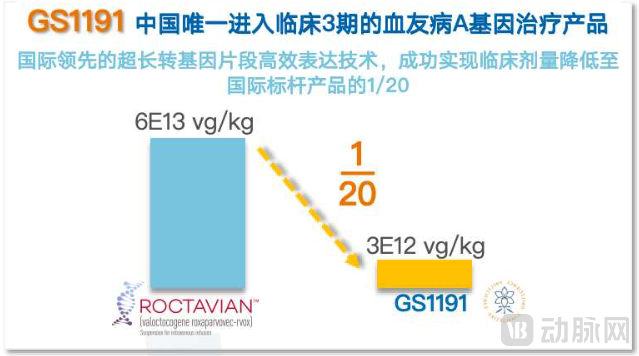
最重要的一点——在实现同等甚至更优疗效的前提下,GS1191-0445临床给药剂量仅为国际同类产品的约1/20。
这不仅是疗效的证明,更是成本结构的证明。在基因治疗中,病毒载体的生产是核心成本之一。剂量的大幅降低,则同样意味着生产规模、纯化难度和物料成本都有望被大幅压缩。
此外,华毅乐健团队还配套开发了预防性使用糖皮质激素和他克莫司的短期免疫调节方案。该方案旨在给药后的关键窗口期,温和地调节患者免疫系统,降低其对病毒载体的清除反应,从而保护刚刚建立的基因表达。这进一步增强了低剂量策略的可行性和持久性。
张磊教授对此解释:“这个创新方案已经获得世界其他国家专家的认可,并正运用于临床实践。”低剂量与免疫调节的结合,共同构成了GS1191-0445差异化的技术护城河。
从“患者可及”到“商业可持续”
技术上的“降本”,其实是要回答一个根本问题:药做出来了,病人怎么才能用上?
290万美元的定价,对于全球绝大多数血友病A患者及其家庭而言,无疑是个绝望的数字。它直接将这种疗法隔绝在现实世界之外。
而GS1191-0445所代表的“中国路径”,正在尝试改变这个局面。虽然该产品尚未定价,但基于其技术特点,业内普遍预期其价格将远低于国际同类产品。此前,国内另一家生物创新药企业针对血友病B的基因疗法,已将价格降至约279万元人民币,这被视作一个重要的市场信号。
“(成本只有国外1/20)这就为将来药物的可及性铺平了道路。”胡豫教授在天津的研究者会议上明确表示。
价格的实质性降低,意味着治疗的可能性从“绝对不可能”进入了“可以探讨”的范畴。对于中国患者而言,百万元级别的治疗费用虽然依然高昂,但已经有可能通过多层次保障体系进行分担:包括基本医疗保险、商业健康保险(如“惠民保”)、企业患者援助项目、以及分期支付等创新支付方式。
西方“天价疗法”模式陷入的悖论在于:高单价必然导致极低的市场渗透率,最终总市场规模受限,商业上难以持续。而“可负担的定价”策略,是想通过一个更合理的价格,去触及更大比例的患者群体,从而打开更真实、更大规模的市场。
血友病诚然是罕见病,但在中国巨大的人口基数面前,血友病患者群体的数量仍然不可小觑(A型患者估算约12.4-14.4万人),这为“以量换价”的模式提供了潜在基础。
一旦产品上市,更有可能被纳入地方普惠型商业保险的保障范围,或与支付方达成基于疗效的付费协议。销量与支付之间有望形成良性循环,避免重蹈国外同类产品“无人问津”的覆辙。
“我们追求的创新,不应该是‘孤芳自赏’的高价药,而应该是既能在技术上对标国际前沿,又能在研发成本和定价逻辑上贴合中国国情、符合医保体系承受能力的‘国民基因药’。”一位参与本次临床研究的研究者这样总结说。
商业的可持续性,不仅关乎一家企业的生存,更决定了前沿疗法能否真正落地,惠及本该受益的患者。
而未来的52周,将是最关键的一段时间,这些随访数据将最终验证GS1191-0445的长期疗效与安全性,也是这款“中国方案”能否最终走向患者、走向市场的临门一脚。
全球CGT格局中的中国力量
GS1191-0445取得的阶段性成果意味着,中国在细胞与基因治疗领域的参与度正在快速提升。
一个值得注意的现象是,在全球最昂贵的基因疗法竞争格局中,来自中国研发管线的候选药物比例已显著提升。这背后是中国在CGT领域逐渐形成的系统性优势:从上游的工艺开发(CMC)、到中游的合同研发生产(CDMO)能力、再到下游高效且成本可控的临床开发体系。
值得注意的是,GS1191-0445本身也获得了国际监管体系的初步认可。它先后获得了美国食品药品监督管理局(FDA)和沙特食品药品监督管理局(SFDA)的孤儿药资格认定(ODD),同时也被中国国家药品监督管理局药品审评中心(CDE)纳入为突破性治疗品种。
虽然孤儿药认定本身不意味着获批,但它代表了监管机构对其针对罕见病、以及初步临床数据的认可,为未来开展国际多中心临床试验乃至上市申请提供了便利。
“这体现了国际学术界和监管机构对中国原创科研质量的认可。”张磊教授评价说,“这不再是简单的‘国产替代’,而是真正的‘同台竞技’。”
中国基因疗法的崛起,其当前的核心价值可能不在于做出了“第一个”药,而在于正在证明,基因治疗可以不是普通人遥不可及的“天价神话”。中国的科学家正通过底层科学创新,在保证疗效的前提下,尽可能优化成本,让更多患者被纳入治疗范围。
这或许正在悄然改变全球基因治疗领域的游戏规则。一种疗法的终极价值,不应仅仅体现在科学论文的突破性上,或者药品标签的价格数字上,而更应体现在它能够实际拯救和改善的生命数量上。
全球基因治疗的竞赛,上半场比拼的是“能否做得出来”,下半场考验的则是“谁能用得起”。在跨越了科学可行性的门槛后,如何跨越商业可行性与社会可及性的鸿沟,成为所有参与者必须回答的问题。
GS1191-0445以及它所代表的中国创新路径,正在给出自己的答案。它指向了一个更朴素的终点:让突破性的科技,成为患者负担得起的希望。而这一进程的背后,不仅是技术的推进,更是一群长期坚守一线的临床医生,与科研与产业力量共同推动医疗进步的缩影。





























