2025年8月,临床阶段神经科学生物技术公司Gilgamesh Pharmaceuticals完成重大战略重组,宣布与艾伯维达成一项最终协议,将临床阶段候选药物布雷替西洛星(GM-2505),以最高12亿美元对价出售给艾伯维,包括预付款和开发里程碑付款。
此次交易也推动Gilgamesh完成分拆,既便于艾伯维聚焦核心资产开发,也为Gilgamesh进行早期管线创新提供了条件。
分拆后,原Gilgamesh的全部员工、剩余管线项目,以及与艾伯维公司的现有合作与选择权协议资产,均转入一家以“Gilgamesh Pharma Inc."(以下简称Gilgamesh)名义运营的新实体。该实体保留管线项目包括伊博格碱类似物GM-3009、口服NMDA受体(NMDAR)拮抗剂布里克瑟罗迪尔(GM-1020)、非致幻性神经可塑性候选药物、M1/M4受体激动剂项目。
2026年3月24日,新实体Gilgamesh宣布完成6000万美元A轮融资,这是该公司的首次正式融资,由Prime Movers Lab与Satori Neuro共同参与投资,资金及收益将用于推进核心管线的临床及临床前试验进程,同时继续推进新型神经精神疗法组合的研发与推进。
寻找答案的蜕变故事,源自精神疾病赛道连续创业者的多年沉淀
2019年,Gilgamesh的首席执行官Jonathan Sporn博士与首席科学官Andrew Kruegel博士共同创立了Gilgamesh Pharmaceuticals。
Jonathan Sporn博士作为美国认证执业精神科医师,先后于塔夫茨大学、哈佛大学完成精神科专科培训,曾任波士顿当地医院精神科主任,以及哥伦比亚大学精神病学助理教授,拥有精神病学相关的学术背景;同时具备超25年的药物开发经验,曾任职于辉瑞、强生等大型药企,并创建Perception Neuroscience公司,该公司已被ATAI Life Sciences收购,成为全球致幻药物赛道首个成功退出的企业案例。
Andrew Kruegel博士则专注于中枢神经系统疾病的治疗领域,拥有10余年的致幻性化合物及伊博格碱类似物的合成研发与专利布局经验;他成功阐明抗抑郁药替安普汀的作用机制(MOA),致力于开发新型阿片类受体调节剂;此外,他曾创办Kures Therapeutics(后被ATAI Life Sciences收购),并担任该公司的创始人兼首席安全官。
公司名字来源于一个好莱坞电影剧本——关于美索不达米亚国王Gilgamesh的蜕变故事。这位国王起初是一位肆意妄为的统治者,随后陷入心理的困顿,踏上了寻找答案的旅程。
Jonathan Sporn说,Gilgamesh这个名字富有魅力,它既承载着古老的历史,又代表着崭新的发现。这则故事不仅呼应了Gilgamesh希望帮助精神疾病患者实现蜕变的初心,也与公司立足既定靶点、挖掘其治疗价值、开发新型化合物,以及从根本上重塑精神疾病治疗范式的核心目标相契合。
Gilgamesh组建了一支神经科学专家团队,成员均拥有在礼来、辉瑞等大型生物制药企业的数十年从业经验,其专业能力覆盖药物研发、临床研究、商业运营等关键环节,为公司发展提供技术与管理支持。
在药物开发层面,首席数据安全官Jorge Quiroz博士拥有20余年药物开发相关经验,曾任职于美国国立卫生研究院(NIH),以及罗氏、强生等国际知名药企,业务范围覆盖从早期临床开发到注册研究的全流程,主要聚焦于小分子药物和基因治疗领域。首席医疗官Gerard Marek博士则具备超25年早期临床开发与药物发现经验,曾任辉瑞副主任、礼来公司精神疾病药物发现部门的生物学首席科学官等重要职务。
运营及商业管理方面,首席品牌官兼研究主管Laszlo Kiss博士曾任职于默克、百时美施贵宝,具备逾20年的药物发现与开发经验,同时在辉瑞、百基担任企业风险投资与业务发展的领导岗位;首席运营官Yoni Falkson则拥有15余年商业开发、支付方策略、市场营销及产品发布相关经验,曾在辉瑞和再生元(Regeneron)担任商业领导职务。
AI+神经回路转化,以结构优化革新传统精神疾病药物
当前主流精神疾病药物治疗仍存在诸多共性局限,尤其以抗抑郁药为代表,普遍存在起效慢、患者应答率低下的问题,且易伴随锥体外系反应、代谢异常等不良反应。同时,部分具有新机制的化合物虽展现出差异化治疗潜力,却往往受限于心血管毒性强、口服利用度低等成药性缺陷,难以广泛应用于临床。
针对上述精神疾病治疗行业痛点,Gilgamesh搭建药物发现和成像平台,采用神经回路转化的方法,进行候选新药的选择与优化,致力于持续产出改良型创新分子。该方法将AI与机器学习算法相结合,可系统监测已知及新型精神活性分子的多维生物活性,以提升临床转化效果,同时针对性地优化药物的安全性、有效性和给药剂量范围。
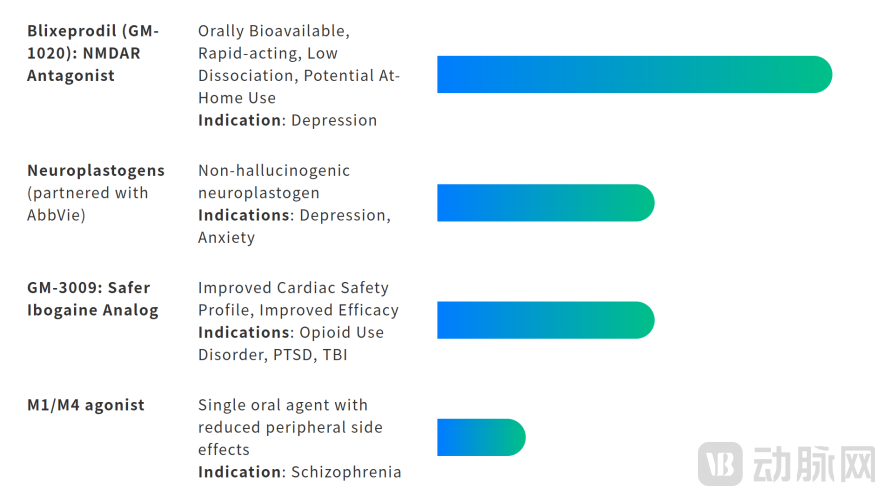
Gilgamesh Pharma管线及其所处阶段
(图源:Gilgamesh Pharma官网)
1GM-3009:更安全的伊博格碱模拟剂
《纽约时报》文章《强效迷幻物质作为阿片类药物成瘾疗法重新受到关注》指出,从临床试验和病例报告积累的数据来看,源自非洲灌木Tabernanthe iboga的天然提取物伊博格碱,对物质使用障碍(SUD)具有潜在抗成瘾活性,然而,其显著的心血管毒性风险长期限制了临床应用,已被包括美国在内的多国禁止使用。
2024年3月14日,Gilgamesh宣布已获得美国国家药物滥用研究所(NIDA)授予的一项多年期、总额1400万美元非稀释性资助,专项用于推进在研药物GM-3009的研发进程。该笔资金将重点支持GM-3009的IND支持性毒理学研究、GMP生产,以及在健康志愿者和阿片类药物使用障碍(OUD)患者中开展的Ⅰ/Ⅰb期临床试验。
作为一种新型伊博格碱类似物,GM-3009针对伊博格碱的骨架进行结构优化,体现了Gilgamesh在解决天然分子安全性问题的改造能力。临床前研究显示,GM-3009起效迅速、可显著降低心脏毒性风险,有望实现更优的抗成瘾疗效。该候选药物拟用于治疗SUD,尤其聚焦于OUD,同时也具备应用于创伤后应激障碍(PTSD)和创伤性脑损伤(TBI)的潜力。
2布里克瑟罗迪尔(GM-1020):NMDAR拮抗剂
尽管SSRI/SNRI类(单胺类神经递质再摄取抑制剂)经典抗抑郁药与NMDAR拮抗剂类麻醉药物为临床提供重要治疗选择,但前者起效较慢、患者应答率有限,后者则受限于口服生物利用度低、镇静与解离副作用显著等问题,临床仍存在大量未满足需求。
GM-1020是一种新型靶向NMDAR拮抗剂,区别于传统静脉麻醉类药物,通过结构优化实现口服给药,成为全球首批临床开发中的新型口服小分子NMDAR通道阻滞剂。
此前,针对GM-1020的Ⅰa期单次升剂量和多重升剂量试验证实,该候选药物在健康志愿者中安全性与耐受性良好,无剂量限制性毒性;而药效学结果显示,在目标剂量下受试者可产生完整可控的迷幻效应,为Ⅱa期重度抑郁症(MDD)临床研究奠定了剂量基础。
基于Ⅰa期 SAD/MAD试验与Ⅱa期临床试验顶线数据,GM-1020展现出起效快速、解离及镇静反应轻微的特点,且具备用户居家自行用药的可能性。因此,该新一代候选药物有望改变重度抑郁症(MDD)、双相情感障碍(BD)、强迫症(OCD)及其他严重精神障碍的治疗格局。
3非致幻性神经可塑性候选药物
2024年5月13日,艾伯维与Gilgamesh Pharmaceuticals宣布达成一项新合作协议,双方将结合艾伯维在精神病学领域的专业优势与Gilgamesh的创新研发平台,联合开发非致幻性神经可塑性候选药物,该项目目前处于IND准备阶段。
此前,经典致幻性化合物为精神障碍的治疗提供了全新的作用机制,部分已展现出良好的临床开发前景。然而,这类第一代化合物也存在明显短板,可能引发强烈的精神活性效应(例如幻觉),因此在门诊给药期间需辅以监护与支持性护理。
在此背景下,非致幻性神经可塑性候选药物致力于克服第一代化合物的成药性缺陷,在保留其抗抑郁等治疗特性的同时,显著减弱甚至消除其精神活性作用。Gilgamesh依托其创新研发平台,已成功筛选出该对应的先导化合物,这类化合物在治疗情绪障碍、焦虑障碍等多种精神疾病方面,具备显著临床获益潜力。
根据协议条款,艾伯维在行使选择权后,将主导后续开发和商业化活动。Gilgamesh将获得6500万美元的预付款,并有权获得最高19.5亿美元的期权费与里程碑付款,以及额外的销售分级特许权使用费。
精神疾病市场需求凸显,改良药物迎来发展机遇
在改良型精神疾病新药研发持续推进的同时,全球及中国的精神疾病治疗市场格局呈现出既存在未被满足的临床需求,也具有广泛潜在市场的双重特征。
《中国国民心理健康发展报告(2023~2024)》蓝皮书显示,我国成年人群心理健康状况在年龄、收入等维度差异突出。该报告抽取代表性成年人样本开展研究,结果显示成年人抑郁风险检出率为10.6%,焦虑风险检出率为15.8%。
现有研究表明,精神分裂症、双相情感障碍等精神疾病核心致病机制集中在四大方面:谷氨酸能系统功能低下、单胺类神经递质(如5-羟色胺、多巴胺等)失衡、神经炎症与免疫紊乱、突触可塑性及转录调控异常,具体包括非编码区遗传风险位点(与特定疾病相关的基因位点)介导的基因表达异常、转录本可变剪切紊乱等。
发表于《Molecular Psychiatry》的相关综述显示,在抑郁症治疗领域,我国28款在研药物中多款实现机制创新,例如DB104实现国内中枢神经系统疾病精准医疗零的突破,JJH-201501等多靶点药物进入Ⅲ期;精神分裂症治疗领域,全球首款First-In-Class(FIC)药物DB-103靶向mGluR2/3受体,为非多巴胺能(不依赖多巴胺通路,不作用于多巴胺受体)治疗的全新方向,再鼎医药引进的呫诺美林曲司氯铵(KarXT)作为近70年来全球首款全新机制抗精神病药,已在国内获批并纳入《我国精神分裂症防治指南(2025年版)》。
同时,国内双相情感障碍、焦虑障碍等适应症的创新药研发也在加速进行,绿叶制药若欣林已获批上市、中国中医科学院中药研究所研发的疏肝宁心颗粒与艾伯维ABBV-932等候选药物获批临床。整体来看,我国精神疾病药物管线已形成多适应症并行、创新与改良并重的格局。
放眼于全球,跨国药企在精神疾病创新药研发领域仍占据主导地位,多款新机制药物已步入后期临床阶段或获批上市。诸如NRx制药研发的口服复方制剂NRX-101,用于治疗严重双相抑郁,已完成以鲁拉西酮为活性对照的Ⅱb/Ⅲ期临床研究;由Sage Therapeutics与渤健携手研发的全球首款专门针对产后抑郁症(PPD)治疗的口服药物Zurzuvae,现已通过FDA批准上市。
与此同时,一批聚焦靶点优化、布局差异化的生物技术公司正在迅速成长,Gilgamesh便是其中的典型代表。其凭借自有的创新研发平台,推进改良型新药研发,在提升药物成药性的同时,优化治疗效果,实现双重价值的突破。





























