原发性肝细胞癌(简称肝癌)是全世界范围内常见的消化系统恶性肿瘤,根据GLOBOCAN 2020公布的数据,全球肝癌的年新发病例数约90.6万人,居于恶性肿瘤第6位,死亡83.0万人,居于恶性肿瘤第3位[1]。
肝癌在我国尤其高发,年新发病例和死亡病例均占全球50%以上[2]。尽管近年我国肝癌发病率和病死率呈下降趋势,但由于人口基数大、老龄化等因素,肝癌负担仍较为严重,对肝癌高危人群的筛查与监测,有助于肝癌的早期发现、早期诊断和早期治疗,是提高肝癌疗效的关键,有其必要性和紧迫性[3]。
目前肝切除术是肝癌患者获得长期生存的重要手段,但是文献报道的术后5年复发率>60%,成为进一步延长病人生存的主要影响因素[4]。如何准确预测和判断转移复发风险、予以及时精准干预,目前主要依赖临床病理特征(包括肿瘤大小、分期与分级、有无血管侵犯等),准确性较低,难以满足临床需求[5]。
因为相同临床分期的患者可能有着截然不同的预后,小癌也可早期转移复发。发展能够准确地预测和评估术后患者转移复发的产品,可以对复发转移风险较高的病人进行术后进一步的干预治疗,从而降低术后复发风险、延长生存期,而对复发风险低的病人避免不必要的术后干预(过度治疗)[5]。有效预防与及时合理治疗复发,对降低病死率,提高总体生存率具有重大意义[6]。
围绕着肝癌早筛早诊、术后转移复发监测领域的精准诊疗,阔然基因研发的IVD和LDT系列产品正在有条不紊地开发中。
围绕着探索新的肝癌筛查、诊疗策略,阔然基因与中山大学生命科学学院庄诗美教授合作研发的肝癌早筛和辅助诊断项目HCC7S“7种microRNA检测试剂盒(PCR荧光探针法)”,鉴定了一个由7个血清microRNAs组成的多分子预测模型,能够较甲胎蛋白(AFP)更早、更准确地预警肝癌的发生。
通过3个阶段(发现、训练、验证)、4个独立人群研究,建立了由7个血清microRNA组成的多分子预测模型,可以较好地区分肝癌与正常人、乙肝病毒携带者、慢性乙型肝炎以及肝硬化患者,其检测肝癌的准确性和敏感性远高于血清AFP和B超,尤其是检测小肝癌(肿瘤大小≤3 cm)和早期肝癌(BCLC 0期及A期)的优势更加明显。同时,对于AFP阴性(AFP ≤ 20 ng/mL)的肝癌也能实现较好地检测[7]。
血清miRNA稳定性好,检测便利且无创伤性,有利于连续动态监测和大规模筛查。肝癌早筛和辅助诊断项目HCC7S“7种microRNA检测试剂盒(PCR荧光探针法)”的应用有助于肝癌早期筛查,从而提高肝癌患者的手术切除机会,降低患者的复发率和病死率,造福广大肝病患者。
为了让更多人深入了解项目细节以及未来在临床上带来的潜在获益,阔然基因特邀中山大学生命科学学院庄诗美教授进行专访。
阔然基因:我们都知道,原发性肝细胞癌是全世界常见的恶性肿瘤之一,我国同样也是肝癌大国,那么在您看来,肝癌早筛早诊的临床意义主要包括哪些方面呢?
庄教授:正如您所说,肝癌在全球高发,中国肝癌的新发及死亡病例均约占全球病例的一半。乙型肝炎病毒(HBV)感染和黄曲霉素暴露是我国肝癌的主要致病因素,长期酗酒和高脂饮食也是高风险因素。慢性肝炎肝硬化患者是肝癌的高危人群。
由于肝癌发病隐匿,进展迅速,目前尚缺乏有效的早期筛查手段,导致60-70%的患者就医时已是中晚期,错失有效治疗的机会,肝癌患者的五年总生存率只有10%左右。
然而,如能在早期发现并切除肝癌,患者的五年生存率则可提高到50%以上。因此,早筛早诊早治是提高患者生存质量和生存时间、降低死亡率最有效的途径,也可大大降低家庭和社会的经济负担。
阔然基因:能谈谈您的团队在研发 “血清microRNA肝癌诊断标志物及试剂盒”时,有哪些独到的考虑吗?
庄教授:我们的研发工作除了获得3项授权发明专利,还被国际顶级杂志Lancet Oncology(16:804-15, 2015)以快速通道给予发表,而且,国际肝癌指南的编者也专门写了同期评述,肯定我们发现的分子组合Cmi提供了具有前景的诊断准确性,指出我们的工作开启了microRNA筛查早期肝癌的大门(Lancet Oncology 16:743-45)。
我们的工作之所以会引起国际同行的高度关注,应该是得益于我们有非常特别的研究队列,而且在临床应用的可操作性、稳定性及普适性方面都有比较独到的考虑,在这里列举几点:
1、选择稳定性好的血清microRNA作为检测指标:microRNA耐酸碱耐高温,是很好的疾病筛查标志物。此外,我们采用血清(不含细胞),而不是血浆,避免血浆中大量存在的细胞可能产生的干扰。
2、选择临床可操作性强的标志物:我们选择在肝癌患者血清中明显升高的microRNA作为候选分子,而不采用那些降低的分子。此外,我们剔除了肝细胞内极高丰度的分子(如miR-122),以避免它们在慢性肝炎引发细胞损伤时被释放到血液,造成假阳性结果。
3、经过严格的多模型多中心验证:我们的研发经历了发现、训练建模和验证三个阶段。选择的组合Cmi在训练阶段经过4个模型分析均获得80%以上的诊断准确性,后续又在来自不同医疗中心的3个人群队列得到了验证。
4、特别关注早期肝癌/亚临床期微小肝癌的检测:在对慢性肝炎患者的定期随访中,我们发现了27例小肝癌(诊断时肿瘤小于3cm)患者,通过检测他们在临床诊断前12、9、6、3个月的系列血清,验证Cmi的诊断效果。
5、易推广,具有普适性:血清需求量少,检测步骤简单,仪器在基层医院也可配置。
阔然基因:听了您的介绍,该项研究的确在临床应用方面具有很好的可操作性、稳定性及普适性,那么相比于目前临床上主要的筛查方法,如血清标志物、影像学等,基于您的团队研发的“血清microRNA肝癌诊断标志物及试剂盒”技术体系,在肝癌早筛早诊方面相比于传统方法有哪些优势呢?
庄教授:目前主要采用血清甲胎蛋白(AFP)及B超筛查肝癌,然而它们检测早期肝癌的准确性和敏感性并不理想。文献报道,在临床已诊断为肝癌的患者中,约40-60%病例的AFP水平仍低于警戒值(20 ng/ml);AFP检测早期肝癌的敏感性仅为7-23%。B超对肝癌的检出率有赖于肿瘤大小及操作者的经验。
我们研发的Cmi可以很好地区分肝癌患者与各个非癌人群,包括健康人、乙肝病毒携带者、慢性乙型肝炎患者、乙肝病毒感染的肝硬化患者,其敏感性和准确性均明显优于AFP(以AFP>20ng/ml或400ng/ml为指标),而且可以检出近80%的AFP阴性的肝癌患者。Cmi检测小肝癌(小于)、早期肝癌(BCLC 0+A期)及亚临床期微小肝癌的优势尤其突出。
比如,从小肝癌临床诊断前12个月(Cmi 与 AFP20检出肝癌的敏感性分别是30% 和 7%)和诊断前9个月(Cmi与 AFP20检出肝癌的敏感性是48% 和11%)的数据,可见Cmi 检出亚临床期微小肝癌的敏感性和准确性都远高于 AFP。更多具体的数据在我们发表的论文有详细的描述(Lancet Oncol 16:804-15, 2015)。
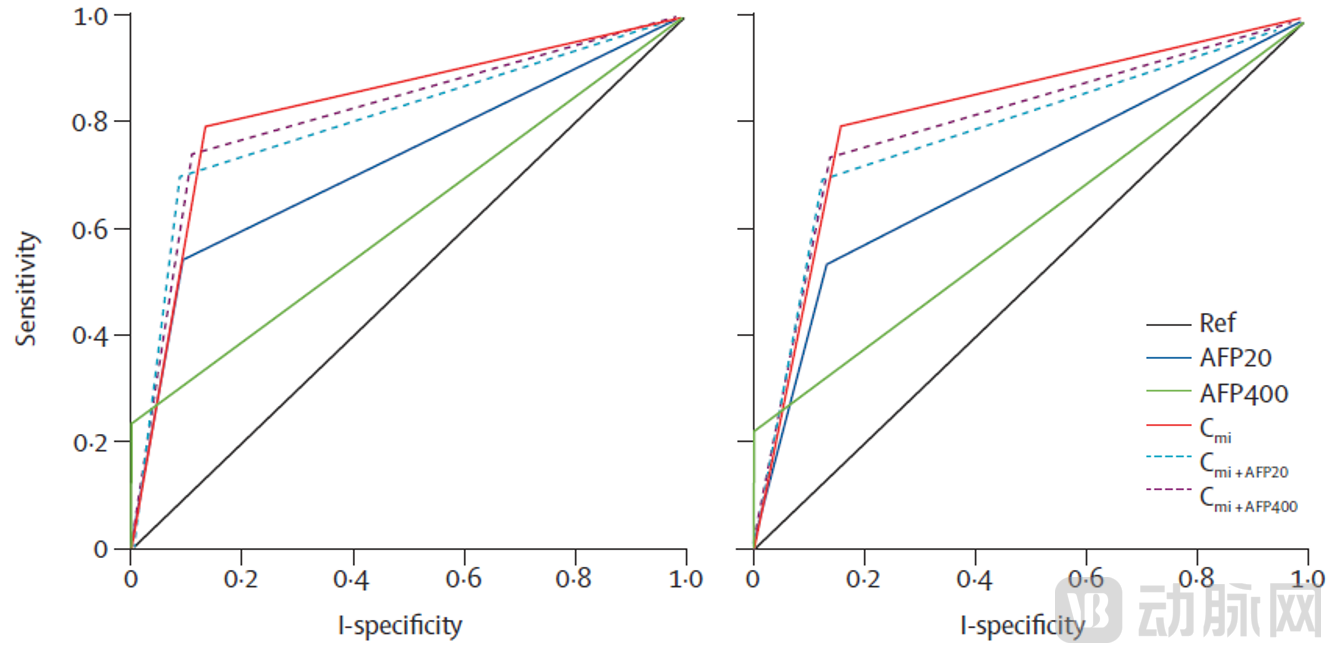
Cmi模型的敏感性和准确性均明显优于AFP[7]
阔然基因:基于此次与阔然基因在血清microRNA肝癌诊断标志物及试剂盒产品转化方面的合作,想请您展望下在肝癌早筛早诊领域的应用前景,获益人群是哪些呢?能够为其目标人群带来什么呢?
庄教授:基于我们成果开发的试剂盒,主要的获益人群是所有肝癌患者,尤其是小肝癌、早期肝癌、AFP阴性肝癌及亚临床期微小肝癌患者,以及肝癌高危人群,包括慢性肝炎、肝硬化患者。
我国有相当大的慢性肝炎肝硬化人群,采用无创性且操作简便的标志物对他们进行长期随访监测,筛查出小肝癌/早期肝癌/亚临床期微小肝癌,及早治疗,可以大大提高肝癌患者的生存率和生存质量,降低死亡率,具有非常重大的临床意义和社会价值。
肝癌术后转移复发监测目前主要基于临床病理特征(包括肿瘤大小、分期与分级、有无血管侵犯等),准确性较低,主要原因包括小癌也会高转移,并且部分患者临床病理特征相似但预后迥异,往往导致术后辅助治疗时,疗效差,副作用大、生存质量差、医疗成本高。
围绕肝癌术后转移复发监测的难题,阔然基因与复旦大学附属华山医院普外科钦伦秀教授团队合作研发的HCC5R“肝癌术后转移复发风险评估试剂盒”,基于转移和关键分子的创新性研究证实分子预测转移可行,创建了一种转移复发预测新方法。
通过筛选分子标志物建立分子预测模型达到更加精准预测的目的,对于低危组,可以定期随访,避免不必要的术后干预(过度治疗);对于高危组,可以更加积极的预防干预,降低术后复发风险。从而达到降低术后复发,延长生存,提高生存质量,降低成本的效果,具有重要的经济价值和社会价值。
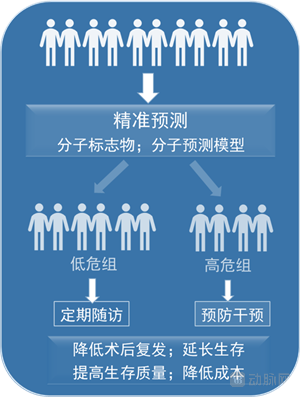
改变术后转移复发的防治模式
HCC5R“肝癌术后转移复发风险评估试剂盒”基于伴转移与不伴转移肝癌之间表达差异显著的153个转移相关基因,建立了能正确预测肝癌转移的多分子预测模型,小样本研究发现区分肝癌有无转移的准确率达90%[8]。
两组独立大样本证实其可准确预测肝癌预后,为全球第二个经大样本验证的转移预测模型(第一为乳腺癌)[9]。进一步优化为“五基因预测模型”,大样本前瞻性研究证实其准确率>70%。
在2021年由北京市希思科临床肿瘤学研究基金会(希思科基金会)、良医汇主办,动脉网等联合主办的第二届肿瘤诊疗黑科技大会上,HCC5R“肝癌术后转移复发风险评估试剂盒”斩获最具学术价值奖,得到全国顶尖肿瘤专家、医疗投资领域及产业大咖的高度关注。
分子残留病灶(molecular residual disease,MRD),在某些情况下也被称为微小残留病灶(minimal residual disease)或可测量残留病灶(measurable residual disease)[10],有越来越多的临床证据表明,MRD状态与肿瘤患者复发、预后分层明显相关[11-15]。
阔然基因肝癌术后MRD检测方案,主要针对接受非姑息性手术的肝癌患者,术后通过NGS平台检测肿瘤循环DNA(ctDNA),获得肿瘤相关热点基因的变异信息,从而评估肝癌术后复发风险,辅助临床医生制定个性化辅助治疗方案。
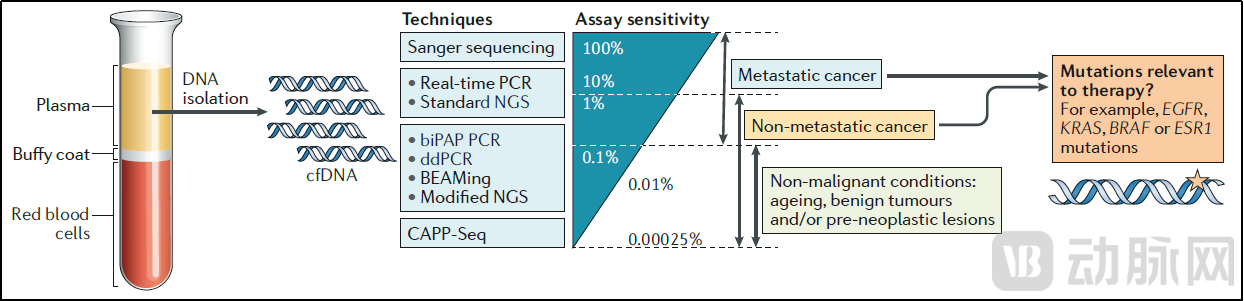
ctDNA检测流程[16]
关于钦伦秀教授
钦伦秀,现任复旦大学附属华山医院外科主任/华山医院北院常务副院长,复旦大学肿瘤转移研究所所长。国家杰出青年基金获得者、长江学者特聘教授、教育部创新团队带头人、973首席科学家,享受国务院特殊津贴。主要从事肝胆外科临床工作30年,每年手术治疗肝胆肿瘤病人400余例。同时从事肿瘤转移复发研究,承担国家科技重大专项肝癌项目、973及国家自然基金国际合作重大项目等多项课题。发表SCI论文180余篇,通讯/第一作者90篇(14篇IF>10),包括Cancer Cell, Cell Metabolism, Gut, Hepatology等,连续三年入选中国高被引学者榜单(hi-index 54),获专利12项。
关于庄诗美教授
庄诗美,中山大学教授,归国博士。本科毕业于复旦大学上海医学院临床医学专业,同时具有儿科学医学博士和细胞生物学理学博士学位,既有临床医生的经历也有基础研究的背景。先后入选/获得教育部长江学者特聘教授、国家杰出青年科学基金、国家百千万人才工程、有突出贡献中青年专家、国务院政府特殊津贴、南粤百杰等。长期从事肝癌发病机制及早期检测和精准治疗策略的研究。作为通讯/共同通讯作者在肿瘤学和肝脏病学的国际一流杂志发表一系列高水平研究论文,包括多篇ESI高被引论文、杂志封面论文、专家同期评述论文。连续入选 “中国高被引学者”榜单。作为第一发明人获授权中国发明专利15项,其中3项已转让。部分成果获 “国家自然科学奖”二等奖(2014)、“教育部高校科研优秀成果奖(自然科学)”一等奖(2013,2019)、广东省科学技术奖自然科学一等奖(2013,2019)。
关于阔然基因
阔然基因成立于2015年,总部位于上海,旗下拥有三家高新技术企业和一家专精特新小巨人企业,致力于提供多应用场景的一站式分子诊断解决方案,包括癌症早期筛查、诊断与监测以及药物研发服务,拥有6款IVD产品注册申报储备,服务中国500余家医院和科研机构,建立了庞大的基因组数据库。公司拥有上海和徐州双研发中心,两家医学检验实验室(“零缺陷”通过CAP权威认证)和精准医学科技研究院,凭借“产品+服务”模式开展肿瘤分子诊断、肿瘤免疫微环境检测及病原微生物检测等业务,为临床医生对患者的诊疗提供一体化解决方案,实现“精准医疗践行者”的理念,推动我国医疗事业发展。
参考文献:
[1] Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021; 71(3):209-249.
[2] Zhou M, Wang H, Zeng X, et al. Mortality, morbidity, and risk factors in China and its provinces, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet, 2019, 394(10204): 1145-58.
[3] 全国多中心前瞻性肝癌极早期预警筛查项目(PreCar)专家组. 中国肝癌早筛策略专家共识[J]. 肝脏, 2021, 26(8):7.
[4] Shim JH, Jun MJ, Han S, et al. Prognostic nomograms for prediction of recurrence and survival after curative liver resection for hepatocellular carcinoma[J]. Ann Surg, 2015, 261(5): 939-946.
[5] 杨 鑫, 贾户亮, 钦伦秀. 肝癌术后复发的分子机制及其预测研究进展[J]. 中国实用外科杂志,2019,39(10):1030-1035.
[6] 国家科技部传染病防治重大专项课题《病毒性肝炎相关肝癌外科综合治疗的个体化和新策略研究》专家组, 陈孝平, 沈锋,等. 肝细胞癌肝切除术后复发预防和治疗中国专家共识(2020版)[J]. 中国实用外科杂志, 2021年41卷1期, 20-30页, ISTIC PKU CSCD, 2021:科技部传染病防治重大专项课题.
[7] Lin XJ, Chong Y, Guo ZW, et al. A serum microRNA classifier for early detection of hepatocellular carcinoma: a multicentre, retrospective, longitudinal biomarker identification study with a nested case-control study. Lancet Oncol. 2015;16(7):804-815.
[8] Ye QH, Qin LX, Forgues M, et al. Predicting hepatitis B virus positive metastatic hepatocellular carcinomas using gene expression profiling and supervised machine learning[J]. Nat Med, 2003, 9(4): 416-423.
[9] Roessler S, Jia HL, Budhu A, et al. A unique metastasis gene signature enables prediction of tumor relapse in early-stage hepatocellular carcinoma patients[J]. Cancer Res, 2010, 70(24): 10202-10212.
[10] 吴一龙, 陆舜, 程颖,等. 非小细胞肺癌分子残留病灶专家共识[J]. 循证医学, 2021, 21(3):7.
[11] GARCIA-MURILLAS I, CHOPRA N, COMINO-MÉNDEZ I, et al. Assessment of Molecular Relapse Detection in Early-Stage Breast Cancer[J]. JAMA Oncol, 2019, 5(10): 1473-1478.
[12] RADOVICH M, JIANG G, HANCOCK B A, et al. Association of circulating tumor DNA and circulating tumor cells after neoadjuvant chemotherapy with disease recurrence in patients with triple - negative breast cancer: Preplanned secondary analysis of the BRE12-158 randomized clinical trial [J]. JAMA Oncol, 2020, 6(9): 1410-1415.
[13] TIE J, COHEN J D, WANG Y, et al. Circulating tumor DNA analyses as markers of recurrence risk and benefit of adjuvant therapy for stage Ⅲ colon cancer[J]. JAMA Oncol, 2019, 5 (12): 1710-1717.
[14] SAUSEN M, PHALLEN J, ADLEFF V, et al. Clinical implications of genomic alterations in the tumour and circulation of pancreatic cancer patients[J]. Nat Commun, 2015, 6: 7686.
[15] PARIKH A R, VAN SEVENTER E E, SIRAVEGNA G, et al. Minimal residual disease detection using a plasma – only circulating tumor DNA assay in colorectal cancer patients[J]. Clin Cancer Res, 2021.
[16] Pantel K, Alix-Panabières C. Liquid biopsy and minimal residual disease-latest advances and implications for cure. Nat Rev Clin Oncol. 2019;16(7):409-424.





























