
石彦教授博士期间师从美国衣阿华大学Charles Lutz教授进行EBV的细胞毒性研究,其后进入马萨诸塞大学医学院在Kenneth Rock教授的指导下开展对免疫危险信号的研究。在加拿大卡尔加里大学建立实验室后,他和Matthias Amrein教授合作,发明了原子力显微镜基础上的单细胞力谱仪,从而开展力学效应在免疫激活中的调节功能。
2012年石彦从加拿大回国,受施一公邀请加入清华大学医学院,研究方向包括Treg免疫抑制的分子机制与转化应用、肠道微生物代谢产物对宿主免疫系统的调控等。2021年成立了针对自身免疫性疾病和炎性疾病的生物制药公司——博迪贺康,致力于创新型Treg免疫治疗,目前已完成从种子到Pre‑A的多轮融资。
在自身免疫性疾病中,Treg细胞作为免疫系统的“刹车”,其功能认知尚不充分,临床上的调控手段也十分有限。清华大学石彦教授团队凭借十余年的研究积累,从一个“偶然的力学发现”出发,不仅揭示了Treg细胞免疫抑制的核心机制,更将这一发现成功转化为创新型Treg免疫治疗——针对自身免疫性疾病和炎性疾病的生物制药公司博迪贺康的药物与细胞治疗管线,旨在为炎症性肠病、银屑病等自身免疫疾病提供全新的解决方案。
从一台意外改装的力学装置,到一条条可进入临床路径的技术管线,石彦教授和他的团队展现了把“基础发现”走向“可产业化”路径的典型样本。更重要的是,这个案例本身对中国科研生态的启示:跨学科的视角、敏锐的可转化意识、以及恰当的团队与组织分工,要比单纯的传统学术追求更能产生对社会有影响力的成果。
在接受动脉橙果局的采访过程中,石彦教授表现出典型的“低调学者”风格:不善露面、不愿过多宣传,而更愿意把精力放在科学问题上。不过他也表示,作为公司的创始人,参与对外沟通与对内技术把关是不可或缺的职责——只是在组织管理和商业推进方面,他更倾向于“做顾问、做技术把关人”,把运营管理交给更专业的职业经理人。
1力学视角下的突破:揭示Treg 细胞“刹车”调控机制
调节性T细胞(Regulatory T cells,简称Treg细胞)是免疫系统中一类重要的T细胞亚群,通过抑制其他免疫细胞(如效应T细胞和B细胞)的活性,发挥“免疫刹车”的作用,确保身体在抵御外来病原体的同时不攻击自身组织。
作为免疫系统的“和平使者”, Treg细胞在多种疾病中具有重要研究价值。例如,Treg功能缺陷可能导致自身免疫病或过敏反应,而Treg过度活跃可能削弱抗肿瘤免疫或抗感染能力。因此,揭示并调控Treg细胞功能也成为许多免疫疗法(如癌症免疫治疗和移植免疫治疗)的关键研究方向。
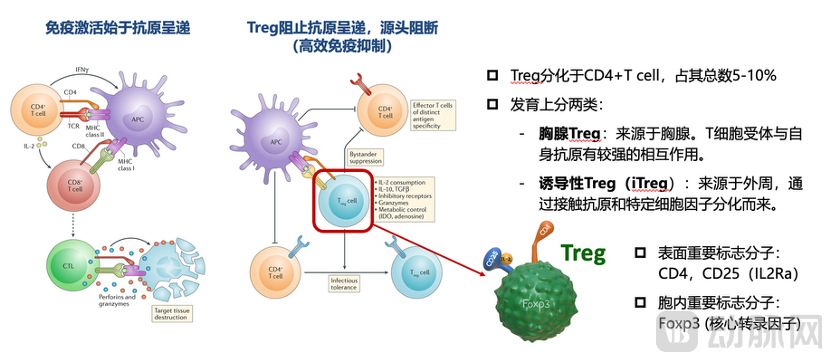
图:调节性T细胞(Treg)
但是如何维持Treg细胞的稳定性和抑制功能是一个关键挑战。首先,Treg细胞亚群众多,其表型和功能在炎症或肿瘤微环境中不稳定,容易失去其免疫抑制功能,甚至可能转化为促炎症细胞(如产生IL-17的细胞);其次,天然Treg细胞在血液中数量稀少(仅占CD4+ T细胞的1%~2%),难以通过直接分离来满足临床治疗所需的大量细胞;此外,Treg细胞的体外扩增过程复杂,需要严格的GMP标准,且扩增后细胞的稳定性和功能可能受损。
石彦教授团队的科研旅程始于对“免疫危险信号”和细胞力学的早期研究。一个偶然的实验现象引起了他们的注意:Treg细胞与树突状细胞(DC)在高强度粘附后,竟然能抑制DC的抗原呈递功能。这一发现颠覆了传统上认为细胞因子是Treg细胞免疫抑制唯一途径的认知,石彦教授因此提出了“力学调控免疫微环境”的全新假说。
这个假说认为,Treg细胞的免疫抑制作用不仅仅依赖于细胞因子,细胞与细胞之间的物理接触和力学作用也在其中扮演了关键角色。Treg与DC之间的强粘附能够直接抑制DC的抗原呈递,从而有效抑制免疫反应。这种力学作用提供了一种不同于传统细胞因子通路的免疫调控机制。
其实石彦教授的科研轨迹并非一开始就在Treg上。早年他在研究尿酸晶体与痛风时,为了研究晶体与细胞膜之间的力学相互作用,搭建了一套单细胞力学测量装置。
“我们用一台研究晶体的机器,观察到调节性T细胞(Treg)在与树突状细胞接触时,偶然结果发现Treg表现出显著的强粘附特性。”正是这句“偶然”,把他的研究视角从传统的分子免疫学扩展到“力学如何影响免疫功能”的问题域——一个长期被忽视但在功能上具有重要意义的维度。
之后石彦教授将实验室的重心逐渐转向解析Treg的力学生物学基础。这一方向既有基础科学的深度,也有明确的可转化路径:如果力学可以作为“开关”调控免疫细胞行为,那么它既是新的药物靶点,也是工程化细胞治疗的设计原则。
进一步的研究表明,这种力学效应的背后涉及多层次信号传导与细胞内效应器的复合机制。根据石彦教授团队已发表的相关文献,Foxp3的表达、Ryr2(Ryanodine receptor 2)在Treg中的调控、细胞内Ca2+浓度的变化、mCalpain(胞内钙激活蛋白酶)活性的差异,最终影响Talin1的切割与LFA-1(整合素)周转,从而改变Treg与树突状细胞接触时的力学表现。这一联系既解释了以往仅靠分子表型难以解释的功能学差异,也为干预提供了多点切入的可能。
科研之外,这一链路也带来了可被临床应用的转化思路:一是通过小分子或外用药调控相关靶点以诱导或加强iTreg的生成;二是通过工程化方法直接将常规CD4+ T细胞改造成具有Treg-like力学和功能的细胞。
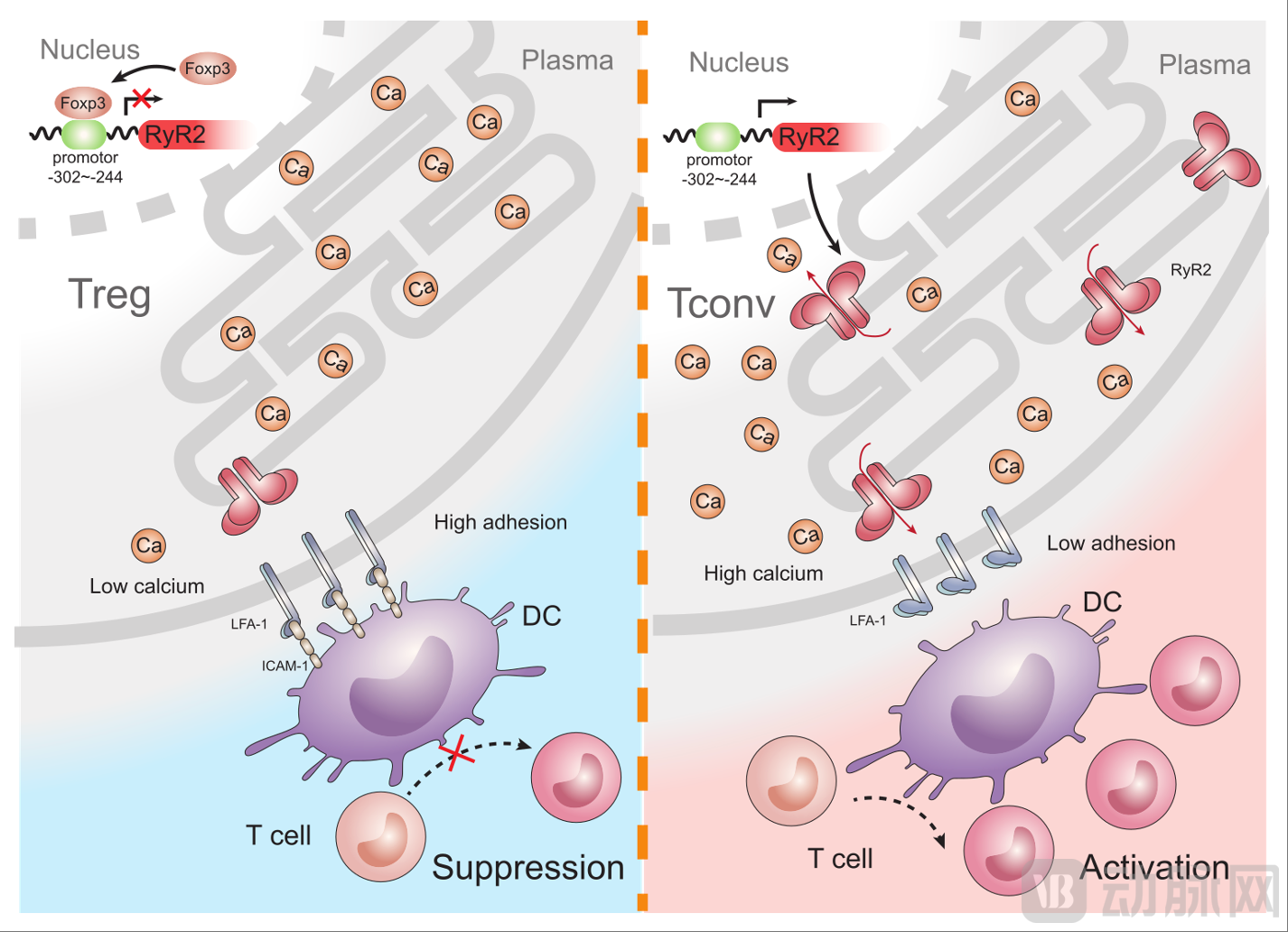
图:基于Treg免疫抑制通路靶点实现免疫抑制性T细胞的生成
2从实验室到临床:Treg 技术的转化与管线布局
据统计,中国约有5000多万自身免疫疾病患者,预估市场规模在百亿元级别。但是现有的治疗手段以长期服用免疫抑制药物或激素为主,患者依从性差且有潜在的肿瘤发生或感染风险。即便是现有的Treg细胞疗法也需要定期从患者身上采血、分离纯化和体外诱导,操作性较差,而体外诱导的Treg回输后存活期短,严重限制了治疗效果。
2021年石彦教授团队与清华大学完成了Treg技术成果转移,并于同年12月成立了博迪贺康。这是一家致力于开发自身免疫性疾病和炎性疾病创新型Treg免疫治疗的生物制药公司,临床开发的背后基础,正是石彦教授团队多年来在Treg领域的科研成果。

目前,博迪贺康围绕Treg全新作用机制(MoA)布局了多条小分子及细胞药物管线。
其中,调控力学通路的工程化细胞,将常规T细胞通过基因编辑或基因调控转化为具备Treg‑样力学特征与免疫抑制功能的“Enforce‑T”,并开展体外扩增与工艺开发,从而克服传统Treg治疗中“数量少、难扩增、体外扩增后丧失功能”的痛点。数据显示,工程化Treg细胞在体外的免疫抑制效率与天然Treg相当,已完成CMC小试并筹划IIT临床。
除了细胞疗法,博迪贺康在小分子化药方向也在推进2个药物管线。
其中,GPCRx激动剂是一种面向炎症性肠病(IBD)的口服小分子候选药物,作用于肠道树突状细胞并驱动其迁移与iTreg诱导的GPCR靶点。该口服肠溶缓释制剂,在肠道局部发挥作用,调动CD11b+、CD103+、RALDH+类型的肠道树突状细胞携带抗原进入引流淋巴结,从而诱导外周来源的pTreg(即iTreg)生成,重建抗原特异性的免疫耐受。目前公司对BT‑101的研发步骤也已经走到了IND‑enabling的阶段:完成先导化合物筛选、药效学(DSS、TNBS、过继性T细胞转移模型)验证、部分安全性评价、CMC与DMPK工作正在推进,计划在中美两地提交临床申请并面向全球化开发。
此外,公司还在推进另一款小分子药物管线——Ryr2抑制剂,主要用于轻度银屑病(及其他自免性皮炎:湿疹、特异性皮炎等)的治疗。
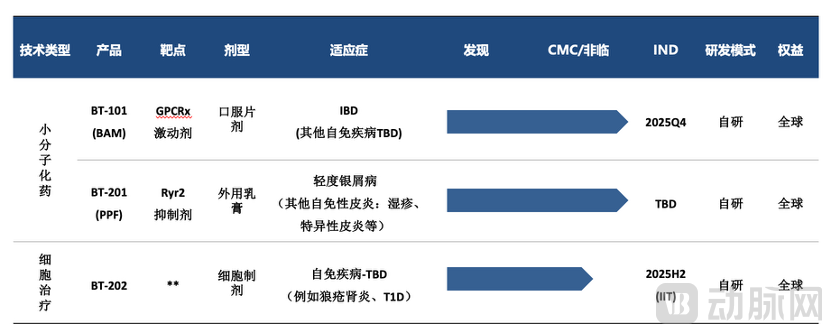
图:博迪贺康围绕Treg全新MoA布局小分子及细胞药物管线(来源:博迪贺康)
“基于Treg细胞的创新疗法,从机制上突破了传统治疗的局限。”石彦教授认为,在自体免疫疾病治疗领域,关于Treg细胞的研究正孕育着改变现有免疫治疗格局的可能性。博迪贺康未来也将继续拓展研发管线,并积极布局临床研究,以期推动Treg细胞在临床中的应用,为自身免疫疾病患者带来福音。
从长远来看,随着机制研究的不断深入,Treg细胞疗法有望完成从实验室到临床的跨越,为患者带来更安全、高效的治疗选择,也为整个行业提供从全新靶点到临床应用的示范路径。
3科研与商业的平衡:技术转化不是“背叛学术”
在生物医药领域,科学家的职业选择往往藏着改变行业格局的伏笔。清华大学医学院石彦教授与清华的结缘,就始于一场"意外邀约"。在加拿大任教授期间,石彦常回国参会,一次与复旦大学的交流,被施一公知晓后,便立马给石彦打电话,邀请他到清华看看。
当时清华大学正着力建设免疫学科,会面中施一公展现出的魄力与远见也打动了石彦。最终,石彦决定加入清华,成为清华大学免疫所早期核心成员之一。这场始于偶然的邀约,促成了他在清华的学术深耕,也助力了清华免疫学领域的持续发展。
回顾自己的科研历程,石彦教授指出,只有让科学发现与产业需求形成共振,才能真正加速生物医药领域的创新效率,避免科研与市场脱节的困境。并且他强调,科学家与企业管理者是两类截然不同的人才谱系。尽管科研人员拥有发现与技术判断力,但企业运营涉及融资、团队管理、人员雇佣等商业决策,这些并非多数学术出身的科学家所擅长或愿意长期承担的事务。
因而他提出了一个相对务实的策略:科学家可以在早期主导技术方向与IP形成,但在公司治理与商业化推进上尽早引入职业经理人或产业化团队。石彦形象地说,教授应当回到实验室,把已进入后期开发的项目交给专业团队管理。
从博迪贺康的成长路径中也可见端倪:公司成立于2021年,三年内发完成从种子轮到Pre‑A的几轮融资,并规划继续融资以支持IND与早期临床试验。公司选择在北京、上海、浙江布局研发与运营,并在北美设立子公司以便推动国际化注册与招募国外早期临床。
“当项目走到临床前节点,如果继续推进将需要大量与自己专长无关的资源,此时应考虑交给专业团队。”石彦教授表示。
在石彦教授及其团队看来,中国科研转化的关键在于建立清晰的分工体系:教授应专注于 IP 创造,凭借学术敏锐度产出原创性成果;职业经理人则负责从研发到上市的全流程运营,弥补科学家在商业思维与管理能力上的短板。
在访谈接近尾声时,石彦教授给年轻科研工作者的建议也非常务实:不要把学术神圣化,也不要把科研成果转化视为“背叛学术”。基础研究与成果转化并非对立,青年学者需在两者间找到平衡——既要有深耕基础、探索未知的定力,也要对产业需求保持敏感度,让科研方向既扎根科学本质,又能回应现实需求。“跨学科视角与可转化意识,比单纯的学术追求更能产生有社会影响力的成果。”
他也鼓励有志于商业化的年轻人趁“年富力强”去尝试技术转化。每个人要根据自己的兴趣与长处选择角色:有的人适合留下继续做基础研究,有的人适合投身企业管理。重要的是,建立起学术与产业的互补机制,而不是把两者杂糅在同一人的肩上。





























