7月1日,根据上交所官网信息,“稻米造血”第一股禾元生物成功通过上海证券交易所上市审核委员会审议,这也是重启科创板第五套上市标准后,首家成功过会的IPO企业。
根据招股书,禾元生物是一家采用第五套上市标准的生物医药行业公司,药品均处于研发阶段,尚无获批上市的药品,尚未盈利。
禾元生物保荐人为国泰海通证券,控股股东及实际控制人为杨代常。
截至招股书签署日,杨代常直接持有禾元生物15.03%股权,为禾元生物第一大股东;通过禾众共创控制禾元生物3.75%的表决权、通过一致行动约定控制发行人10.47%表决权,合计控制禾元生物29.25%的表决权。
2005年5月至2021年1月,杨代常任职武汉大学生命科学学院遗传学系教授,2006年11月发起设立禾元生物,目前担公司董事长兼总经理。
禾元生物持股前十名股东还包括上海同盛、贝达药业、光谷生物基金等。
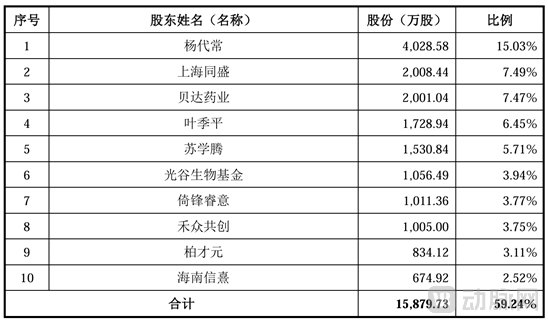
来源:招股说明书(以下图片均来自招股书)
自2022年12月29日递交科创板IPO申请获受理至过会,禾元生物的IPO历程已有两年半,但是离正式上市仍有一段距离。
根据相关统计,2024年至今,科创板上市的20家企业从受理到上市平均时长为624天,其中从过会到成功上市平均需要277天。
01
第五套标准重启后的“首单”
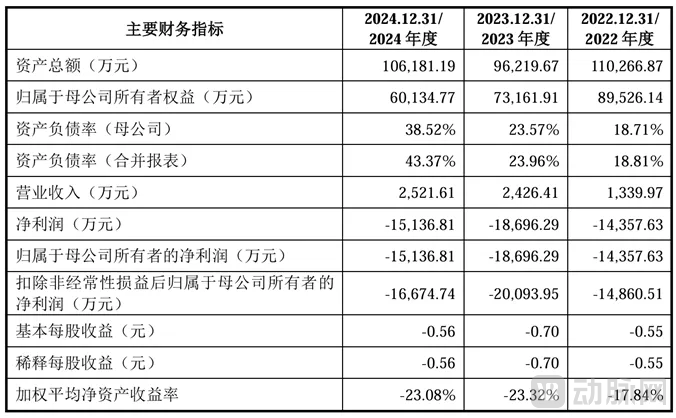
根据招股书,2022年至2024年,禾元生物的营收分别为1339.97万元、2426.41万元和2521.61万元,分别亏损1.49亿元、2.01亿元、1.67亿元,三年累计亏损5.17亿元。
科创板第五套上市标准的重启,让禾元生物在亏损之时也能过会。
据了解,第五套上市标准不对企业营收和净利润规模做出要求,而是强调“主要业务或产品需经国家有关部门批准,市场空间大”“已取得阶段性成果”等,为暂不具备盈利能力但真正有核心竞争力的企业登陆资本市场提供便利。
禾元生物成功过会或许给整个生物医药行业都打了一剂“强心针”。
南开大学金融发展研究院院长田利辉曾在接受采访时分析,恢复科创板第五套标准适用,可以显著增强了资本市场的包容性和适应性,为尚未盈利但拥有核心技术和发展潜力的科技企业提供了直接融资渠道,而且可以激发市场对高科技行业的投资热情。
另有业内人士指出,在没有盈利能力的情况下,从资本市场“输血”对于创新药企非常重要。
据《每日经济新闻》梳理,6年来,54家共有未盈利企业成功登陆科创板。在科创板助力下,这批企业正在快速步入研发成果兑现周期,迈向商业化发展新阶段。
其中20家按照第五套上市标准上市的生物医药企业中,有19家实现核心产品上市,其中2024年,泽普凝、迈卫健、高瑞哲、贝塔宁、金立希、君适达、安方宁、海克威等9款新药产品获批,其中5款为1类新药。
02
核心产品预计近期上市
禾元生物持续亏损主要因为重组人白蛋白等核心产品尚未实现商业化。
据梳理,禾元生物产品主要包括药品、药用辅料以及科研试剂。目前药品均处于研发阶段,尚未开展商业化生产销售,营业收入主要来源于销售药用辅料、科研试剂及其他产品的收入及少量技术服务收入。

药品管线推进情况
从药品研发情况来看,其中HY1001重组人白蛋白注射液(OsrHSA)已完成III期临床试验并取得临床研究报告(CSR),2024年9月NDA获得受理,药品上市审评进展顺利,已完成了大部分的审评程序,预计将于近期获批上市,获批适应症预计为“肝硬化低白蛋白血症”。
HY1002治疗由轮状病毒引起的儿童感染性腹泻的重组人乳铁蛋白溶菌酶口服液已完成II期临床试验,预计2025年第三季度完成与CDE的沟通,2025年底启动III期临床。
另外值得关注的是,在核心产品尚未商业化之时,与最初披露的招股书相比,禾元生物的募资金额缩水了11亿元。
禾元生物初版招股书显示,拟募集资金35.02亿元,但是在禾元生物上会稿中,募资金额变为24亿元。植物源重组人血清白蛋白产业化基地建设项目、新药研发项目、补充流动资金三个项目的拟分别投入募资分别减少了2.52亿元、1.52亿元和7亿元。
03
以合成生物实现“稻米造血”
支撑禾元生物“稻米造血”核心产品的是其背后的技术平台。
根据招股书,禾元生物“稻米造血”产品的开发是基于其水稻胚乳细胞生物反应器表达体系,包括上游技术水稻胚乳细胞生物反应器高效重组蛋白表达平台(OryzHiExp)和下游技术重组蛋白纯化技术平台(OryzPur)。
除了技术本身,禾元生物备受关注的因素或许还在于背后的人血白蛋白市场——需求量非常大,但以进口为主,替代空间较大。
弗若斯特沙利文的数据显示,2020年中国人血白蛋白治疗药物市场规模为258亿元,2030年预计增长至570亿元,2025-2030年复合增长率达6.0%。
据太平洋证券研报分析,受限于国内血浆供应,国内市场的供给仍以进口为主,存在较大的国产替代空间。
中检院批签发数据显示,2023年我国人血白蛋白批签发批4401批。其中Octapharma、CSLBehring、Takeda和Grifols四家海外血制品巨头占我国人血白蛋白批签发批次接近70%,国内市场的供给仍以进口为主,存在较大的替代空间。
但巨大的需求也导致重组人血白蛋白产品需要面对规模化难题。
据报道,杨代常曾分析,人血白蛋白每剂量20克,相比之下单抗是每剂量100mg,相差200倍,所以抗体中国一年只要30多公斤就能解决问题,疫苗的产量要求更少,相比之下,人血白蛋白中国市场年需求量600多吨。
同时,剂量大就意味着对安全性要求更高,人血白蛋白对宿主蛋白杂质要求为0.00001%,抗体药物为0.01%,相差100倍,与疫苗之间则是10万倍差别。从内毒素看,人血白蛋白要求小于0.0083EU/mg,是抗体要求的100倍,疫苗的10万倍,但是人血白蛋白售价约35-40元/g,抗体超过2万元/克。
因此重组人血白蛋白要面对纯度、安全、生产成本和规模化四方面挑战。
“重组人血白蛋白其实在技术层面可以实现,关键就是成本下不来,如果用细胞生产,1克要数千元,一针10克的话价格太高,患者用不起,所以重组人血清白蛋白需要攻克规模化和高成本的难题。”杨代常说。
据介绍,禾元生物的植物源重组人血清白蛋白从稻米中提取,在规模化和安全性方面具有一定优势。
另外,从人血白蛋白市场来看,除了上述提到的外企,国内还有天坛生物、上海莱士、华兰生物等多个参与者,但是从重组人白蛋白市场来看,似乎仍是一片蓝海。
根据招股书,截至2025年5月31日,全球市场仅安睿特的重组人白蛋白药品于2024年4月和2025年3月分别在俄罗斯和吉尔吉斯斯坦实现注册上市。
日本田边三菱制药株式会社通过毕赤酵母表达系统生产的重组人白蛋白药物Medway于2007年在日本批准上市,但是由于该药物试验数据涉嫌造假,已于2009年撤市。
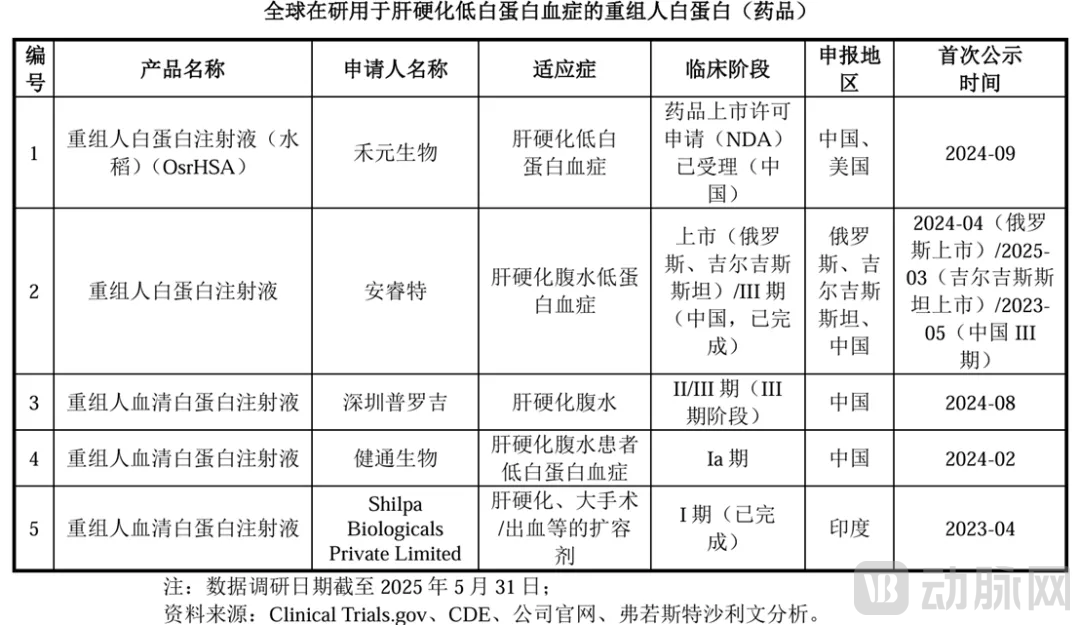
目前国内除了禾元生物,安睿特、深圳普罗吉和健通生物均在布局重组人白蛋白,目前均未上市,禾元生物有望成为国内首个上市的用于肝硬化低白蛋白血症的重组人白蛋白产品。
但是禾元生物在招股书中表示,虽然HY1001具有先发优势,但目前国内仍有2款重组人白蛋白在研药物已完成或已进入III期临床研究阶段,若审评顺利,该等竞品预计将在1-3年后陆续实现获批上市,与HY1001展开竞争,届时公司可能需开展更大规模的研发和营销活动。
另外,由于属于较为创新的产品,上市后的商业化和临床实际接受程度可能存在一定未知数。
禾元生物在招股书中进一步指出,HY1001可能存在销售不及预期的风险。
因为血浆来源的人血清白蛋白(pHSA)拥有数十年的真实世界临床使用经验,相较而言,重组人白蛋白产品HY1001与其他创新药相似,为获取医生和患者群体的广泛接受和认可,需要开展较多的学术推广、市场教育和真实世界数据研究等,将会有一段时间的市场导入期。
另外,HY1001未来商业化市场可分为院外和院内市场。
根据招股书,在进入国家医保目录前,HY1001销售主要以院外市场为主,院外市场准入尚需经历定点关联报备、各省挂网公示等环节,与零售药房建立合作,并通过处方外流路径实现院外市场的销售。
同时,禾元生物在积极筹备医保目录谈判的各项准备工作,将积极参与国家医保目录谈判,若纳入国家医保目录,将面临一定的价格降幅,且后续仍需各省挂网公示、医院药事委员会审批等环节方能实现院内市场大规模销售,公司尚需一段时间按照相关规定履行必要的市场准入程序。

—END—
生物制造产品注册与准入培训
重磅开启
2025年7月26-27日,北京·亦庄国际生物医药园,“生物制造产品注册与准入培训”重磅开启。
本活动由动脉网与芳博士联合主办,首次聚焦六大黄金赛道(医药、美妆、食品、动保、农业、材料),为您提供从实验室到市场的实战突围指南。
亮点一:顶级专家阵容
汇聚药品、兽药、食品等领域的权威大咖:余立(原北京市药检所专家)、董义春(中国兽药协会秘书长)、斯榕(国际食品法规领袖)等十余位实战讲师。将带来全球监管标准(FDA、NMPA等)的深度解析,助您精准选择注册路径、构建合规数据包。
亮点二:实战目的导向
直面企业痛点,解决中试“死亡谷”、注册准入难题。通过案例研讨,学习医药IND/NDA、化妆品新原料备案、兽药审批等策略,制定定价、集采应对制胜方案。高效跨域协同,提升市场竞争力。
具体日程如下:
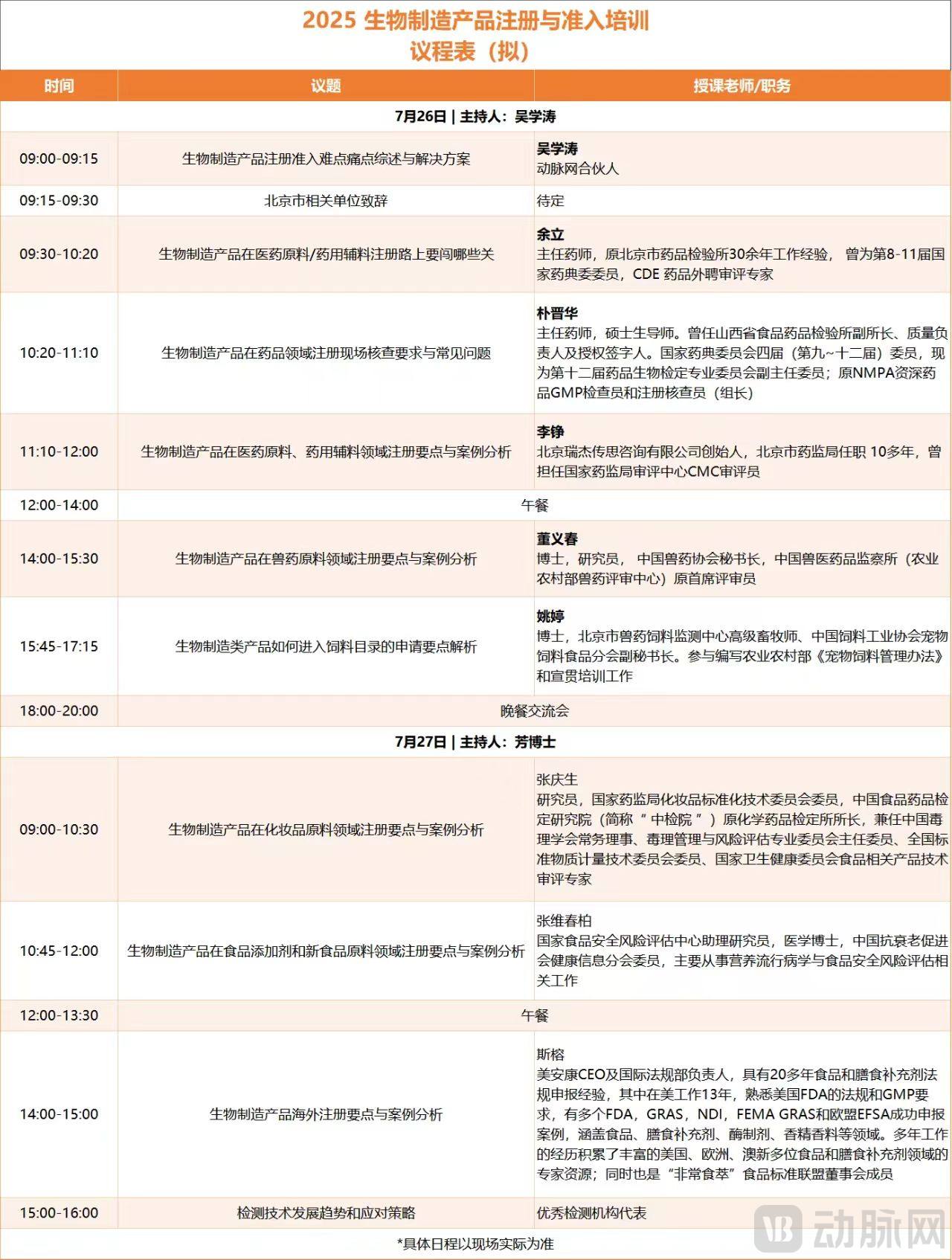
限席80人,先到先得,与专家面对面,助您的产品从“生物造”迈向“市场赢”!
识别下方二维码报名锁定席位,开启合规突围之旅!






























