11月10日,下一代CAR-T细胞疗法的晚期临床公司Lyell Immunopharma,宣布与斯丹赛生物(ICT,Innovative Cellular Therapeutics)达成合作,获得研究、开发、制造和商业化LYL273(前身为GCC19CART)除中国(含港澳台)外的全球独家权利。
根据协议,斯丹赛生物将获得4000万美元的预付款和190万股Lyell普通股,有资格获得额外的现金和股权对价,以及未来净销售额的特许权使用费。额外的现金对价包括潜在的3000万美元临床里程碑,后期监管里程碑高达1.15亿美元,商业销售里程碑高达6.75亿美元。在达到某些临床和后期监管里程碑后,额外的股权对价包括185万股Lyell普通股。潜在交易总金额约为8.6亿美元(约合人民币61.25亿元)。
LYL273正在推进具有巨大未满足需求的结直肠癌适应症,已获得FDA授予治疗mCRC(转移性结直肠癌)的快速通道资格。目前,1期临床试验正在继续招募难治性mCRC患者,以确定推荐的2期剂量。
1独家靶点:CAR-T治疗难治性结直肠癌,首次观察到客观临床活性
结直肠癌(CRC)是全球癌症死亡第二大原因,约半数患者会进展为晚期结直肠癌。据世界卫生组织(WHO)数据,全球每年新增超过190万例结直肠癌患者,每年大约90万人死于结肠或直肠癌,其中转移性结直肠癌患者预后较差,5年生存率<15%,开发新的治疗策略用于晚期结直肠癌很有必要。鸟苷酸环化酶-C(GCC)表达于胃肠上皮细胞,是治疗结直肠癌及转移性结直肠癌(mCRC)的重要靶点。目前,斯丹赛在这一靶点CAR-T上具有独家性。
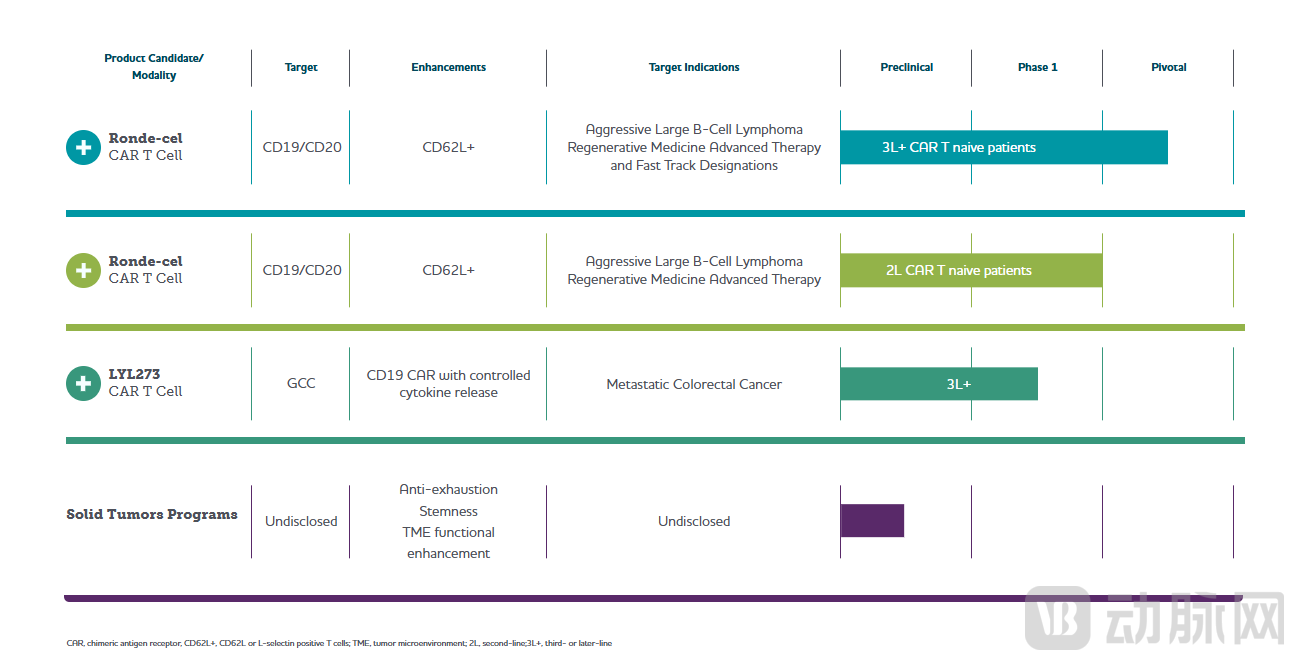
LYL273是一种新型的自体GCC靶向CAR--T细胞治疗候选产品,用于治疗转移性癌症(mCRC)和其他表达GCC的癌症。资料显示,LYL273是一种慢病毒载体转导的自体CAR-T细胞治疗产品,由靶向实体瘤的GCC CAR,CD19 CAR及细胞因子组成。其通过CD19 CAR促进实体瘤CAR-T细胞的体内扩增,使CAR-T细胞向肿瘤迁移和浸润,并且增加CAR-T细胞在肿瘤微环境中的杀伤能力。
2024年,一项发布在JAMA Oncology的中国研究表明,对于接受过预治疗的转移性结直肠癌患者而言,接受GCC19CART治疗安全且可耐受。文章指出,这是作者团队所知的首次CAR-T疗法治疗难治性结直肠癌且观察到客观临床活性的研究。
数据显示,在接受任一剂量的共15例患者中,6例(40%)达到部分缓解(PR),5例为疾病稳定(SD),4例病情进展(PD),整体临床获益率(DCR)为73%。而在2x106CAR-T细胞/kg剂量水平下,ORR和DCR分别提升至57.1%和100%,无进展生存期(FPS)显著高于1x106低剂量水平治疗组(6.0个月vs.1.9个月),且中位总生存期(mOS)达到了26.1个月。
在美国进行的I期临床试验中,根据实体瘤反应评估标准(RECIST)1.1,使用LYL273治疗难治性mCRC的患者达到了67%的总体反应率和83%的疾病控制率(完全和部分反应加稳定疾病),在迄今为止研究的最高剂量水平下具有可管理的安全性。
今年8月,LYL273完成用于三线或以上的复发/难治转移性结直肠癌(R/R mCRC)患者的美国I期临床试验关键剂量爬坡试验。在1x106与2x106CAR-T细胞/kg的两个剂量组中,均未观察到3级或以上细胞因子释放综合征(CRS)。尤其,LYL273在高剂量水平下具有良好的安全性和有效性:在2x106CAR-T细胞/kg剂量水平下,5名已经评估疗效的患者中有4名(80%)达到客观缓解,中位缓解持续时间(mDoR)为6.9个月。
2实体瘤CAR-T:破局细胞扩增、杀伤能力、肿瘤微环境难题
CAR-T技术治疗实体瘤需要解决四个关键问题:CAR-T细胞迁移(trafficking)与浸润(inflitration)、CART细胞在体内扩增受限(amplification)、有限的杀伤能力以及T细胞耗竭难以在体内维持(persistence)。
LYL273(GCC19CART)源于斯丹赛自主研发的针对实体瘤CoupledCAR®平台。该平台使用双重CAR方法来刺激免疫系统,促进CAR-T细胞扩增;增强了与肿瘤细胞迁移相关的基因表达,改善了CAR-T细胞向肿瘤迁移和浸润受到抑制的困境;增强CAR-T细胞在肿瘤微环境中的杀伤能力;进入实体瘤后,CoupledCAR可刺激机体产生、募集更多的免疫细胞产生更有效和持久的反应。
斯丹赛创始人肖磊博士在接受动脉网此前采访时提到,“尽管CAR-T仅能识别占细胞抗原总数不到20%的细胞表面抗原,但根据血液肿瘤的经验,一种血液肿瘤只需要一个细胞表面抗原就能够靶向和治疗。所以原则上讲,只需要一个有效的实体瘤的靶点就可以用于治疗一种实体瘤。细胞表面抗原应该能够找到相当多个合适的实体瘤靶点。例如,我们找到了治疗肠癌的靶点GUCY2C,以及治疗甲状腺癌的靶点TSHR。因此难以识别细胞内抗原不应该成为CAR-T不能够治疗实体瘤的原因,更不该解读为CAR-T比TCR-T或TIL技术有效性可能更差。实际上,三个技术平台如果都能找到合适的靶点,接下来将要面对同样的问题,如抑制性肿瘤微环境。CAR-T一定会因为其简单易操作,更快地发展改进,最终胜出。”
目前,斯丹赛已将CoupledCAR®平台扩展至其他实体瘤产品线,如治疗前列腺癌的产品PAPCAR-T,数据显示出明显的临床活性;以及卵巢癌、甲状腺癌等临床需求巨大的实体瘤。
2009年,肖磊博士创立了斯丹赛,并从2016年初全职担任公司CEO。2005年,肖磊博士回国后,在中国科学院上海生物化学与细胞生物学研究所担任PI。此前,他获得了德国慕尼黑大学博士学位,随后在约翰霍普金斯大学从事博士后研究,在胚胎/诱导多能干细胞,细胞疗法和基因编辑领域有着20余年的经验。
作为国内早期入局的CAR-T Biotech,斯丹赛曾获多家医疗领域资本支持,并在全球范围内拥有百余项全球专利及专利申请。2016年完成鼎晖创投和健桥资本投资的A轮融资;2017年底,斯丹赛完成了包括火山石资本、高特佳投资、软银中国等的1.8亿元B轮融资;2019年完成领航新界领投的B+轮融资;2021年达成超4000万美元C轮融资,由鼎晖VGC领投、多家投资机构跟投。
3“不差钱”的海外买家:现金+股权对价的长期合作模式
从交易细节来看,“现金+股权对价”具有鲜明的合作属性。对于斯丹赛而言,此次交易更重要的是GCC19CART出海价值,并将向全球生物医药领域展示与验证其实体瘤平台CoupledCAR®。
对于Lyell而言,LYL273交易完成将加强其实体瘤管线布局。
Lyell是个“不差钱”的海外买家。公告指出,Lyell当前预计2025年的净现金使用量将在1.55亿美元至1.6亿美元之间,不包括交易的4000万美元预付款,低于其之前1.75亿美元至1.85亿美元的净现金用途指导。交易完成后,Lyell预计其现金将足以供应其大型B细胞淋巴瘤患者临床项目的数据和进展更新,以及LYL273一期临床试验的额外临床数据,为直至2027年的运营提供资金。
Lyell创立于2018年,总部位于美国加州旧金山,聚焦克服癌症免疫疗法中的T细胞衰竭,致力于开发针对血液系统恶性肿瘤和实体瘤患者的下一代CAR-T细胞疗法产品。
早期,Lyell同步推进CAR-T、TCR-T与TIL三大T细胞疗法。2019年与GSK达成协议,就靶向NY-ESO-1合作开发针对实体瘤的TCR-T管线。核心管线包括CAR-T疗法LYL797、TIL疗法LYL845,TCR-T疗法NY-ESO-1C239。
但在2024年6月,基于其专有的Gen-R技术平台开发的核心产品LYL797(ROR1靶向CAR-T)在三阴乳腺癌的I期临床中发生了1例死亡事件。患者在第41天出现5级呼吸衰竭后死亡;22%的患者出现肺炎相关的剂量限制毒性,最常见的严重程度为3级或更高。虽然FDA并未即刻叫停临床试验,但Lyell在四个月后全面停止了LYL797的临床开发,同时放弃了LYL845在内的所有TIL项目。
而后,Lyell迅速进行了战略调整——推进其自有平台早期管线的同时,通过收购与授权合作丰富临床阶段管线。自有平台方面,以LYL797为基础开发的下一代ROR1 CAR-T疗法LYL119,结合四项新型重编程技术。临床前研究表明,LYL119具有提供有效而持久作用的潜力,正在推进至一项针对ROR1实体瘤患者的I期临床试验。
2024年10月,Lyell收购了ImmPACT Bio,支付3000万美元的预付款和3750万股Lyell普通股,获得当前进展最快的临床管线LYL314。这是一款下一代双靶向CD19/CD20 CAR-T细胞疗法,已获得用于治疗三线或三线以上复发/难治性大B细胞淋巴瘤(LBCL)的快速通道资格认定,预计在年底更新PiNACLE试验进度,2027年提交BLA。今年4月,LYL314已获得FDA的再生医学先进疗法(RMAT)认定,用于治疗接受过两种或两种以上既往治疗后复发或难治性LBCL的成年患者。
资本背景上,Lyell与中国链接紧密,并拥有着同样“不差钱”的产业端资源。2021年6月17日,Lyell在纳斯达克上市。主要股东包括ARCH Venture Partners、GSK、Foresite Capital、Gemini Investments、Milky Way Investments;药明康德、高瓴、红杉中国均为其股东。
Lyell创始人Richard D.Klausner从事过近30年的过继性细胞疗法研究,是美国国家科学院、美国艺术与科学院、美国国家医学院院士,曾任美国国家癌症研究所第十一任所长、盖茨基金会全球健康执行董事。作为医疗健康领域的连续创业者,他曾是illumina前高级副总裁、首席医疗官和首席机会官,参与创立与管理Juno Therapeutics、GRAIL、Sonoma Bio、LifeMine Therapeutics等多家明星Biotech。
2021年红杉全球医疗健康产业峰会上,Richard D.Klausner院士在与红杉资本全球执行合伙人沈南鹏的对谈中提到:“在过去的5年里,不管是人员质量还是创新性上,中国的生物科技行业的成长令人印象深刻。生物科技行业需要从科技行业来吸取经验——我们正在看到,生物技术领域的一流企业都是平台型公司。不是惯常说的合同外包加工或技术工具公司,而是像Moderna这样具有拓展性、可以生产“APP”,甚至是生物科技领域里供普通消费者使用的“杀手级应用程序(killer apps)”。 我认为我们将会看到一批比想象中更雄心勃勃、善于扩张的生物科技公司,他们将不再仅仅是凭借着一款好的产品从而迅速‘卖身’给大型制药企业,而是更会和科技企业一样崛起。 ”
对于斯丹赛而言,现在就是这个崛起时刻。





























