8月20日,ADC新锐普众发现和丹麦公司Adcendo ApS(简称“Adcendo”)共同宣布,双方就代号为ADCE-T02(普众发现研发代号AMT-754)的一种新型、高度差异化的靶向组织因子(Anti-TF)的抗体偶联药物(ADC)达成许可协议,Adcendo将获得在中国大陆、香港特别行政区、澳门特别行政区及中国台湾地区以外的全球独家开发和商业化权利,而普众发现将保留以上地区的开发和商业化权利。
根据协议的财务条款,普众发现将获得数千万美元的首付款,并将在达成后续开发、监管及商业里程碑时,将收取总计超过10亿美元(约71亿元)的总里程碑付款,以及基于全球(不包括大中华地区)净销售额的个位数至低两位数百分比的销售提成。
这是普众发现的第二笔对外授权交易。两年前,普众发现与昂阔医药达成许可协议,将一款潜在高度差异化、Second-in-Class,靶向CDH6的抗体药物偶联物(ADC)在大中华区以外的全球范围内独家开发和商业化授权昂阔医药。
ADCE-T02已在澳洲申报进入临床试验,预计将于近期申报美国IND
本次交易的管线ADCE-T02是一种新型的、高度差异化的Anti-TF ADC。据公告,其独特的抗体设计能够减弱对凝血通路的影响,同时,T1000-exatecan连接子-有效载荷技术平台经研究证明,能够放大“旁观者效应”、提高连接子稳定性,并具备克服耐药性机制的潜力。这些差异化的特性有望转化为更高的临床治疗反应率、更长的疗效持续时间以及更好的安全性,拥有更优异的治疗窗口。
TF又称凝血因子Ⅲ,是一个由263个氨基酸残基组成的跨膜单链糖蛋白。多项研究表明,TF在多种实体瘤中存在阳性表达,包括宫颈癌(100%),非小细胞肺癌(34%-88%),子宫内膜癌(14%-100%),卵巢癌(75%-100%)等。TF的这种高表达可能有助于肿瘤细胞的生长和存活、血管生成和转移。因此,被认为是一个极具潜力的肿瘤治疗靶点。
目前,全球范围内TF ADC在研项目相对较少,仅有一款由Seagen与Genmab联合开发的Tivdak(Tisotumab Vedotin)获批FDA,用于治疗化疗期间或化疗后疾病进展的复发性或转移性宫颈癌成年患者。2022年,再鼎医药以3000万美元的首付款引进该款药物,目前已经在中国澳门获批。
ADCE-T02采用普众发现自主的开发的连接子技术T moiety。T-Moiety是一种高亲水性自裂解连接子修饰技术,用于开发ADC的新型Linker。T-Moiety连接子具有更优的“疏水屏蔽效应”与稳定性,相较于PEG修饰毒性更低,毒素同样采用Exatecan,在耐药性方面优于Dxd。此前授权昂阔医药的AMT-707同样来自此技术平台。
在T-Moiety平台上,普众发现进一步开发了T1000连接子,该连接子能够克服Exatecan因其过强的疏水性导致无法直接偶联抗体的困难,并赋予ADC更强的旁观者效应和肿瘤浸润能力。相关研究成果被发表在《Cancer Discovery》(IF=38.272)上。
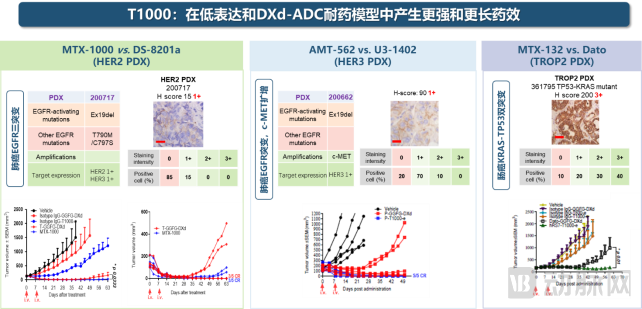
根据此前的披露,ADCE-T02在卵巢癌、膀胱癌、肺癌和宫颈癌的多种CDX和PDX模型中均表现出显著疗效。另外,ADCE-T02已在澳洲申报进入临床试验,预计将于近期申报美国IND。
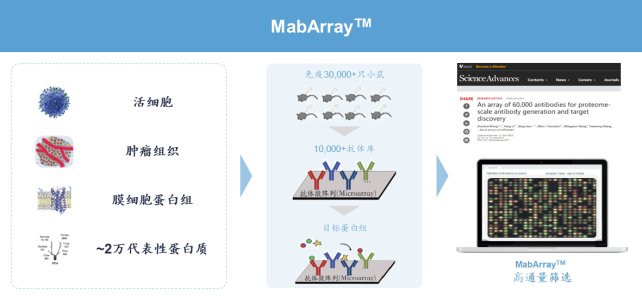
此外,普众发现还有另一核心技术平台——MabArray工业级抗体芯片平台。凭借10万级超高密度抗体芯片库,可以实现传统方法无法完成高分辨率抗原筛选,并识别高难度抗原如多次跨膜,特殊构象,糖蛋白等,一次性覆盖人类细胞表面膜蛋白(潜在药靶)~50%,推动细胞表面抗原识别抵达新境界。
今年初,普众发现还与ADC CDMO龙头药明合联达成了基于T-Moiety的合作,致力于构建更高效的ACD研发平台。
多款ADC药物进入临床,中美澳同步推进
此前授权昂阔医药的CDH6 ADC药物AMT-707(现称为CUSP06)已经证明了普众发现两大核心技术平台的实力。2024年初,昂阔医药宣布完成1亿美元的A轮融资,用于推进其核心管线CDH6 ADC的研发——该条管线便来自于普众发现。目前,CUSP06 已于2023年第三季度获得美国 FDA 临床试验许可,并正在美国启动I 期临床试验。
自2019年创办以来,普众发现共完成4轮融资,投资方包括默克投资、凯风创投、北极光创投等。据公开信息,普众发现多个ADC药物已在中美澳同期进入临床,涉及靶点包括FRα、HER3、PTK7、MUC18和CDH6。除已将大中华区以外独家开发和商业化权利授权昂阔医药的AMT-707外,普众发现还有三款已进入临床的ADC管线。
AMT-151
AMT-151靶向叶酸受体α(FRα),目前已经在中澳获批临床试验。AMT-151抗体为普众发现自主研发的重组人源化抗体,payload为新型毒素分子DUO-5,linker则采用联宁K-lock定点偶联技术。
ImmunoGen公司开发的ELAHERE®(mirvetuximab soravtansine-gynx)是首款且目前唯一获批上市的靶向FRα的ADC药物,于2022年11月获得FDA加速批准,用于治疗接受过1至3种疗法的FRα阳性、铂耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌患者。2020年,华东医药以3.05亿美元获得了该药在大中华区的独家临床开发及商业化权益。
AMT-253
AMT-253靶向MUC18,由人源化的抗MUC18 IgG1抗体和拓扑异构酶I抑制剂exatecan通过自降解T连接子偶联而成,具有较高的治疗指数和良好的药代动力学特性。目前已经取得CDE临床试验默示许可。
在临床前研究中,AMT-253展现出了对MUC18阳性肿瘤细胞的特异性细胞毒性,通过DNA损伤和凋亡机制发挥作用,并具有强大的旁观者效应,导致对黑色素瘤细胞系和患者衍生的异种移植模型产生强大的抗肿瘤活性。
AMT-562
AMT-562靶向HER3,由一种新型的抗HER3抗体Ab562和一个改良的自毁PABC间隔基(T800)构成,用于将细胞毒性药物exatecan偶联到抗体上。
在低HER3表达的异种移植和异质患者衍生的异种移植/类器官模型中,无论是单药还是联用,AMT-562都显示出了有效且持久的抗肿瘤反应。此外,与Patritumab-GGFG-DXd相比,AMT-562在药代动力学和安全性方面表现出更好的特性,并且在食蟹猴中最高剂量为30 mg/kg时没有严重毒性。
Adcendo ApS:全力推进uPARAP ADC,与映恩生物合作
Adcendo ApS于2017年由哥本哈根大学和Rigshospitalet的科学家团队创立,专注于开发用于治疗癌症的ADC药物。至今为止,Adcendo ApS 已经完成了3轮融资,总金额达到9800万欧元,投资机构包括Gilde Healthcare、Novo Holdings、RA Capital Management等。
Adcendo ApS目前唯一的管线是一款靶向uPARAP受体的ADC。uPARAP是一种在多种间质性癌症中高度表达的细胞表面受体,包括软组织肉瘤、骨肉瘤、胃肠道间质瘤(GIST)以及恶性胶质瘤(如胶质母细胞瘤)等。
Adcendo ApS的uPARAP靶向ADC在临床前模型中显示出了对胶质母细胞瘤(glioblastoma multiforme, GBM)的强大抗肿瘤活性,并且在体外对GBM癌细胞表现出细胞毒性。这些数据表明,uPARAP靶向ADC可能是GBM患者的潜在新型治疗选择。
2023年,Adcendo ApS与国内ADC药企映恩生物就ADC技术平台达成合作,获得映恩生物独创的肿瘤 ADC平台 “DITAC” 技术许可,用于其治疗间叶组织肿瘤的 uPARAP ADC 项目。四个月后,双方扩大了合作范围,Adcendo ApS将获得针对两个指定创新靶点基于DITAC平台开发 ADC的选择权。
从2023年末至今,BD已经成为了中国创新药企“回血”的主要来源,ADC更是其中的大热项目。2024年上半年,全球ADC领域的交易额显著增长,已公开披露的总交易额超过160亿美元,同比去年增长65%。这之中,中国企业参与了近半的交易。
参考文章:
普众发现,越低调成功?bioSeedin柏思荟





























