近年来,随着利拉鲁肽、司美格鲁肽等“重磅炸弹”药物陆续上市,多肽赛道正重回大众视野。
2021年,Linzess®(利那洛肽)在美净销售额超10亿美元,成为多肽药物领域新的一枚“重磅炸弹”药物。
该药早在2019年就获得我国NMPA批准,用于治疗成人IBS-C 患者,填补了我国成人IBS-C的治疗空白。
利那洛肽是由Ironwood研发的全球首个鸟苷酸环化酶‐C(GC-C)激动剂,一直是便秘治疗领域品牌药处方市场的领先者,代表着Irowood在肠胃(GI)领域的最高成就。
Irowood已在美国、欧洲、日本、中国等地为利那洛肽的全球化销售搭建了强健的合作网络,同时也在积极研下一代GI创新管线,旨在成为美国领先的GI医疗保健公司。
Ironwood拥有30多年的发展历史,行业经验丰富。其前身是由美国麻省理工怀特海研究所(Whitehead Institute)于1988年成立的Microbia。经过多年的发展,Ironwood于2010年2月成功登陆纳斯达克,代码为IRWD。
Ironwood备受资本青睐。据不完全统计,自成立以来,Ironwood已经完成超10轮融资,融资总额超6亿美元。
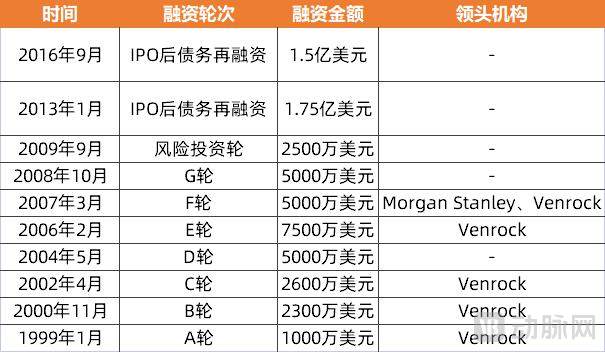
数据来源:crunchbase
除了悠久的历史和较强的融资能力,Ironwoo最为人所知的是其销售冠军产品——利那洛肽。
利那洛肽是全球首个鸟苷酸环化酶‐C(GC-C)激动剂,可通过激活GC-C受体,升高胞内环鸟苷酸(cGMP)浓度,促进肠液分泌,改善变异;同时也可升高胞外cGMP浓度,降低痛觉神经活性,环节腹痛,具有增加肠液分泌/运输,和降低疼痛神经敏感性的双重机制。
,
利那洛肽在2012年8月被美国FDA批准用于治疗成人慢性特发性便秘(chronic idiopathic constipation,CIC)和成人便秘型肠易激综合征(IBS-C);2017年,FDA批准72微克 LINZESS(利那洛肽)用于CIC治疗。截至目前,利那洛肽已获美国FDA批准3种剂量:290微克用于IBS-C成人患者的治疗,145微克和72微克用于CIC成人患者的治疗。
除了美国,利那洛肽还在日本、中国、加拿大等超40个国家上市,销售网络遍布全球。
2019年1月,利那洛肽获得我国NMPA批准,用于治疗成人IBS-C 患者,并于当年11月正式在中国上市,填补了我国成人IBS-C的治疗空白。中国Ⅲ期临床试验证实,与安慰剂组相比,利那洛肽可显著缓解IBS-C相关症状,其缓解程度反应者比例是安慰剂组的两倍以上(31.7% vs 15.4%),疗效在治疗第一周就有体现,并在整个治疗期间症状都得到了改善。此外,由于利那洛肽作用于肠道局部,几乎不吸收入血,其安全性更为良好。研究显示,利那洛肽最常见的不良反应为轻度和中度腹泻,未见临床显著后遗症。
为了进一步推广利那洛肽在全球的应用,Ironwoo和众多大型药企建立了合作关系。在北美和欧洲地区,Ironwood和艾伯维(AbbVie)合作销售利那洛肽(美国品牌名Linzess,欧洲品牌名Constella);在日本,则由安斯泰来(Astellas)负责利那洛肽的开发和商业化;阿斯利康(AstraZeneca)则是Ironwood在中国市场的合作伙伴。
但整体来看,利那洛肽的销售市场还是以美国为主。2021年,利那洛肽(Linzess)在美净销售额突破10亿美元大关,成为同行中的一枚“重磅炸弹”,为Ironwood带来了巨额的销售收入。据IQVIA数据,2021年Linzess的处方总需求达到了1.59亿粒LINZESS胶囊。
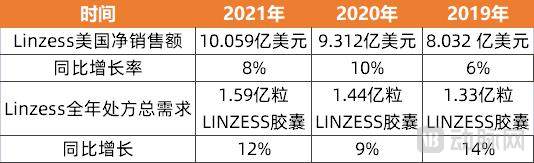
Linzess美国净销售额及全年处方总需求(数据来源:Irowood年报)
在搭建全球销售网络的同时,Ironwood也在积极选拔符合公司未来商业化战略的人才。
2021年6月,Thomas McCourt正式成为Ironwood新任首席执行官和董事会成员。Thomas McCourt拥有丰富的营销和商务拓展经历,他于2009年正式加入公司,曾担任营销高级副总裁、首席商务官、临时首席执行官等职位;在加入Ironwood之前,他曾在Amgen领导denosumab的美国品牌团队、在诺华(Novartis AG)负责ZELNORM™的推广,也曾是Astra Merck的创始团队成员,担任PRILOSEC®和NEXIUM®的品牌经理。
目前Linzess仅适用于18岁以上成人患者,但实际上仍有大量儿童患有功能性便秘(FC)。为了满足更多患者的临床需求,Ironwood正在积极拓宽Linzess的可使用年龄范围。2022年9月,Irowood宣布,Linzess在6-17岁功能性便秘患儿中的III期临床试验满足了主要和次要终点。目前FDA还没有批准功能性便秘(FC)的儿童处方疗法,Linzess有望成为首个。
Irowood致力于重新定义胃肠道(GI)疾病患者的护理标准。为了加强在GI领域的创新能力,除了CIC和IBS-C,Irowood正在积极拓展适应症范围,并产生了多条药物研发管线,其中IW-3300和CNP-104这两个管线产品尤其值得关注。

产品介绍(图片来源:Irowood官网)
IW-3300是一种鸟苷酸环化酶- c激动剂,用于潜在的内脏疼痛疾病的治疗,例如间质性膀胱炎/膀胱疼痛综合征(IC/BPS)和子宫内膜异位症,这些疾病在美国影响着数百万患者。Ironwood已经成功完成了I期研究,预计在2022年底前启动IC/BPS患者的II期概念证明研究
CNP-104是一种耐受性免疫修饰纳米颗粒,用于治疗原发性胆道胆管炎(PBC),这是一种罕见的针对肝脏的自身免疫性疾病。Ironwood已与生物制药公司COUR签署了合作和许可选项协议,获得了在美国研究、开发、生产和商业化含有CNP-104的产品的独家许可。目前,FDA已经授予了CNP-104快速通道指定,Ironwood预计在2023年公布数据,如果研发成功,CNP-104有可能成为第一个被批准的PBC疾病修饰疗法。
Irowood长期专注于GI领域,2021年全年总收入为4.004亿美元,是GI领域不可忽视的实力选手。凭借着多肽药物利那洛肽持续强劲的市场需求,Irowood计划在2022年实现利那洛肽在美国净销售额个位数增长,并将营收保持在4.2亿至4.3亿美元。




























