2022年2月14日,北京泽辉辰星生物科技有限公司(以下简称泽辉生物)研发的多能干细胞来源的细胞药物注射液(受理号CXSL2101443)正式获得国家药品监督管理局药品审评中心(CDE)的临床试验默示许可,临床研究适应症为急性呼吸窘迫综合征(ARDS)。此前该在研药物还先后获得药监局批准开展治疗新冠肺炎导致的ARDS、新冠肺炎相关的肺纤维化以及半月板损伤的药物注册临床试验。
“截至2022年4月底,国内获得药监局批准的干细胞药物注册试验有36项,除泽辉生物在研药物和另外一家企业新获批的多能干细胞(pluripotent stem cell,PSC)试验药物外,其它所有申办方的在研药物都是不同组织来源的成体干细胞(somatic stem cell,SSC)制剂。泽辉生物是中国最早获批开展注册临床试验的多能干细胞制药企业,并且也是唯一一家正式开展多能干细胞注册临床试验的制药企业。”泽辉生物首席医学官(CMO)贾懿博士解释道,早在2020年2月,泽辉生物的一款细胞注射液就已经获批并开展注册临床试验。
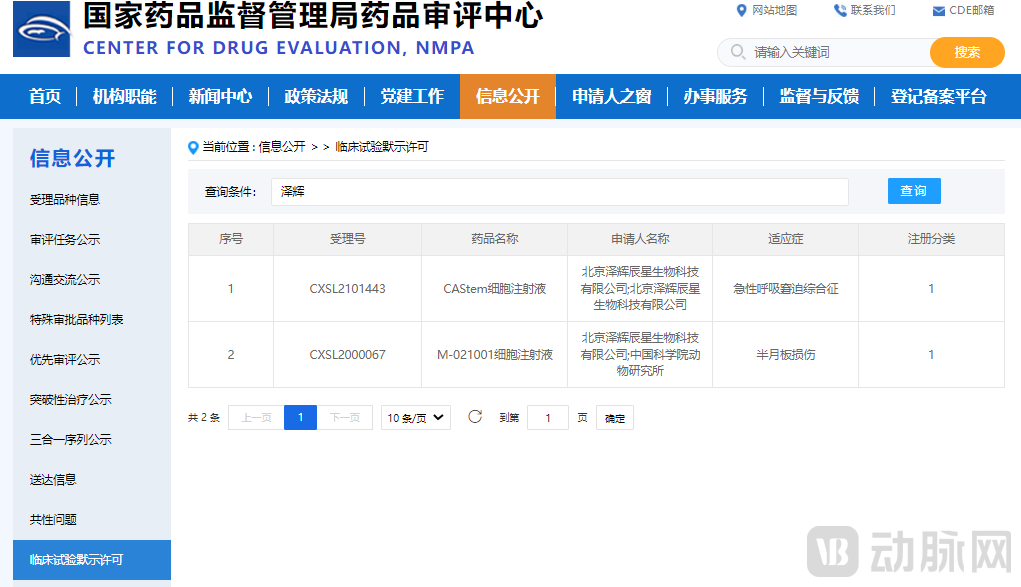
泽辉生物获临床试验默示许可的在研药物
干细胞领域正在飞速发展,根据Transparency Market Research报告,到2025年底,全球干细胞市场规模预计达到2705亿美元,2017年-2025年的年复合增长率有望达到13.8%。
据全球企业增长咨询公司弗若斯特沙利文(Frost&Sullivan)最新报告,在全球范围内,已有14款干细胞产品在不同国家获批上市,且均来源于成体干细胞。据贾懿博士介绍:“不同于各类人体组织来源的成体干细胞药物,泽辉生物的多能干细胞来源的细胞药物,是以人胚干细胞为种子细胞,通过定向分化获得特定类型的功能细胞,与辅料配制成即用型(off-the-shelf)细胞药物,这在干细胞成药研发方面有着特殊的优势。”
多能干细胞成药尤其是人胚干细胞来源的细胞药物成药具有哪些优势?泽辉生物将如何为干细胞药物研发痛点提供新的解决方案?
目前全球范围进入药物临床试验阶段的治疗类干细胞产品主要包括多能干细胞来源的细胞药物和人体组织来源的成体干细胞药物。其中多能干细胞主要包括人胚干细胞(human embryonic stem cell,hESC)和诱导多能干细胞(induced pluripotent stem cell,iPSC)。泽辉生物在人胚干细胞和iPSC的研究应用均有布局,目前主要专注于基于人胚干细胞的细胞药物研发。
据贾懿博士介绍,从2009年至今,已在国外上市销售的多款以间充质干细胞为主的成体干细胞药物都没能实现大范围商业推广和临床应用,主要原因是成体干细胞的特性所限:一是间充质干细胞增殖能力有限,供体单次取材难以满足大规模商业化生产需求;二是不同供体来源的细胞存在生物特性差异,导致不同供体批次细胞制剂在临床疗效上可能存在差异。
多能干细胞来源的细胞药物研发首先需要建立一个稳定的多能干细胞系,无论是基于受精卵的人胚干细胞系,还是成体细胞人工诱导后形成的iPSC细胞系,多能干细胞系都是基于单细胞克隆技术,通过扩增后形成的单克隆细胞系,所有细胞来源于一个共同的祖先细胞,细胞基因型和细胞表型保持高度一致,从源头上保证细胞药物生产用起始物料的均一性,确保最终生产得到的不同批次细胞产品的生物特性和临床疗效一致。
此外,多能干细胞在体外具有自我更新和无限扩增的特性,为后续功能细胞分化提供充足的种子细胞,辅以成熟的体外扩增培养和诱导分化技术,以及标准化的生产工艺和质量控制策略,最终能够实现多能干细胞药物的规模化生产和广泛临床应用。
同时,泽辉生物考虑到,采用人胚干细胞系作为种子细胞,能够避免因重编程过程带来的药物安全性评估的不确定性,也避免相对繁杂的工艺流程,在现阶段是个最优化选择。
虽然相比成体干细胞,基于多能干细胞的细胞药物在成药研发上受限较少,但成体干细胞来源多样,供体组织分离、培养、扩增等方面工艺简洁,从获取供体组织到完成细胞制剂,整个流程工艺简便易控;而多能干细胞来源的细胞药物制备需要先建立一个多能干细胞系,例如人胚干细胞系,其工艺要求相对较高,存在一定的技术壁垒。因此,自上世纪九十年代,国外最早开始干细胞临床研究所采用的,都是不同组织来源的成体干细胞制剂,随后基于这些研究,陆续有几款干细胞药物获批上市。国内干细胞药物研发的情况也类似,目前绝大部分企业都投入到成体干细胞成药赛道,国内外真正涉足多能干细胞的企业还比较少。
“我们不希望跟在别人后面,而希望做真正的原研创新药。”怀着这样的愿景,2019年5月,泽辉生物和中国科学院干细胞与再生医学创新研究院(中国科学院动物研究所)签署了战略合作协议,共同研发拥有自主知识产权的多能干细胞药物。基于中科院干细胞与再生医学创新研究院的人胚干细胞系,泽辉生物已从“细胞产品批间一致性”以及“干细胞药物规模化生产”两方面解决了干细胞药物研发的痛点。
目前,国内已有多家企业布局干细胞药物领域,行业整体欣欣向荣。相较于其他企业而言,泽辉生物拥有自己独特的适应成药研发需求的布局。
团队成员拥有多年药物开发及干细胞研究的经验。
泽辉生物组建了一支具备优秀教育背景和丰富工作经验的团队。公司核心团队成员均取得国内外知名高校博士学位,是专家教授级人才,拥有海外留学和工作的经历,主要成员长期在大型跨国制药企业中担任高级研发和管理岗位。比如贾懿博士本人,有十余年的外科临床工作经验,随后在跨国药企负责在中国以及亚太多个国家开展生物药物、化药、药械结合产品的临床研发工作近十年。在加入泽辉生物并担任CMO职务后领导并完成国内第一个多能干细胞来源细胞产品的新药注册临床试验申请批准。在2020年初的新冠疫情期间,开展了世界上首个采用人胚干细胞来源细胞制剂治疗新冠肺炎相关疾病的注册临床试验。
核心技术具备成药和应用前瞻性。
第一,细胞制剂生产全流程中实现了无血清培养。血清成分多样,能够提供生长因子、激素、蛋白质、维生素等细胞成长所需的营养物质,但所有人或动物来源的物质,成分都是复杂不清的,最终成药的产品存在潜在外源因子污染风险。监管部门要求在细胞生产用原材料中尽可能采用成分明确的培养基组分。“基于前期大量的基础研究,目前泽辉生物的多能干细胞已经实现无血清扩增,其定向分化的功能细胞在整个生产工艺中通过使用成分限定的血清替代物,最大程度上规避了血清带来的安全性风险,打破了成药的技术瓶颈。”贾懿博士介绍道。
第二,在干细胞成药的过程中没有采用任何基因修饰技术。基因修饰细胞相对来说在成药过程中需要提供更多的安全性评价与质量保证,而泽辉生物基于人胚干细胞的细胞药物则完全规避了这一风险,也在一定程度上加快了研发进展。
第三、定位于即用型干细胞药物。为了维持细胞活性和功能,需要采用液氮进行超低温长期保存,在临床使用前把细胞药物从液氮中取出,细胞复苏后进行给药。贾懿博士介绍说:“目前干细胞制剂在临床使用操作仍存在差异,有些企业研发的干细胞制剂在使用前从液氮复苏后需要较长时间的体外培养,甚至涉及细胞传代,可能需要两三天甚至1周以上,以达到临床所需的细胞数量和细胞活性,这给药物上市后临床广泛应用带来了困难。而泽辉生物研发的细胞药物始终坚持即用型(off-the-shelf)策略,即医护人员只需在患者使用前花2-5分钟,通过定制的细胞复苏仪进行细胞解冻复苏,随后即可配制成细胞注射液完成临床给药,类似于临床常规药物的使用操作,非常方便。”
已建立完善的CMC研发技术平台和质量管理体系。
泽辉生物已经建立了多能干细胞二级生产用细胞库,掌握了多能干细胞向内胚层、中胚层和外胚层细胞定向分化技术,相继建立多能干细胞及其衍生细胞基于scale-out和scale-up的规模化扩增技术、制剂处方和工艺开发技术和基于off-the-shelf细胞制剂的程序降温技术等工艺平台,及其质量评价技术平台。
泽辉生物还开发了首个人胚干细胞来源M细胞药物标准化、规模化、易于放大的生产工艺;批产细胞不少于1010个,制剂批产千余支;覆盖货架期超过2年。按已建立的人胚干细胞生产用细胞库规模计算,足以支持数亿支细胞制剂的商业化生产。
此外,泽辉生物已经在北京中关村科技园建成了2400平方米的cGMP生产基地,从设计、施工到运行都达到了国际细胞治疗产业的先进标准。公司已建立有效的质量管理体系,该体系涵盖影响临床试验用药物质量的所有因素,包括厂房、设备设施、人员、生产、检验、储存及运输全链条、完备文件系统等各方面。
泽辉生物的干细胞药物研发进展迅速,目前已经有4项I至II期的注册临产试验获药监局批准,其中2项关于治疗新冠相关疾病的I/II期试验已完成;1项关于治疗半月板损伤的试验已于2022年3月正式启动;1项关于治疗ARDS的试验计划于2022年中启动。
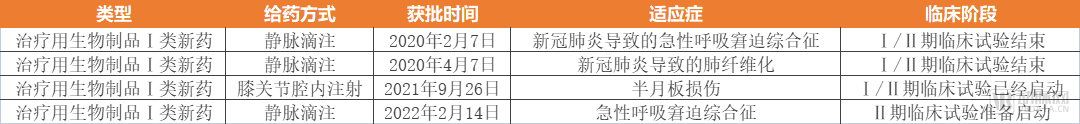
泽辉生物获批注册临床试验的4类适应症
据悉,泽辉生物已计划布局更多适应症研发,如炎症性肠病、急性移植物抗宿主病、中重度宫腔粘连、难治性创面等,以及干细胞和不同材料复合的药械结合产品研发。同时还计划开发基于人胚干细胞的不同功能细胞,例如视网膜色素上皮细胞的细胞药物等,用于目前尚未被满足的临床治疗需求。
提到公司未来规划,贾懿博士表示:“短期内,希望能够尽快完成第一款产品的获批上市,让中国患者能够尽早用上泽辉生物普适型、即用型的多能干细胞药物。”
泽辉生物已经打通了基于多能干细胞药物从科研到临床的技术壁垒,正走在通往干细胞药物产业化的道路上。相信在泽辉生物的引领带动下,不久的将来,多能干细胞这个细分赛道将成为细胞药物的新蓝海。





























