如果说1类新药的价值是从0到1,那2类创新药就是从1到N。
一个有效成分可以开发出多个新药。例如布洛芬(Ibuprofen)是一种常用解热镇痛类,非甾体抗炎药, 分子式为C13H18O2,最早于1968年在英国上市,由Boots公司开发,商品名Brufen TM。由于其疗效好,副作用小,很多跨国公司基于其有效成分开发了很多新药,如GSK的芬必得布洛芬缓释胶囊、强生的美林布洛芬缓释片、ABBOTT的布洛芬混悬剂、艾伯维的布洛芬-重酒石酸氢可酮复合片剂、Horizon的布洛芬-法莫替丁复合片剂,还有其它公司开发的布洛芬分散片、布洛芬咀嚼片、布洛芬静脉注射剂等,这些都是改良药。
改良药在国内也称之为2类创新药,在国内外都有很多成功的案例。例如硝苯地平从普通制剂变成缓控释新药之后,在国内的年销售额达48.9亿元;非洛地平从普通制剂变成缓控释新药之后,在国内的年销售额达17.8亿元;美托洛尔缓释片作为美托洛尔的迭代产品,在国内的年销售额达23.4亿元;国外的舒利迭(Advair Diskus)年销售额是45亿美元;紫杉醇白蛋白纳米粒年销售额为10亿美元;盐酸羟考酮缓释片年销售额是24亿美元;右哌甲酯缓释胶囊年销售额是13亿美元。
改良药是在已知药物活性成分的基础上,通过更改酸根/碱基、新的剂型/新的给药方式、新复方制剂、新的适应症等方面对现有药物进行二次开发,满足还未满足的临床需求,让更多患者从药物中获益。并且,相较于NCE类新药,改良药具有研发周期相对短、风险相对低、投入相对少、成功率相对高等一系列特点,也使得其研发收益比起NCE类新药来不遑多让。
2016年,参考FDA的NDA 505(b)(2),NMPA发布了《化学药品注册分类改革工作方案》。《方案》中重新调整了化学药品注册分类类别。在新分类中,“改良药”的官方名称是“2类创新药”, NMPA强调中国的二类新药并不完全和NDA 505(b)(2)等同,具有中国特色。
近年来,随着2类创新药相关的政策逐渐明晰化,国内2类创新药注册热度迅速蹿升。据新浪医药百家号显示,过去三年2类创新药的总受理号承办数量由2019年188条上升到2021年418条,年增长率近49%;其中,新药临床许可承办数量,由2019年141条上升到2021年304条,年增长率近47%。1
2类创新药的火爆程度可见一斑。
巨头纷纷布局,
成功案例数不胜数
2类创新药之所以备受欢迎,是因为相比于1类新药广为流传的“二八定律”、“双十成本”等高风险,2类创新药由于简化了基础药物研发和临床试验,资金投入更少,研发周期也相对短。并且在新剂型药物的基础上,还可以通过继续对产品进行剂型上的持续升级来不断延长药物寿命。这一系列特点决定了改良药“收益高,生命周期长”的优势。
由于已经有了原研药物的市场基础,2类创新药凭借临床优势,在药物研发阶段就可以对药物未来的市场潜力做出相对明确的预判。
强生的利培酮就曾通过多次剂型升级的方式持续“延寿”。强生在利培酮的基础上对剂型进行了多次改良,共推出了五款不同剂型的同类产品。因此在利培酮常规制剂专利到期之后,强生在利培酮方面的业务几乎没有受到影响,改良型利培酮的产品仍旧占据着大量的市场份额。拜尔出品的拜新同也是改良药成功的典型案例之一。硝苯地平是拜尔的一代普通制剂,拜尔在硝苯地平化合物专利到期之后推出了其二代产品硝苯地平控释片—拜新同。拜新同通过改变药物剂型的方式达到缓释效果,并迅速在市场上置换掉了硝苯地平。直到今天拜新同仍是全球范围内最热门的降压药之一。
在大型药企身上,类似利培酮和硝苯地平这样的案例数不胜数。辉瑞的托法替尼、西地那非;诺华的妥布霉素;默克的二甲双胍;GSK的安非他酮等等,都曾以改良药的方式成功延寿。研发改良药让这些大型药企能够以较少的投入长期占据特定适应症领域的优势地位,几乎不受专利悬崖影响。
“由于医生和患者对原研药已经有了明确的认知,2类创新药在投入市场后学术推广的成本也大大降低。只要医生和患者了解到2类创新药相比于第一代产品的临床优势,很快就会转而选择具有显著临床优势的2类创新药。”越洋医药创始人、董事长兼CEO闻晓光博士说。
大型药企与小型平台技术药企站在同一起跑线上,
共切国际市场蛋糕
所以,无论是病人所受到的临床益处,还是药企在资金、时间、风险等方面的投入与控制,2类创新药都是一个不错的选择。在这方面,大型药企具有丰富的资源和管线,留给小型平台技术药企的机会是否不多?
闻晓光博士曾先后在GSK和辉瑞参与多个缓控释新药产品的开发。他告诉动脉新医药采编,他在GSK任职的时候曾被小型平台技术药企抢过先:“当时我们公司分布在英国、美国、加拿大三个国家的四个研发团队都在同时开发同一个产品的缓控释新药,同时还有其他三家小型平台技术药企也在开发同一个产品。对大型药企来说,新药来源于内部研发(R&D)和外部购买(BD),因此公司内外部的产品同时进入临床研究,几番临床试验下来,最终一个法国小型平台技术药企的产品胜出,‘打败’了我们。”
大型药企的药物管线丰富,这既是优势,也是劣势。由于大型药企要同时兼顾的管线数量过多,他们无法在每个管线的开发上都投入大量的精力。再加上目前大型药企的药物管线来源逐渐从自研向收购迁移,R&D部门持续缩水,导致大型药企自己推出二代产品的效率越来越低。这也为研发改良药的平台技术药企提供了大量的机会。并且对于研发改良药的平台技术药企来说,产品上市只是他们的选择之一,寻求大型药企的收购也是一种很好的选择。
比起一代产品,改良药在患者依从性上一般都会有明显的提升。医生和患者在了解了改良药的优势后,很快就会放弃一代产品转而使用改良药。比如有了硝苯地平缓释片后大部分患者会选择缓释片而非普通片,有了布洛芬缓释胶囊后大部分患者会选择缓释胶囊而非普通制剂……因此改良药产品大多有能力在3-5年内取代一代产品,成为新的市场宠儿。
目前,国内的2类创新药研发处于起步阶段,市场上涉足的企业主要可分为两类:一类以恒瑞医药、正大天晴为代表具有一定规模的传统企业;另一类以越洋医药、力品药业为代表新型药物平台的创新型公司。其中,国内2类创新药临床试验许可获批最多的企业为恒瑞医药,其次为正大天晴,第三是越洋医药,第四是力品药业,另外,江苏豪森、石药集团、东阳光等企业均有获批2类创新药临床试验许可。
但改良药并不仅是在和一代产品分蛋糕,除了可以覆盖原研药的市场空间,它还有能力扩大市场空间。改良药可以通过解决临床上未被满足的需求,在原本适应症的基础上拓宽适应症或适应患者的范围,把“蛋糕”做大。
“比如我们自主研发的产品‘维压®”,就是将地平类产品做成缓控释解决辰时高血压的问题。”闻晓光博士继续说,“临床上大约有1/4的高血压患者在早上7-9点会有一个血压高峰,也就是辰时高血压的症状。这个适应症目前在临床上还没有合适的药物用以治疗。‘维压®’会在患者服药后的第二天早上释放,从而防止患者早上出现的血压峰。通过这样的新剂型药物,我们就解决了一个未被满足的临床需求,抢占其它非地平类降压药的市场,从而把地平类降压药这块‘蛋糕’做大了。”
越洋读书,越洋工作,
越洋回国创业,技术和产品越洋走向全球
闻晓光博士说,他自己创业的想法其实由来已久了:“我们的缓控释新药被那家法国公司打败的时候,当时我觉得非常有挫败感,觉得就像比赛输了一样,但同时我也觉得缓控释新药这个事情,自己也可以做。所以从那个时候开始,我就萌生了出来创业做缓控释新药的念头。”
回国后,闻晓光博士曾担任科技部制剂新技术国家重点实验室主任(扬子江药业承载),在此期间有机会向有关部门呼吁参照NDA 505(b)(2)调整中国新药分类策略,明确改良药的新药地位。
2011年底,闻晓光博士创办了越洋医药。“我们越洋留学读书,又越洋回来创业,将来还要让我们的新药产品越洋销售全球。因此,公司起名越洋医药。”闻晓光博士说。

实验室里的闻晓光博士,图源越洋医药提供
越洋医药在最初成立的时候经历过一个非常艰难的阶段,当时国家还没有明确2类创新药的分类,对NDA 505(b)(2)感兴趣的投资机构几乎没有。2016年新的药品分类出台以后,越来越多的投资者关注到2类创新药领域,融资环境发生了非常大的变化,受到国内多家投资机构认可和支持,两年前完成了3.3亿新一轮的融资,目前的股东包括九洲药业、广发乾和、川创投、越秀产业基金、横琴乐三伍号、拓金资本、上海医药、华美集团和乾道集团等。
在资本的支持下,越洋医药迅速发展,目前已经在管理团队中聚集了6名全职欧美海归博士。这些核心团队成员曾在国外的大型药企从事新药和仿制药产品开发工作,对改良药的研发和上市过程非常熟悉。
30个新药获批中国和美国临床试验许可,
1个新药开展国际多中心III期临床,
1个缓控释产品美国获批上市
目前,越洋医药18个口服缓控释新药在中国(包括中国台湾)获批临床试验许可(IND)(约占CDE公布总数的50%,遥遥领先),12个新药在美国获批临床试验许可(IND)。此外,越洋医药已完成15个新药的动物药代动力学研究,已完成30多个新药的人体药动学研究,试验结果均达到预期,大大降低了下一阶段药物开发的风险。其中,新药“维安”已在美国等地开展500多名患者的国际多中心III期临床试验,另有多个新药在进行NDA批次生产,生产完成后将进入efficacy试验。
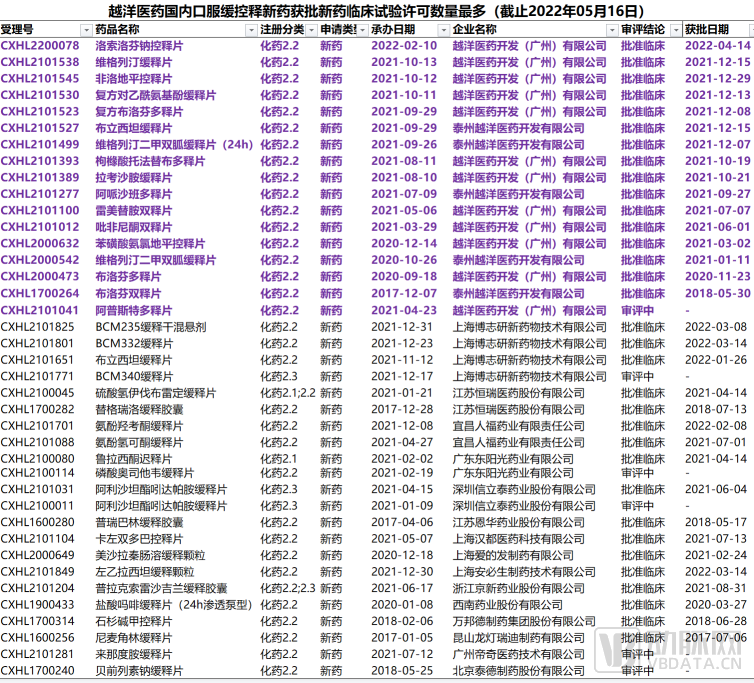
越洋医药国内口服缓控释新药获批新药临床试验许可数量最多
(截止2022年5月16日,图源越洋医药提供)
2021年12月,越洋医药成功举行了左乙拉西坦缓释片出口美国的首次发货仪式。闻晓光博士表示:“越洋医药的缓控释产品首次发货美国标志着公司实现了产品越洋零的突破。这是公司轻资产重技术、自主研发、委托生产战略的一次成功验证。这次发货以及随后的销售意义重大,它标志着公司实现了从研发到销售的闭环,标志着公司从创新型研发企业向商业化制药企业的转型。”
由于越洋医药2类创新药的开发处于领先地位,被中国化学制药工业协会推荐为二类新药专委会主任单位,也获得了业内很多赞誉和认可。但在闻晓光看来,“数量最多只能代表我们赢在了起跑线,我们的目标是赢在终点线,需要更多的支持和合作。”
越洋医药计划今年多个新药进入NDA注册批生产阶段,明年多个新药进入三期临床,未来几年还有更多储备的管线进入NDA申报阶段,希望能够通过募集更多资金以及与企业合作开发的方式将更多的新药产品成功推上市场,为人类健康提供解决方案。
参考文献:1新浪医药,《新浪医药年度盘点丨2021年化药2类改良型新药迎研发高潮》。





























